- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
МЕТОДЫ КЛИНИЧЕСКОГО ИССЛЕДОВАНИЯ 5 страница
|
№ 34 Гипертермические состояния: причины, стадии и общие механизмы развития. Отличие экзогенной гипертермии от лихорадки.
ГИПЕРТЕРМИЯ - типовая форма расстройства теплового обмена, возникающая в результате действия высокой температуры окружающей среды и/или нарушения процессов теплоотдачи организма; характеризуется нарушением (срывом) механизмов теплорегуляции, проявляется повышением температуры тела выше нормы. Причинами гипертермии являются: • высокая температура окружающей среды; • агенты, препятствующие реализации механизмов теплоотдачи организма; • разобщители процессов окисления и фосфорилирования в митохондриях Стадии гипертермии . Гипертермия, как правило, процесс стадийный. При действии гипертермического фактора в организме включается триада экстренных адаптивных реакций: 1) поведенческая («уход» от действия теплового фактора); 2) интенсификация процессов теплоотдачи и снижение активности теплопродукции; 3) стресс-реакция. В ходе развития гипертермии условно выделяют две основные стадии: компенсации (адаптации); декомпенсации (деадаптации) механизмов терморегуляции организма. Иногда выделяют финальную стадию гипертермии — гипертермическую кому. Механизм развития гипертермии включает комплекс адаптивных и патогенных реакций организма. На начальной стадии доминируют первые, на последующих (если компенсаторные и защитные реакции оказались недостаточными) — преобладают процессы повреждения. На каждой из стадий гипертермии в организме развиваются характерные метаболические, физико-химические, структурные и функциональные изменения. Стадия компенсации характеризуется активацией экстренных механизмов адаптации организма к перегреванию. Эти механизмы направлены на увеличение теплоотдачи и снижение теплопродукции. В результате температура тела хотя и повышается, но остаётся в пределах верхней границы нормального диапазона. Проявления гипертермии в значительной мере определяются температурой окружающей среды. Стадия декомпенсации характеризуется срывом и неэффективностью как центральных, так и местных механизмов терморегуляции, что и приводит к нарушению температурного гомеостаза организма. ТЕПЛОВОЙ УДАР. Тепловой удар — своеобразная форма гипертермии. Это своеобразие заключается в остроте развития гипертермии с быстрым достижением опасных дляжизни значений температуры тела (ректальной) 42-43 °С. Другими словами, тепловой удар — следствие быстрого истощения и срыва приспособительных процессов, характерных для стадии компенсации гипертермии. Причины. Действие теплового фактора высокой интенсивности; Низкая эффективность механизмов адаптации организма к повышенной температуре внешней среды. Патогенез. Перегревание организма после кратковременной (иногда клинически не определяемой) стадии компенсации быстро приводит к срыву механизмов терморегуляции и интенсивному нарастанию температуры тела. Последняя имеет тенденцию приближаться к температуре внешней среды. Следовательно, тепловой удар — гипертермия с непродолжительной стадией компенсации, быстро переходящая в стадию декомпенсации. Последствия. Смерть пациентов при тепловом ударе является результатом острой прогрессирующей интоксикации, сердечной недостаточности, остановки дыхания. СОЛНЕЧНЫЙ УДАР. Солнечный удар, являясь одной из форм гипертермических состояний, имеет ряд отличий от гипертермии как по причине, так и по механизмам развития. Причина. Причиной солнечного удара является прямое воздействие энергии солнечного излучения на организм. Наибольшее патогенное действие, наряду с другими, оказывает инфракрасная часть солнечной радиации, т. е. радиационное тепло. Последнее, в отличие от конвекционного и кондукцион-ного тепла, одновременно прогревает и поверхностные, и глубокие ткани организма. Кроме того, инфракрасная радиация, действуя на весь организм, интенсивно прогревает и ткань головного мозга, в котором располагаются нейроны центра терморегуляции. В связи с этим солнечный удар развивается быстротечно и чреват смертельным исходом. Патогенез. Патогенез солнечного удара — комбинация механизмов гипертермии и собственно солнечного удара. Ведущими являются различные поражения ЦНС. Гипертермические реакции. Причиной гипертермических реакции являются непирогенные агенты. В основе развития гипертермических реакций обычно лежит временное преобладание теплопродукции над теплоотдачей. Механизмы терморегуляции организма при этом сохраняются. ЛИХОРАДКА Лихорадочная реакция — динамичный и стадийный процесс. По критерию изменения температуры тела выделяют три стадии лихорадки: I. подъёма температуры, II. стояния температуры на повышенном уровне и III. снижения температуры до значений нормального диапазона. I. Стадия подъёма температуры тела. Стадия подъёма температуры тела характеризуется накоплением в организме дополнительного количества тепла за счёт преобладания теплопродукции над теплоотдачей. II. Стадия стояния температуры тела на повышенном уровне. Стадия стояния температуры тела на повышенном уровне характеризуется относительной сбалансированностью теплопродукции и теплоотдачи. Однако баланс этих двух процессов достигается уже на уровне, существенно превышающем долихорадочный. Именно это и поддерживает температуру тела на повышенном (по сравнению с долихорадочным периодом) уровне: интенсивная теплопродукция уравновешивается эквивалентной ей теплоотдачей. III. Стадия снижения температуры тела до нормальной. Стадия снижения температуры тела до значений нормального диапазона характеризуется постепенным снижением продукции лейкоцитарных пирогенных цитокинов. ОТЛИЧИЯ экзогенной гипертермии от лихорадки Лихорадку следует отличать от других гипертермических состояний и от гипертермических реакций. Лихорадка • Причиной лихорадки являются пирогены. • В основе развития лихорадки лежит переход системы терморегуляции на новый — более высокий функциональный уровень. • При лихорадке сохраняются механизмы терморегуляции организма. Указанные признаки используют для дифференцировки лихорадки от качественно иного состояния — перегревания организма (гипертермии). Гипертермия • Причиной гипертермии (перегревания организма) чаще является высокая температура внешней среды. • Ключевым звеном патогенеза перегревания организма является срыв механизмов терморегуляции. От лихорадки и гипертермии необходимо отличать гипертермические реакции организма. | № 35 Гипотермические состояния: причины, стадии и общие механизмы развития. Понятие об управляемой гипотермии в медицине.
К гипотермическим относятся состояния, характеризующиеся понижением температуры тела ниже нормы. В основе их развития лежит расстройство механизмов терморегуляции, обеспечивающих оптимальный тепловой режим организма. Различают охлаждение организма (собственно гипотермию) и управляемую (искусственную) гипотермию, или медицинскую гибернацию.
Гипотермия — типовая форма расстройства теплового обмена — возникает в результате действия на организм низкой температуры внешней среды и/или значительного снижения теплопродукции в нём. Гипотермия характеризуется нарушением (срывом) механизмов теплорегуляции и проявляется снижением температуры тела ниже нормы.
Причиныразвития охлаждения организма многообразны.
• Низкая температура внешней среды (воды, воздуха, окружающих предметов и др. ) — наиболее частая причина гипотермии. Важно, что развитие гипотермии возможно не только при отрицательной (ниже О °С), но и при положительной внешней температуре.
• Обширные параличи мышц и/или уменьшение их массы (например, при их гипотрофии или дистрофии). Это может быть вызвано травмой либо деструкцией (например, постишемической, в результате сирингомие-лии или других патологических процессов) спинного мозга, повреждением нервных стволов, иннервирующих поперечнополосатую мускулатуру, а также некоторыми другими факторами (например, дефицитом Са2+ в мышцах, миорелаксантами).
• Нарушение обмена веществ и/или снижение эффективности экзотермических процессов метаболизма. Такие состояния наиболее часто развиваются при надпочечниковой недостаточности, ведущей (помимо прочих изменений) к дефициту в организме катехоламинов, при выраженных гипотиреоидных состояниях, при травмах и дистрофических процессах в области центров симпатической нервной системы гипоталамуса.
• Крайняя степень истощения организма.
Патогенез гипотермии
Развитие гипотермии — процесс стадийный. В основе её формирования лежит более или менее длительное перенапряжение и в итоге срыв механизмов терморегуляции организма. В связи с этим при гипотермии различают две стадии её развития: 1) компенсации (адаптации) и 2) декомпенсации (деадаптации). Некоторые авторы выделяют финальную стадию гипотермии — замерзание.
Стадия компенсации. Стадия компенсации характеризуется активацией экстренных адаптивных реакций, направленных на уменьшение теплоотдачи и увеличение теплопродукции.
Стадия декомпенсации (деадаптация) процессов терморегуляции является результатом срыва центральных механизмов регуляции теплового обмена.
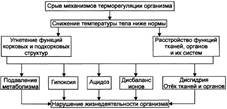 На стадии декомпенсации температура тела падает ниже нормального уровня (в прямой кишке она снижается до 35 °С и ниже) и продолжает снижаться далее. Температурный гомеостаз организма нарушается — организм становится пойкилотермным.
УПРАВЛЯЕМАЯ ГИПОТЕРМИЯ (МЕДИЦИНСКАЯ ГИБЕРНАЦИЯ) - метод управляемого снижения температуры тела или его части с целью уменьшения интенсивности обмена веществ, уровня функции тканей, органов и их физиологических систем, повышения их устойчивости к гипоксии.
На стадии декомпенсации температура тела падает ниже нормального уровня (в прямой кишке она снижается до 35 °С и ниже) и продолжает снижаться далее. Температурный гомеостаз организма нарушается — организм становится пойкилотермным.
УПРАВЛЯЕМАЯ ГИПОТЕРМИЯ (МЕДИЦИНСКАЯ ГИБЕРНАЦИЯ) - метод управляемого снижения температуры тела или его части с целью уменьшения интенсивности обмена веществ, уровня функции тканей, органов и их физиологических систем, повышения их устойчивости к гипоксии.
|
№ 36 Инфекционный процесс: характеристика понятия, этиология, общий патогенез, последствия, принципы терапии. Инфекционный процесс (инфП) — типовой патологический процесс, возникающий под действием микроорганизмов. ИнфП — комплекс взаимосвязанных изменений: функциональных, морфологических, иммунобиологических, биохимических и других, лежащих в основе развития конкретных инфекционных болезней (инфБ). Различают следующие виды инфП. • Сепсис — тяжёлая генерализованная форма инфП, обусловленная размножением микроорганизмов в крови и нередко в других биологических жидкостях организма. • Септикопиемия — инфП, характеризующийся вторичным развитием гнойных очагов в различных тканях и органах у пациентов с сепсисом. • Бактериемия, вирусемия — наличие в крови бактерий и/или вирусов без признаков их размножения. Является одним из этапов развития ряда инфП. • Микстинфекция — инфП, вызванный одновременно двумя возбудителями и более. • Реинфекция — повторное (после выздоровления пациента) возникновение инфП, вызванного тем же микроорганизмом. • Суперинфекция — повторное инфицирование организма тем же возбудителем до периода выздоровления. • Вторичная инфекция — инфП, развивающийся на фоне уже имеющейся (первичной) инфБ, вызванной другим микроорганизмом. Этиология. Условия возникновения инфекции определяются входными воротами инфекции, путями её распространения в организме, механизмами противоинфекционной резистентности. Входные ворота инфекции — место проникновения микробов в макроорганизм. Такими воротами могут быть: кожные покровы; слизистые оболочки дыхательных путей; слизистые оболочки ЖКТ; слизистая оболочка мочеполовых органов; стенки кровеносных и/или лимфатических сосудов, через которые возбудитель поступает в кровь или лимфу. Входные ворота могут определять нозологическую форму заболевания. Пути распространения бактерий . Известны следующие пути распространения бактерий в организме: по межклеточному пространству; по лимфатическим капиллярам — лимфогенно; по кровеносным сосудам — гематогенно; по жидкости серозных полостей и спинномозгового канала. Общий патогенез. ИнфП — типовой патологический процесс, основными общими звеньями развития которого являются лихорадка, воспаление, гипоксия, нарушения обмена веществ, а также расстройства функций органов, тканей и их систем. Лихорадка. Лихорадка является наиболее частым компонентом инфБ. Возбудители инфекций при помощи первичных пирогенов стимулируют синтез и высвобождение лейкоцитами вторичных пирогенов — лейкоцитарных цитокинов. Это запускает лихорадочную. Воспаление. Воспаление развивается в ответ на внедрение в организм или активации в нём инфекционного флогогенного агента. При этом очаг воспаления играет двоякую — как защитную, так и патогенную — роль. Защитная роль заключается в ограничении распространения возбудителя инфекции и его токсинов, а патогенная — в выбросе медиаторов воспаления и повреждении тканей в очаге воспаления. Это может усугубить нарушения обмена веществ, функции многих органов, гемодинамики, трофики тканей и т. д. Гипоксия. Нарушения биологического окисления — важный компонент инфП. Тип развивающейся при инфП гипоксии во многом зависит от особенностей инфБ. Так, респираторная гипоксия может возникать в результате угнетающего действия ряда токсинов на дыхательный центр, циркуляторная — следствие нарушения микроциркуляции. Гемический тип гипоксии может развиваться за счёт уменьшения количества эритроцитов (например, при малярии). Тканевая гипоксия формируется вследствие разобщения окисления и фосфорилирования под действием эндотоксинов (например, сальмонелл, шигелл). Нарушения метаболизма. На начальных этапах инфП, как правило, преобладают процессы катаболического характера: протеолиз, липолиз, распад гликогена (и как следствие — гипергликемия). На этапе выздоровления катаболические реакции сменяются стимуляцией анаболических процессов. В зависимости от нозологической формы могут преобладать нарушения определённых видов обмена. Так, при кишечных инфекциях преимущественно наблюдаются расстройства водно-электролитного обмена и КЩР, при гепатитах — белкового, при сепсисе расстраиваются в большей или меньшей мере все виды метаболизма. Расстройства функций. Если защитные механизмы оказываются недостаточными для локализации инфекции, то происходит её генерализация, развиваются выраженные общие реакции различных систем организма хозяина. Принципы терапии инфекционного процесса Терапию инфП проводят с учётом этиотропного, патогенетического и симптоматического принципов лечения. Этиотропное лечение. Этиотропная терапия заключается в воздействии на возбудителя. Для этого применяют: антибактериальные средства; противовирусные; противогрибковые средства; антипротозойные препараты. Патогенетическая терапия. Патогенетическое лечение имеет целью блокаду механизма развития инфП. Это достигается при помощи: дезинтоксикационной терапии; противовоспалительного лечения; иммунотерапии и иммунокоррекции; нормализации функций органов, тканей и их систем; коррекции основных параметров гомеостаза организма. Симптоматическая терапия. Симптоматическое лечение направлено на облегчение состояния пациента и устранение у него тягостных, болезненных ощущений, усугубляющих течение инфП. | |
|
№ 37 Типовые нарушения углеводного обмена. Гипо- и гипергликемические состояния: виды, причины, механизмы возникновения, последствия, принципы терапии. Многочисленные расстройства метаболизма углеводов условно объединяют в несколько групп: гипогликемии, гипергликемии, гликогенозы, гексоз- и пентоземии, агликогенозы. Перечисленные расстройства рассматривают как типовые формы нарушений углеводного обмена.
Гипогликемии — состояния, характеризующиеся снижением уровня глюкозы плазмы крови (ГПК) ниже нормы (менее 65 мг%, или 3, 58 ммоль/л). В норме ГПК натощак колеблется в диапазоне 65—110 мг%, или 3, 58—6, 05 ммоль/л. Причины Гипогликемии. Патология печени . Наследственная и приобретённая патология печени — одна из наиболее частых причин гипогликемии. К гипогликемии приводят нарушения транспорта глюкозы из крови в гепатоциты, снижение активности гликогенеза в них и отсутствие (или малое содержание) депонированного гликогена. Гипогликемия развивается также при длительном голодании, а также может развиться при значительной активации жизнедеятельности организма (например, при физической нагрузке или стрессе). Нарушения пищеварения. Нарушения пищеварения — полостного переваривания углеводов, а также их пристеночного расщепления и абсорбции — приводят к развитию гипогликемии. Гипогликемия развивается также при хронических энтеритах, алкоголь ном панкреатите, опухолях поджелудочной железы, синдромах нарушенного всасывания. Патология почек. Гипогликемия развивается при нарушении реабсорбции глюкозы в проксимальных канальцах нефрона почек. Эндокринопатии. Основные причины развития гипогликемии при эндокринопатиях: недостаток гипергликемизирующих факторов или избыток инсулина. Углеводное голодание. Углеводное голодание наблюдается в результате длительного общего голодания, в том числе углеводного. Дефицит в пище только углеводов не приводит к гипогликемии в связи с активацией глюконеогенеза (образование углеводов из неуглеводных веществ). Длительная значительная гиперфункция организма при физической работе. Гипогликемия развивается при длительной и значительной физической работе в результате истощения запасов гликогена, депонированного в печени и скелетных мышцах. Последствия гипогликемии: гипогликемическая реакция, синдром и кома. Гипогликемическая реакция — острое временное снижение ГПК до нижней границы нормы (как правило, до 80—70 мг%, или 4, 0—3, 6 ммоль/л). Гипогликемический синдром — стойкое снижение ГПК ниже нормы (до 60— 50 мг%, или 3, 3—2, 5 ммоль/л), сочетающееся с расстройством жизнедеятельности организма. Гипогликемическая кома — состояние, характеризующееся падением ГПК ниже нормы (как правило, менее 40—30 мг%, или 2, 0—1, 5 ммоль/л), потерей сознания, значительными расстройствами жизнедеятельности организма. Принципы терапии. Этиотропный принцип направлен на ликвидацию гипогликемии и лечение основного заболевания. Патогенетический принцип терапии ориентирован на блокирование главных патогенетических звеньев гипогликемической комы или гипогликемического синдрома (расстройств энергообеспечения, по вреждения мембран и ферментов, нарушений электрогенеза, дисбаланса ионов, КЩР, жидкости и др. ), а также на ликвидацию расстройств функций органов и тканей, вызванных гипогликемией и её последствиями. Симптоматический принцип лечения направлен на устранение симптомов, усугубляющих состояние пациента (например, сильной головной боли, страха смерти, резких колебаний АД, тахикардии и др. ). Гипергликемии. Гипергликемии — состояния, характеризующиеся увеличением ГПК выше нормы (более 120 мг%, или 6, 05 ммоль/л натощак). Причины гипергликемии: эндокринопатии, неврологические и психогенные расстройства, переедание, патология печени. Эндокринопатии. Эндокринопатии — наиболее частая причина гипергликемии. Основные причины развития гипергликемии при эндокринопатиях: избыток гипергликемизирующих факторов и дефицит инсулина. Неврологические и психогенные расстройства. Нейро- и психогенные расстройства характеризуются активацией симпатико-адреналовой, гипоталамо-гипофизарно-надпочечниковой и тиреоидной систем. Гормоны этих систем вызывают ряд эффектов, приводящих к значительной гипергликемии. Переедание. Переедание— одна из причин гипергликемии. Глюкоза быстро всасывается в кишечнике. ГПК повышается и превышает возможность гепатоцитов включать её в процесс гликогенеза. Кроме того, избыток углеводсодержащей пищи в кишечнике стимулирует гликогенолиз в гепатоци-тах, потенцируя гипергликемию. Патология печени. При печёночной недостаточности может развиваться преходящая гипергликемия в связи с тем, что гепатоциты не способны трансформировать глюкозу в гликоген. Обычно это наблюдается после приёма пищи. Последствия гипергликемии: гипергликемический синдром и гипергликемическая кома. Гипергликемический синдром — состояние, характеризующееся значительным и относительно длительным увеличением ГПК выше нормы (до 190—210 мг%, т. е. 10, 5-11, 5 ммоль/л и более), сочетающееся с расстройством жизнедеятельности организма. | № 38 Сахарный диабет: характеристика понятия; первичные и вторичные формы сахарного, их механизмы. Типы сахарного диабета.
САХАРНЫЙ ДИАБЕТ - заболевание, которое характеризуется нарушением всех видов метаболизма и расстройством жизнедеятельности организма; развивается в результате гипоинсулинизма (т. е. абсолютной или относительной инсулиновой недостаточности).
Первичные формы сахарного диабета. Первичные формы СД характеризуются отсутствием у пациента каких-либо определённых заболеваний, вторично приводящих к развитию диабета. Выделяют две разновидности первичного СД:
• инсулинзависимый сахарный диабет (ИЗСД);
• инсулиннезависимый сахарный диабет (ИНСД).
 Вторичные формы сахарного диабета. Вторичные формы СД характеризуются наличием у пациента какой-либо основной болезни или патологического состояния, повреждающих поджелудочную железу, а также действие на неё физических или химических факторов. Это приводит к возникновению СД. К таким болезням, патологическим состояниям и факторам относятся:
• Заболевания, поражающие ткань поджелудочной железы (например, панкреатит).
• Другие болезни эндокринной системы (например, семейный полиэндокринный аденоматоз).
• Воздействие на поджелудочную железу химических или физических агентов.
Сахарный диабет типов I и II
В более ранних классификациях выделяли СД типов I и II. Эти обозначения вначале применяли как синонимы ИЗСД и ИНСД соответственно. Современные специалисты считают такой подход не совсем корректным. Это объясняется тем, что, например, больные с ИНСД также могут приобрести зависимость от инсулина. При его недостатке у них развивается кетоацидоз, чреватый коматозным состоянием (например, это наблюдается у многих пациентов без ожирения, имеющих в крови AT.
• Термин «Тип I СД» применяли для обозначения тех его вариантов, основным патогенетическим звеном которых являлся иммунный (иммуноагрессивный) механизм.
• Термин «Тип II СД» рекомендовали использовать для той формы СД, патогенез которой не включал в качестве причинного (! ) иммунный механизм.
Вторичные формы сахарного диабета. Вторичные формы СД характеризуются наличием у пациента какой-либо основной болезни или патологического состояния, повреждающих поджелудочную железу, а также действие на неё физических или химических факторов. Это приводит к возникновению СД. К таким болезням, патологическим состояниям и факторам относятся:
• Заболевания, поражающие ткань поджелудочной железы (например, панкреатит).
• Другие болезни эндокринной системы (например, семейный полиэндокринный аденоматоз).
• Воздействие на поджелудочную железу химических или физических агентов.
Сахарный диабет типов I и II
В более ранних классификациях выделяли СД типов I и II. Эти обозначения вначале применяли как синонимы ИЗСД и ИНСД соответственно. Современные специалисты считают такой подход не совсем корректным. Это объясняется тем, что, например, больные с ИНСД также могут приобрести зависимость от инсулина. При его недостатке у них развивается кетоацидоз, чреватый коматозным состоянием (например, это наблюдается у многих пациентов без ожирения, имеющих в крови AT.
• Термин «Тип I СД» применяли для обозначения тех его вариантов, основным патогенетическим звеном которых являлся иммунный (иммуноагрессивный) механизм.
• Термин «Тип II СД» рекомендовали использовать для той формы СД, патогенез которой не включал в качестве причинного (! ) иммунный механизм.
|
№ 39 Этиология, варианты патогенеза и проявления сахарного диабета. Этиология. СД развивается вследствие либо дефицита инсулина (ИЗСД), либо недостаточности его эффектов (ИНСД). Дефицит инсулина может возникнуть под влиянием факторов биологической, химической, физической природы, а также при воспалительных процессах поджелудочной железы Биологические факторы. Генетические дефектыβ -клеток островков Лангерханса. Иммунные факторы: Ig, цитотоксические Т-лимфоциты, а также продуцируемые ими цитокины, повреждающие β -клетки и реализующие реакции иммунной аутоагрессии. Вирусы, тропные к β -клеткам: Коксаки В4, гепатита, кори, ветряной оспы, эпидемического паротита, краснухи и др. Эндогенные токсичные вещества, повреждающие β -клетки, наиболее «агрессивный» из них — аллокеан. Воспалительные процессы, возникающие в поджелудочной железе под действием факторов биологической (главным образом, микроорганизмов), химической и физической природы. Хронические панкреатиты примерно в 30% случаев являются причиной инсулиновой недостаточности. Недостаточность эффектов инсулина развивается под влиянием причин нейро- или психогенной природы, контринсулярных факторов, а также вследствие дефектов инсулиновых рецепторов и пострецепторных нарушений в клетках-мишенях. Патогенез. Дефицит инсулина
При дефиците инсулина происходит: повреждение и гибель р-клеток островков Лангерханса, уменьшение суммарной массы β -клеток, подавление синтеза и выделения в кровь инсулина из повреждённых β -клеток. Недостаточность эффектов инсулина Реализация различных вариантов патогенеза СД при недостаточности эффектов инсулина происходит при нормальном или даже повышенном его синтезе и инкреции в кровь (при этом развивается ИНСД). Выделают контринсулярные факторы, устранение или снижение эффектов инсулина на ткани-мишени, а также инсулинорезистентность. Устранение или снижение эффектов инсулина на ткани-мишени достигается благодаря гипергликемизирующему эффекту избытка гормонов — метаболических антагонистов инсулина. К ним относятся катехоламины, глю-кагон, глюкокортикоиды, СТГ и йодсодержащие тиреоидные гормоны. Длительная и значительная гипергликемия стимулирует повышенное образование инсулина (3-клетками. Однако этого может быть недостаточно для нормализации ГПК, так как продолжительная гиперактивация островков поджелудочной железы ведёт к повреждению р-клеток. Инсулинорезистентность. Нарушение реализации эффектов инсулина на уровне клеток-мишеней известно как инсулинорезистентность. Известны рецепторные и пострецепторные механизмы этого феномена. ПРОЯВЛЕНИЯ САХАРНОГО ДИАБЕТА СД проявляется двумя группами взаимосвязанных расстройств: нарушениями обмена веществ и патологией тканей, органов, их систем. Это приводит к расстройству жизнедеятельности организма в целом. У пациентов с СД выявляются признаки нарушений всех видов метаболизма, а не только углеводного, как следует из его названия. Нарушения обмена веществ
Патология тканей, органов и их систем При СД поражаются все ткани и органы, хотя и в разной степени. В наибольшей мере повреждаются сердце, сосуды, нервная система, почки, ткани глаза, система ИБН. Это проявляется кардиопатиями, ангиопатиями, нейро- и энце-фалопатиями, нефропатиями, снижением остроты зрения и слепотой, комами и другими расстройствами. Их обозначают как осложнения СД. | |
|
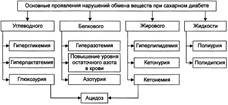
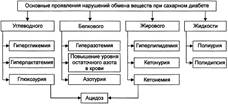
№ 40 Метаболические и функциональные расстройства при сахарном диабете. Осложнения сахарного диабета (острые и хронические). СД проявляется двумя группами взаимосвязанных расстройств: нарушениями обмена веществ и патологией тканей, органов, их систем. Это приводит к расстройству жизнедеятельности организма в целом. У пациентов с СД выявляются признаки нарушений всех видов метаболизма, а не только углеводного, как следует из его названия. Нарушения обмена веществ
Патология тканей, органов и их систем При СД поражаются все ткани и органы, хотя и в разной степени. В наибольшей мере повреждаются сердце, сосуды, нервная система, почки, ткани глаза, система ИБН. Это проявляется кардиопатиями, ангиопатиями, нейро- и энце-фалопатиями, нефропатиями, снижением остроты зрения и слепотой, комами и другими расстройствами. Их обозначают как осложнения СД. ОСЛОЖНЕНИЯ САХАРНОГО ДИАБЕТА Осложнения СД — патологические процессы и состояния, не обязательные для него, но обусловленные либо причинами диабета, либо расстройствами, развившимися при СД. Осложнения СД подразделяют на острые и хронические. Остро протекающие («острые осложнения диабета»): диабетический кето-ацидоз, чреватый развитием ацидотической комы; гиперосмолярная (неке-тоацидотическая) и гипогликемическая кома. Длительно (хронически) протекающие («поздние осложнения диабета»): ангиопатии, невропатии, энцефалопатии, нефропатии, снижение активности факторов ИБН, другие осложнения (остео- и артропатии, катаракта). Остро протекающие осложнения. Эти осложнения обычно возникают под влиянием каких-либо провоцирующих факторов. Наиболее частые причины — неправильная инсулинотерапия (нарушения расчёта необходимого количества вводимого инсулина), стресс-реакции, развитие других заболеваний. Диабетический кетоацидоз. Диабетический кетоацидоз характерен для ИЗСД. Кетоацидоз и кетоацидотическая кома относятся к числу основных причин смерти пациентов с диабетом. Гиперосмолярная кома. Гиперосмолярная некетоацидотическая (гипергликемическая) кома наиболее характерна для пожилых пациентов с ИНСД. Гиперосмолярная кома развивается существенно медленнее, чем кетоацидотическая. Однако летальность при ней выше. Поздние осложнения. Признаки поздних осложнений СД наиболее часто появляются через 15—20 лет после выявления гипергликемии. Вместе с тем у некоторых пациентов они могут или возникнуть раньше, или вообще не проявиться. В основе поздних осложнений СД лежат главным образом метаболические расстройства в тканях. Ангиопатии. Различают микроангиопатии и макроангиопатии. Микроангиопатии— патологические изменения в сосудах микроциркуля-торного русла. Макроангиопатиихарактеризуются ранним и интенсивным развитием склеротических изменений в стенках артерий среднего и крупного калибра у пациентов с СД, являющимся одним из основных факторов риска развития (ускоренного! ) атеросклероза. Невропатии. Симптомы диабетических невропатий могут наблюдаться уже на ранних стадиях заболевания в любом отделе нервной системы. Они являются одной из наиболее частых причин инвалидизации пациентов. Наиболее выражены невропатии у пожилых пациентов с хроническим течением диабета и значительной гипергликемией. Ретинопатии. Поражение сетчатки глаза при диабете является основной причиной снижения остроты зрения и слепоты. Нефропатии. Нарушение функции почек — одна из частых причин инвалидизации и смерти при СД. Последняя является исходом почечной недостаточности. Диабетическая нефропатия занимает второе место среди причин смерти больных диабетом. Иммунологические поражения. Для СД характерно снижение эффективности системы ИБН. Об этом свидетельствуют данные о более частом развитии и тяжёлом течении у пациентов с СД: Прочие осложнения. У пациентов с СД наблюдаются и многие другие осложнения (кардиопатии, катаракта, триглицеридемия, нарушения ионного обмена, остео- и артропа-тии). Это обусловлено тем, что патологические изменения при СД развиваются во всех тканях и органах. | № 41 Диабетическая кома, её разновидности, общие звенья патогенеза и проявления. Принципы терапии сахарного диабета. Диабетический кетоацидоз. Диабетический кетоацидоз характерен для ИЗСД. Кетоацидоз и кетоацидоти-ческая кома относятся к числу основных причин смерти пациентов с диабетом. Причины: Недостаточное содержание в крови инсулина и/или его эффектов и Повышение концентрации и/или выраженности эффектов контринсу-лярных гормонов (глюкагона, катехоламинов, СТГ, кортизола, тирео-идных). Механизм развитиявключает несколько звеньев: существенная активация глюконеогенеза, протекающая на фоне стимуляции гликогенолиза, протеолиза и липолиза; нарушение транспорта глюкозы в клетки, ведущее к нарастанию гипергликемии; стимуляция кетогенеза с развитием ацидоза. Гиперосмолярная кома. Гиперосмолярная некетоацидотическая (гипергликемическая) кома наиболее характерна для пожилых пациентов с ИНСД. Гиперосмолярная кома развивается существенно медленнее, чем кетоацидотическая. Однако летальность при ней выше. Гипогликемическая кома. Причины: Передозировка инсулина; Задержка очередного приёма пищи или голодание (вынужденное либо осознанное, в последнем случае наблюдается при попытке самоубийства); Избыточная и/или длительная физическая нагрузка.; Дефицит контринсулярных гормонов и/или их эффектов. Это одна из частых причин гипогликемической комы, поскольку синтез глюкагона и катехоламинов у этих пациентов обычно снижен; Все указанные причины (особенно если они действуют в сочетании) приводят к значительной гипогликемии. Механизмы развития Причинный фактор патогенеза — гипогликемия. Она обусловливает: § Снижение потребления кислорода нейронами мозга. В связи с этим субстратное «голодание» нервных клеток усугубляется кислородным. § Острое нарушение ресинтеза АТФ в нейронах ЦНС. § Активацию симпатико-адреналовой системы. Катехоламины в данной ситуации тормозят развитие тяжёлой гипогликемии, стимулируя гликогенолиз и вызывая тахикардию, аритмии, дрожь, мышечную слабость, неприятные ощущения в области сердца, потливость, заставляющие пациента немедленно принять глюкозу. Недостаточность энергоснабжения нейронов головного мозга вызывает расстройства ВНД и психические изменения: нарастающую сонливость, спутанность сознания и его утрату, головную боль, нарушение речи, судороги. Нарушение функции сердца (развитие аритмий, сердечной недостаточности). Расстройства дыхания, гиповентиляция лёгких, нередко — прекращение дыхания. Недостаточность кровообращения проявляется нарушением центральной, органно-тканевой и микрогемоциркуляции. У пациентов развивается острая гипотензия (коллапс). ПРИНЦИПЫ ТЕРАПИИ САХАРНОГО ДИАБЕТА Этиотропный принцип направлен на устранение причины СД и условий, способствующих развитию заболевания. Данный подход наиболее рационален на начальном этапе болезни. Патогенетический принцип имеет целью разрыв патогенетических звеньев СД. В рамках этого принципа решаются следующие задачи: § Контроль и коррекция уровня ГПК. Нормализация содержания глюкозы в течение длительного времени, как правило, снижает выраженность или устраняет основные метаболические, функциональные и ряд структурных отклонений в организме. § Коррекция водного и ионного обмена, сдвигов кислотно-основного состояния. § Предотвращение острых осложнений диабета § Предотвращение или уменьшение степени хронических осложнений. Симптоматический принцип направлен на устранение и предотвращение состояний и симптомов, усугубляющих течение СД и самочувствие пациента: фурункулёза, гипер- или гипотензивных реакций, снижения остроты зрения, тяжёлой головной боли, изменений кожи и слизистых оболочек, невропатических болей, расстройств пищеварения. |
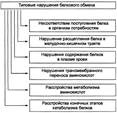
№ 42 Типовые нарушения обмена белков и нуклеиновых кислот: этиология, основные звенья, патогенез, проявления. Подагра: причины, механизмы развития, проявления. Нарушения обмена белков
НЕСООТВЕТСТВИЕ КОЛИЧЕСТВА И АМИНОКИСЛОТНОГО СОСТАВА БЕЛКА, ПОСТУПАЮЩЕГО В ОРГАНИЗМ, ПОТРЕБНОСТЯМ В БЕЛКЕ
РАССТРОЙСТВА ПИЩЕВАРЕНИЯ В ЖЕЛУДКЕ И КИШЕЧНИКЕ К расстройствам пищеварения, приводящим к нарушению обмена белка, относят нарушения расщепления белка в желудке и переваривания его в тонкой кишке. Нарушения расщепления белка в желудке Причины : Гипоацидные состояния; Снижение содержания и/или активности пепсина; Резекция части желудка. Последствия и проявления: Нарушения набухания белка; Торможение переваривания коллагенового компонента продуктов; Недостаточное расщепление белков мышечных волокон; Замедление эвакуации пищи в двенадцатиперстную кишку. Нарушения переваривания белка в тонкой кишке Причины: факторы (в том числе наследственные), вызывающие расстройства пищеварения в кишечнике, включая синдромы мальабсорбции (синдромы нарушенного всасывания). Проявления: Креаторея; Целиакия глютеновая — синдром, характеризующийся нарушением полостного и мембранного переваривания белков, а также торможением всасывания аминокислот; Недостаточность энтерокиназы приводит к существенному снижению протеолитической активности кишечного сока. НАРУШЕНИЯ ТРАНСМЕМБРАННОГО ПЕРЕНОСА АМИНОКИСЛОТ Их причины: мембранопатии различного генеза (первичные — моногенные дефекты и вторичные). Мембранопатии приводят к нарушениям транспорта аминокислот на нескольких этапах: из кишечника в кровь, из крови в гепатоциты, из первичной мочи в кровь, из крови в клетки органов и тканей. РАССТРОЙСТВА МЕТАБОЛИЗМА АМИНОКИСЛОТ Нарушения обмена аминокислот, как правило, существенно изменяют метаболизм белков и приводят к расстройствам обмена нуклеиновых кислот, липи-дов, витаминов, углеводов, электролитов и воды. Различают первичные (наследственные, врождённые) и вторичные (приобретённые, симптоматические) расстройства метаболизма аминокислот. НАРУШЕНИЕ СОДЕРЖАНИЯ БЕЛКОВ В ПЛАЗМЕ КРОВИ Уровень протеинемии является результатом соотношения процессов протео-синтеза и протеолиза в различных тканях и органах.
РАССТРОЙСТВА ФИНАЛЬНЫХ ПРОЦЕССОВ КАТАБОЛИЗМА БЕЛКА Расстройства конечных стадий катаболизма белка характеризуются нарушением образования и дальнейших изменений мочевины, мочевой кислоты, аммиака, креатинина, индикана, а также их выведения из организма. Нарушения обмена нуклеиновых кислот Нарушения обмена нуклеиновых кислот характеризуются расстройствами синтеза и деструкции пиримидиновых и пуриновых оснований. РАССТРОЙСТВА МЕТАБОЛИЗМА ПИРИМИДИНОВЫХ ОСНОВАНИЙ К расстройствам, сопровождающимся нарушением метаболизма пиримиди-новых оснований, относятся оротацидурия, гемолитическая анемия и ами-ноизобутиратурия вследствие недостаточности 3-гидроксиизобутират дегидрогеназы. НАРУШЕНИЯ ОБМЕНА ПУРИНОВЫХ ОСНОВАНИЙ К основным проявлениям, вызванным нарушениями обмена пуриновых оснований, относят подагру, гиперурикемию, синдром Леша—Найена и гипоурикемию. ПОДАГРА - типовая форма патологии пуринового обмена, характеризующаяся хроническим повышением содержания в крови мочевой кислоты, отложением избытка её солей в органах, тканях, суставах, уратной нефропатией, нефро- и уролитиазом. Причины.
Патогенез.
| |
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|
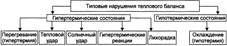

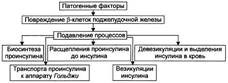


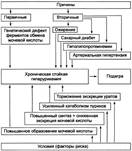 Проявления подагры: Постоянно повышенная концентрация мочевой кислоты в плазме крови и моче; Воспаление различных суставов (чаще моноартриты); Лихорадка; Сильная боль в зоне накопления уратов (может иметь характер длительных эпизодов: до 2—3 сут); Повторное появление тофусов; Признаки почечной недостаточности; Нефро- и уролитиаз, рецидивирующие пиелонефриты; Изменения в почках завершаются нефросклерозом, почечной недостаточностью, уремией.
Проявления подагры: Постоянно повышенная концентрация мочевой кислоты в плазме крови и моче; Воспаление различных суставов (чаще моноартриты); Лихорадка; Сильная боль в зоне накопления уратов (может иметь характер длительных эпизодов: до 2—3 сут); Повторное появление тофусов; Признаки почечной недостаточности; Нефро- и уролитиаз, рецидивирующие пиелонефриты; Изменения в почках завершаются нефросклерозом, почечной недостаточностью, уремией.