- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
МЕТОДЫ КЛИНИЧЕСКОГО ИССЛЕДОВАНИЯ 10 страница
| № 79 Основные этапы и механизмы трансформации нормальной клетки в опухолевую. Понятие об онкогенах и онкосупрессорах (“антионкогенах”). Несмотря на большое число канцерогенных агентов и разнообразие клинических форм опухолевого роста на уровне клетки происходит общее закономерное изменение — трансформация нормальной генетической программы в программу формирования опухолевого атипизма. В основе опухолевой трансформации лежат стойкие изменения ДНК. При этом программа опухолевого роста становится фрагментом общей реализуемой клеткой программы, закодированной в её геноме. Единый конечный результат действия канцерогенов различной природы (химической, биологической, физической) на клетки и как результат — их опухолевая трансформация, обеспечивается нарушением взаимодействия в клеточном геноме онкогенов и антионкогенов. Стимуляция канцерогенными агентами экспрессии онкогенов и/или депрессия антионкогенов и обеспечивает опухолевую трансформацию клеток. Онкогены. Вирусные онкогены и контролирующие клеточный цикл и пролиферацию клеточные гены имеют как сходство, так и важные отличия. В связи с этим говорят о протоонкогенах и онкогенах. Протоонкоген — ген нормального генома человека; участвует в регуляции пролиферации клеток. Продукты экспрессии протоонкогенов во многих случаях важны для нормальной дифференцировки клеток и межклеточных взаимодействий. В результате соматических мутаций протоонкоген может стать онкогенным. Онкоген • Онкоген — один из генов, в обычных условиях (т. е. в качестве протоонкогена) кодирующий белок, обеспечивающий пролиферацию и диф-ференцировку клеточных популяций. У опухолевых ДНК-вирусов онкогены кодируют нормальные вирусные белки; онкогены, однако, могут спровоцировать — в случае их мутаций или активации ретровирусами — злокачественный рост. • Онкогены найдены в некоторых ДНКовых опухолевых вирусах. Они необходимы для репликации вируса (трансформирующий ген). • К онкогенам относятся также гены вируса или ретровируса, вызывающие злокачественное перерождение клетки-хозяина, но необязательные для репликации вируса. Онкосупрессоры. Трансформированные (опухолевые) клетки делятся бесконтрольно и неограниченно долго. Онкосупрессоры, или антионкогены тормозят их пролиферацию. ЭТАПЫ КАНЦЕРОГЕНЕЗА Вне зависимости от конкретной причины опухолевой трансформации клетки, гистологической структуры и локализации новообразования, в процессе онко-генеза можно условно выделить несколько общих этапов. • На первом этапе происходит взаимодействие канцерогенов химической, физической и биологической природы с протоонкогенами и антионкогенами (онкосупрессорами) генома нормальной клетки. • В результате такого взаимодействия на втором этапе канцерогенеза подавляется активность онкосупрессоров, а также происходит трансформация протоонкогенов в онкогены. Экспрессия онкогена — необходимое и достаточное условие для трансформации нормальной клетки в опухолевую. • В результате подавления активности онкосупрессоров и экспрессии онкогенов на третьем этапе синтезируются и реализуют свои эффекты (непосредственно или с участием клеточных факторов роста и рецепторов к ним) он-кобелки. С этого момента генотипически изменённая клетка приобретает опухолевый фенотип. • На четвёртом этапе опухолевая клетка начинает бесконтрольно проли-ферировать, что ведёт к формированию новообразования (опухолевого узла). |
№ 80 Характеристика опухолевого атипизма роста, обмена веществ, функции, структуры: механизмы, проявления, последствия. Общая характерная черта трансформированных клеток — опухолевый атипизм. Опухолевый атипизм проявляется большим числом признаков, характеризующих рост, структуру, метаболизм и функции клеток. Атипизм роста. Атипизм клеточного роста характеризуется своеобразием пролиферации опухолевых клеток, расстройствами их дифференцировки, инвазивным ростом, метастазированием и рецидивированием.
Атипизм пролиферации . В опухоли значительно увеличено количество делящихся клеток. В опухолях число пролиферирующих клеток превышает в очень большое количество раз. Увеличение числа делящихся клеток ведёт к быстрому нарастанию массы солидной опухоли или суммарного количества клеток (например, лейкозных) при гемобластозах. Атипизм дифференцировки. Заключается в частичном или полном подавлении процесса созревания (дифференцировки) опухолевых клеток. Инвазивный рост. Характеризуется проникновением клеток опухоли в окружающие нормальные ткани. Сочетается с их деструкцией. Метаболический атипизм. Атипизм обмена веществ (метаболический, биохимический) заключается в существенном изменении всех видов обмена: нуклеиновых кислот, белков, углеводов, липидов, ионов, жидкости, витаминов. В связи с этим закономерно изменяются и физико-химические параметры опухолевых клеток и новообразования в целом. Атипизм обмена нуклеиновых кислот. Вопухоли увеличен синтез ДНК и РНК. Атипизм белкового обмена. Проявления: - Усиление включения аминокислот в реакции протеосинтеза - Интенсификация синтеза различных классов белков (структурных, ферментов, онкобелков и других) при одновременном уменьшении или прекращении синтеза ряда иных белков. - Изменение антигенного профиля опухолей. Это обусловлено модификациями макромолекул белка. Нарушения метаболизма белка в новообразованиях, с одной стороны, обеспечивают реализацию большинства других проявлений их атипизма, лежащих в основе прогрессирующего опухолевого роста, а с другой — способствуют активации механизмов антибластомной защиты организма, обусловленной появлением у клеток опухоли Аг, не свойственных нормальным аутологичным клеткам. Атипизм обмена углеводов. Метаболизм углеводов в опухолях характеризуется рядом особенностей. Проявления: - Активация реакций транспорта и утилизации клетками бластомы глюкозы. - Уменьшение относительной доли тканевого дыхания при ресинтезе АТФ. - Интенсификация процесса прямого окисления углеводов в пентозофос-фатном цикле. Атипизм обмена липидов. Проявления: - Значительное усиление утилизации ВЖК и холестерина. - Активация синтеза липидных структур клеток. - Интенсификация процессов липопероксидации. Изменение липидного метаболизма в новообразованиях направлено на энергетическое и пластическое обеспечение усиленных анаболических процессов, реакций синтеза структур интенсивно делящихся бластомных клеток. Подобные отклонения в опухолях нередко сочетаются с торможением развития ате-росклеротических изменений в стенках сосудов у онкологических больных. Атипизм обмена ионов и воды. В новообразованиях наблюдается избыточное (в сравнении с нормальными аутологическими тканями) накопление ряда ионов и воды, а также изменение соотношения отдельных ионов как в цитозоле бластомных клеток, так и межклеточной жидкости. Отклонения характера обмена ионов и воды в новообразованиях способствует реализации других видов атипизма: роста, функции и структуры. Это, в свою очередь, повышает приспособляемость опухоли. Атипизм обмена витаминов. Особенности обмена витаминов в опухолевой ткани изучены недостаточно. Проявления: - Многие витамины интенсивно захватываются клетками бластомы. Полагают, что витамины в опухоли используются в качестве предшественников различных коферментов (как и в нормальных клетках), а также — субстратов обмена веществ и пластических процессов, обеспечивающих интенсивный рост и деление бластомных клеток. - Различные опухоли являются «ловушкой» жирорастворимого витамина Е. Он обладает антиоксидантной активностью в связи с его способностью нейтрализовать свободнорадикальные агенты и способствовать стабилизации клеточных мембран. По-видимому, это является одним из механизмов повышения устойчивости опухолевых клеток к цитотоксическим воздействиям. Атипизм функций. Обычно функции клеток новообразования снижены и/или качественно изменены, реже — повышены. Гипофункция. Как правило, отдельные опухолевые клетки и новообразование в целом характеризуются пониженным функционированием. Гиперфункция. Нередко наблюдаются признаки гиперфункции как отдельных раковых клеток, так и опухоли в целом. Обычно речь идет о неадекватной потребностям организма продукции каких-либо веществ. Дисфункция. В некоторых опухолях выявляются признаки, не свойственные для нормальных аутологичных тканей. Таким образом, атипизм функции опухолей обусловливает нарушение деятельности тканей и органов, которые они поражают, а также — расстройство жизнедеятельности организма-опухоленосителя. С учётом этого в онкологии сложилось представление об опухолевой болезни. Метастазирование — одно из фатальных проявлений атипизма опухолевого роста — перенос клеток бластомы на расстояние от основного (материнского) узла и развития опухоли того же гистологического строения в другой ткани или органе. Рецидивирование — повторное развитие новообразования того же гистологического строения на прежнем месте после его удаления или деструкции. |
№ 81 Понятие об опухолевой прогрессии. Характеристика механизмов противоопухолевой защиты организма. Принципы профилактики и лечения опухолей. Опухолевая прогрессия — генетически закреплённое, наследуемое опухолевой клеткой и необратимое изменение одного или нескольких свойств клетки. ПРОТИВООПУХОЛЕВАЯ ЗАЩИТА ОРГАНИЗМА Различают антиканцерогенные, антимутационные и антицеллюлярные механизмы противоопухолевой защиты. Антиканцерогенные механизмы Антиканцерогенные механизмы обеспечивают торможение и/или блокаду проникновения канцерогенов в клетку, её ядро, действие их на геном и инактивацию и элиминацию бластомогенных агентов из клетки и организма. Механизмы, препятствующие действию химических канцерогенных факторов - Физико-химическая фиксация и удаление из организма - Поглощение канцерогенов в процессе фагоцитоза, сочетающееся с их инактивацией и разрушением. - Инактивация бластомогенных агентов как гаптенов при помощи AT и Т-лимфоцитов с последующей их деструкцией и элиминацей из организма. - Конкурентная блокада неканцерогенными метаболитами клеточных рецепторов, с которыми способны взаимодействовать истинные бластомогенные вещества. - Разрушение и/или инактивация канцерогенов в клетках и биологических жидкостях в процессе их окисления, восстановления, деметилирования, глюкуронизации, сульфатирования. - Ингибирование («гашение») свободных радикалов и гидроперекисей органических и неорганических соединений ферментативными и неферментными факторами антиоксидантной защиты. Механизмы, препятствующие действию онкогенных вирусов - Инактивация вирусов Ig, образуемыми плазматическими клетками под влиянием антигенных вирусных белков. - Ингибирование ИФН — белками, тормозящими или блокирующими процесс внутриклеточной репликации вирусов. - Обнаружение и разрушение вируссодержащих клеток организма неспецифическими цитолитическими клетками. Механизмы, препятствующие действию канцерогенов физической природы - Улавливание и/или инактивация свободных радикалов кислорода, липидов, других органических и неорганических веществ. - Разрушение перекисей и гидроперекисей различных веществ. Антимутационные механизмы Антимутационные механизмы обеспечивают обнаружение, устранение или подавление активности онкогенов. Реализуются антимутационные механизмы при участии онкосупрессоров и систем репарации ДНК. При недостаточности антимутационных механизмов и активации онкогенов нормальная клетка приобретает опухолевый генотип и характерные для него фенотипические признаки. Это служит сигналом для включения антицеллю-лярных механизмов противоопухолевой защиты. Антицеллюлярные механизмы Антицеллюлярные механизмы обеспечивают обнаружение и разрушение гено-типически и фенотипически чужеродных для организма опухолевых клеток или торможения их роста. Сигналом для активации антицеллюлярных механизмов противоопухолевой защиты организма является генетическая чужеродность клеток бластомы. Различают неиммунные (неспецифические) и иммунные (специфические) антицеллюлярные механизмы. Неиммунные механизмы . Эти механизмы осуществляют надзор за сохранением нормального (индивидуального и однородного) клеточного состава организма. Реализуют эти механизмы как клетки, так и гуморальные факторы. Иммунные механизмы. Эти механизмы реализуют клеточное и гуморальное звенья иммунитета. ПРОФИЛАКТИКА ОПУХОЛЕЙ Цель профилактики новообразований: предупредить действие на клеточный геном клеток канцерогенов, значительно снизить их бластомогенное действие и предотвратить тем самым возникновение опухолевой клетки. Мероприятия • Снижение содержания или устранение в окружающей человека среде канцерогенных агентов. • Индивидуальную защиту организма, особенно на производстве • Повышение общей и противоопухолевой устойчивости организма. • Своевременное (максимально раннее) обнаружение и ликвидацию так называемых предопухолевых состояний. ПРИНЦИПЫ ЛЕЧЕНИЯ ОПУХОЛЕЙ Общие подходы Лечение опухолей может быть радикальным и паллиативным. Радикальное лечение направлено на ликвидацию опухоли и предполагает возможность полного выздоровления либо длительной ремиссии. Паллиативное лечение применяют при невозможности проведения радикальной терапии. Лечение приводит к удлинению жизни и уменьшению страданий. Риск рецидива достаточно велик, хотя первоначально больной может чувствовать себя полностью здоровым. Большинство онкологических больных лечат хирургически и с применением лучевой терапии, химиотерапии и иммунотерапии. Выбор метода лечения зависит от характера заболевания, стадии, гистологического типа опухоли, возраста больного, наличия сопутствующих заболеваний и цели лечения (излечение или паллиативное вмешательство). Хирургическое вмешательство и лучевая терапия воздействует на первичную опухоль и регионарные лимфатические узлы. Ни тот, ни другой метод не влияет на области отдалённого распространения. Химиотерапия и иммунотерапия — системные методы лечения, способны воздействовать на области отдалённого распространения. Дополнительное лечение — системная терапия, применяемая после местного лечения (например, резекции) при высоком риске наличия микроскопического очага в лимфатических узлах или отдалённых органах. У значительной части таких больных развивается рецидив, цель дополнительного лечения — уничтожение этих удалённых и микроскопических очагов опухоли. Комплексное лечение использует преимущества каждого метода лечения для компенсации недостатков других. |
|
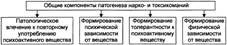
№ 82 Наркомании и токсикомании: характеристика понятий, причины и факторы риска; общие звенья патогенеза и стадии развития. Наркомания/токсикомания — типовая форма психосоматических расстройств. Проявляется стойким патологическим влечением к повторному приёму соответствующего психоактивного вещества, как правило, в возрастающих дозах. Характеризуется психической, а также физической зависимостью, проявляющейся развитием абстинентного синдрома при прекращении его приёма. Сопровождается патологическими изменениями личности, развитием комплекса психических, невротических, вегетативных и соматических расстройств. Наркомании — формы патологии, вызываемые средствами, включёнными в официальный список наркотиков. Токсикомании — формы патологии, формирующиеся при злоупотреблении не относящимися к наркотикам веществами (в том числе ЛС и алкоголем). Причины • Средства, вызывающие наркоманию. Примеры: - Опиаты (героин, морфин, препараты опийного мака, например омнопон). - Стимуляторы ЦНС (кокаин, марихуана и другие препараты индийской конопли). - Галлюциногены (диэтиламид лизергиноюй кислоты — ЛСД, мескалин и др. ) • Токсикоманические средства, применяемые с немедицинской целью: для улучшения самочувствия, настроения, умственной деятельности, устранения ощущения дискомфорта. Примеры: - Некоторые химические реактивы (например, летучие органические растворители). - Бытовые химические вещества (например, инсектициды, клеи, репелленты). - Этанол. - ЛС, не относящиеся к наркотикам (например, транквилизаторы). Факторы риска К факторам риска относятся такие, которые способствуют повторному применению указанных веществ. - Социальные факторы (например, низкий материальный уровень, информационные перегрузки, нестабильные периоды развития общества и личности, стрессы, национальные обычаи, окружающая социальная среда и др. ). - Психологические факторы (низкая социальная адаптированность, слабый тип ВНД). - Биологические факторы (наследственная предрасположенность к применению психоактивных веществ). Патогенез.
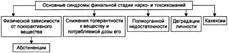
Патологическое влечение к повторному употреблению психоактивного вещества • Приём наркотика или токсикоманического вещества вызывает индивидуальные, более или менее выраженные положительные эмоции. Это побуждает к повторному использованию данного вещества (феномен «подкрепления»). • Каждый эпизод искусственно вызванного состояния комфорта способствует формированию патологической системы. Функция этой системы имеет целью приём очередной — подкрепляющей порции вещества для достижения психологического и физического комфорта. Наркотики и другие психоактивные вещества активируют систему подкрепления. Это сопровождается массированным выбросом дополнительных количеств нейромедиаторов из мест их депонирования. Они обеспечивают развитие очередного эпизода чувства комфорта, эйфории, хорошего настроения и даже повышение работоспособности. Так формируется устойчивое патологическое влечение к повторному приёму психоактивного средства. Развитие толерантности к психоактивному веществу Патогенетическая основа феномена — модифицирующее влияние психоактивных веществ на клеточные мембраны, рецепторные структуры клеток, ферменты. • Повторный приём наркотиков, токсичных веществ, алкоголя увеличивает вязкость мембран клеток, в том числе нейронов. Возрастает их ригидность (в определённой мере это связано с накоплением в мембранах избытка холестерина и/или пальмитиновой кислоты, других ВЖК). • Повышение плотности биомембран увеличивает их устойчивость к действию психоактивных веществ. Формируется состояние толерантности к данному и подобным веществам. • Возрастание плотности мембран препятствует подвижности в них рецепторов, что делает их менее доступными для нейромедиаторов системы подкрепления чувства комфорта. Это. потенцирует состояние толерантности к психоактивному веществу. Формирование психической и физической зависимости • Психическая зависимость — состояние, характеризующееся развитием дискомфорта при прекращении поступления в организм психоактивного вещества, обеспечивающего чувство удовлетворения, психического и физического подъёма и требующее периодического или постоянного употребления этого вещества или его аналога. • Физическая зависимость — состояние, характеризующееся выраженными острыми нарушениями физического состояния, глубокими расстройствами деятельности ЦНС, органов, тканей и их систем при прекращении поступления в организм психоактивного вещества, требующее периодического или постоянного введения его в организм. • Синдром абстиненции — состояние, развивающееся при прекращении введения в организм психоактивного вещества на фоне физической зависимости от него. Характеризуется комплексом признаков психических, вегетативных и физических расстройств. При воздержании от употребления наркотика состояние постепенно облегчается, хотя некоторые признаки сохраняются ещё в течение нескольких месяцев. Вместе с тем у 5—8% страдающих алкоголизмом абстинентный синдром сопровождается нарушением сознания, галлюцинациями, судорогами, нарушениями функций сердца, дыхания и смертью Стадии. Начальная стадия (психического влечения к психоактивному веществу, адаптивная, психической зависимости, психастеническая, неврастеническая) характеризуется развитием комплекса синдромов.
Стадия физической зависимости (наркоманическая, токсикоманическая, субкомпенсации, средняя) характеризуется формированием своеобразного комплекса патогенных синдромов.
Финальная стадия (энцефалопатическая, соматическая, декомпенсации, истощения) — комплекс патогенных синдромов
|
№ 83 Алкоголизм: факторы риска, патогенез, стадии, общие признаки и синдромы, принципы лечения. Алкоголизм — выраженное нарушение социальной, психологической и физиологической адаптации вследствие регулярного употребления алкоголя. Заболевание постепенно ведёт к физической, интеллектуальной, эмоциональной деградации и распаду личности. Характеризуется психологической и физической зависимостью от алкоголя, развитием абстинентного синдрома, социальных проблем. Чаще формируется в 20—29 лет. Факторы риска • Употребление алкоголя • Влияние других психотропных веществ, в том числе никотина • Алкоголизм в семейном анамнезе • Принадлежность к мужскому полу в сочетании с молодым возрастом, отсутствием семьи • Систематическое употребление алкоголя в количестве 5 алкогольных доз и более, пребывание в состоянии опьянения по крайней мере 1 раз в неделю • Семейный или социокультурный фон, благоприятствующий злоупотреблению алкоголем; восприятие злоупотребления алкоголем как нормального явления • Повышенная чувствительность к алкоголю • Неблагополучие общества. Метаболизм этанола • После приёма этанол быстро всасывается из желудка и тонкой кишки в кровь и циркулирует в ней, легко проникая в клетки. 5—10% этанола выделяются с мочой, калом, потом, молоком, выдыхаемым воздухом. 90% окисляются в итоге до воды и С02 • Окисление этанола происходит преимущественно в печени сначала до аце-тальдегида. Окисление ацетальдегида до воды и С02 катализируют ацетальдегиддегидрогеназы. Ацетальдегид циркулирует во внутренней среде, легко проникает через клеточные мембраны и крайне токсичен. Токсичность алкоголя определяется токсичностью прежде всего ацетальдегида, а затем — этанола. • Изменение функций ЦНС определяется содержанием этанола в крови Общие признаки • Больные выглядят старше своих лет • Лицо пастозное, розоватого цвета; в последующем — гиперемия. При воздержании гиперемия постепенно исчезает и на фоне бледности проступают телеангиэктазии на крыльях носа, щеках, шее, верхней части груди • Тургор кожи снижен • Тонус мышц восстанавливается при приёме спиртного. Синдромы • Синдром изменённой реактивности — изменение переносимости спиртных напитков, исчезновение защитных реакций при передозировке алкоголя, способность к систематическому употреблению спиртного и извращение его действия, амнезии на период опьянения (палимпсесты). • Синдром психической зависимости — навязчивое влечение к опьянению, психический дискомфорт в трезвом состоянии и улучшение психических функций в состоянии опьянения. • Синдром физической зависимости — физическая (неудержимая) потребность в опьянении, потеря контроля за количеством выпитого спиртного, проявления абстиненции, улучшение физических функций в состоянии опьянения. • Синдром последствий хронической интоксикации • Психические последствия: астения, психопатизация, • Неврологические последствия: острые мозговые синдромы; атрофия зрительного, слухового нервов. • Синдром алкогольного идиосинкразического опьянения возникает редко и характеризуется внезапным появлением выраженных отклонений в поведении после употребления небольшого количества алкоголя • Абстинентный синдром развивается обычно через 12—24 ч после последнего приёма алкоголя • На начальных стадиях — симпатикотоническое перевозбуждение • На последних стадиях — вегетативные расстройства: • Делирий алкогольный — позднее проявление алкогольного синдрома отмены. Проявления: возбуждение, беспокойство, агрессивное поведение, бессонница, тремор, бред, галлюцинации, • Алкогольный галлюциноз — органический галлюциноз с красочными и устойчивыми галлюцинациями (слуховыми или зрительными), чаще неприятного содержания; • Алкогольный амнестический синдром — необратимые нарушения краткосрочной памяти при отсутствии поражения сенсорной сферы; • Алкогольная энцефалопатия • Деменция. • Гиперлипидемия типа V: панкреатит, гиперлипидемия, гиперли-попротеинемия, гипербеталипопротеинемия, повышенное содержание холестерина, выраженная триглицеридемия, нарушения теста переносимости глюкозы. Стадии развития • I стадия (длительность 1—4 года) • Синдром изменённой реактивности: значительное возрастание переносимости спиртного, рвоты при передозировке нет, палимпсесты • Синдром психической зависимости: постоянные мысли о спиртном, чувство дискомфорта в трезвом состоянии • Синдром физической зависимости отсутствует • Синдром последствий интоксикации: астения, преходящие соматоневрологические нарушения. • II стадия (длительность 5-15 лет) • Синдром изменённой реактивности: максимальная переносимость спиртного; ежедневное пьянство. • Синдром психической зависимости: психическое благополучие зависит от постоянства приёма алкоголя; в трезвом состоянии — дезорганизация психической деятельности, неспособность к умственной работе • Синдром физической зависимости: неудержимое влечение к алкоголю. • Абстинентный синдром в форме симпатико-тонического перевозбуждения • III стадия (длительность 5—10 лет) • Синдром изменённой реактивности: снижение переносимости спиртного. Многодневное пьянство (запои) приводит к физическому и психическому истощению с последующим воздержанием в течение некоторого времени, глубокое опьянение достигается малыми дозами. • Синдром психической зависимости: симптомы незаметны на фоне грубых психических изменений • Синдром физической зависимости: неудержимое влечение определяет жизнь больного; • Абстинентный синдром в форме вегетативных расстройств Лечение. Общая тактика • Контролируемое потребление алкоголя сопровождается высоким риском возобновления алкоголизма • Большинство алкоголиков обращаются к врачу в результате воздействия извне. Прогноз лучше дать при добровольном обращении • Необходим благоприятный психологический фон — понимание и отсутствие осуждения со стороны врача и близких • Лечение обычно проводят в наркологических диспансерах, больницах, специализированных отделениях и палатах врачи-наркологи и психиатры (лечение в общемедицинской сети часто неэффективно). Патогенетическая лекарственная терапия • При абстинентном синдроме — большие дозы витаминов С и В, особенно тиамина и инфузионная терапия • С целью детоксикации и купирования абстиненции применяют хлордиазе-поксид (хлозепид), диазепам (сибазон) • Специальные средства для лечения алкоголизма | № 84 Адаптационный синдром и стресс: характеристика понятий, причины, стадии, общие механизмы развития, роль в развитии патологических процессов. Виды стресса, антистрессорные механизмы, принципы коррекции стресс-реакции. Адаптационный процесс – общая реакция организма на действие чрезвычайного фактора внешней или внутренней среды, характеризующийся стадийными специфическими и неспецифическими изменениями жизнедеятельности, обеспечивающая повышение резистентности организма к воздействующему на него фактору и как следствие – приспособляемости его к меняющимся факторам существования. Причины возникновения: 1. Экзогенные факторы Физические (атмосферное давление, температура окр. среды и т. д. ) Химические (Содержание О2, голодание, потребление жидкости, интоксикации) Биологические (инфекции, интоксикации экзогенными БАВ) 2. Эндогенные факторы Недостаточность функций тканей, органов, систем Дефицит или избыток БАВ(гормонов, ферментов) Стадии: 1. Стадия срочной адаптации, заключается в мобилизации предсуществующих компенсаторных и защитных механизмов, характеризуется значительной активацией исследовательской функции, гиперфункции многих систем организма, мобилизацией органов и систем, которые реагируют на воздействие любого чрезвычайного фактора для данного организма Механизмы: - Активация нервной и эндокринной систем и, как следствие, увеличение в крови стрессорных гормонов и нейромедиаторов – адреналина, норадреналина, глюкокортикоидов и т. д. - Увеличение содержания в клетках местных «мобилизаторов» функций (Са, цитокины, пептиды), что ведет к увеличению функций, катализируемых ими - Изменения в мембранном аппарате клеток, интенсификация СПОЛ, липаз, протеаз - усиление распада органических соединений, клеточных структур, мобилизация пластических ресурсов организма - Увеличение функций всех органов 2. Стадия повышенной резистентности – стадия долговременной адаптации - Формируется состояние специфической устойчивости к конкретному агенту и другим факторам - Увеличение мощности и надежности функций органов и физиологических систем, обеспечивающих адаптацию к определенному фактору - Устранение признаков стрессорной реакции, формируется эффективное приспособление организма Всё это достигается путем перераспределения кровотока и активации генетического аппарата длительно гиперфункционирующих клеток. 3. Стадия истощения – эта стадия необязательна, в большинстве случаев адаптация завершается на предыдущей стадии. Наступление этой стадии может быть обусловлено многократным возникновением и изменением процессов адаптации. Возможности систем энергетического и пластического обмена истощаются, нарушается синтез структур, репарации нуклеиновых кислот и т. д. Стресс – генерализованная неспецифическая реакция организма, возникающая под действием различных факторов необычного характера силы и/или действия. Причины возникновения: те же, что и у адаптационного синдрома | |
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|