
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
эффекты. Кроме того, гидрокортизон измен»» ■' иммунный ответ организма Гидрокортизон > рошо всасывается из ЖКТ. 52 страница
Основные патофизиологические изменения, происходящие в организме при феохромоцитоме, связаны с высокой концентрацией катехоламинов в крови (табл. 38.1).
Разнообразие адренергического рецепторного аппарата, большое количество органов, в которых он представлен, возможность смешанной опухолевой секреции, — это факторы, объясняющие, почему клинические проявления феохромоцитомы, в основе которых лежат столь различные патофизиологические механизмы, чрезвычайно разнообразны.
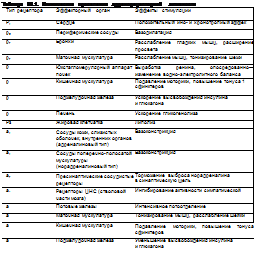 Изменение чувствительности адрено- рецепторов, нарушение механизмов инактивации катехоламинов и энергетическое истощение сосудистых миоцитов на фоне повышенного содержания катехоламинов
Изменение чувствительности адрено- рецепторов, нарушение механизмов инактивации катехоламинов и энергетическое истощение сосудистых миоцитов на фоне повышенного содержания катехоламинов
в сосудистом русле может приводить к развитию катехоламинового шока, для которого характерно резко повышенное АД в центральных сосудах (вазокострик- торный статус) и значительное снижение АД на периферии.
Парадоксальная артериальная гипотония при феохромоцитоме может быть обусловлена прекапиллярным шунтированием, профузной потливостью, хроническими запорами, а также кровоизлиянием в опухоль, левожелудочковой недостаточностью, изолированным влиянием адреналина на Рг-адренорецепторы или развитием катехоламинового шока (в результате изменения чувствительности I адренорецепторов, нарушения механизмов инактивации катехоламинов и энергетическим истощением сосудистых мио- цитов).
Клинические признаки и симптомы
Главным симптомом феохромоцитомы служит повышение АД (пароксизмальное или постоянное).
К дополнительным симптомам отно-
статическая гипотония;
Wboc-гь;
•оянные головные боли;
- .ение внутренней дрожи, беспо-
■ ыцая слабость, снижение трудоспособ-
■улассическом течении феохромоцито- фл говорят при наличии у больных гипер- Ьических кризов, с внезапным повыше- црм, прежде всего, систолического АД, второе может достигать 300 мм рт ст. I зизы могут провоцироваться незначи- «льной физической нагрузкой, пальпа- >1 живота, иногда приемом Р-адрено- ‘"аторов, а при локализации феохро- .ицитомы в стенке мочевого пузыря —- Лучеиспускание м; сопровождаются у чайным сердцебиением (до 180/мин), ^итмиями и/или изменениями на ЭКГ —; типу острой коронарной ишемии *ычно не связанными с нарушением Иронарного кровообращения, а обуслов- •лными прямым токсическим действием катехоламинов). Также во время при-
I да нередко отмечают тремор, шум в ушах, беспокойство или страх, бледность кожных покровов, особенно кистей и стоп (возможен синдром Рейно), расши- венные зрачки, потливость, боли в гру- (и или животе, тошноту или рвоту. Mo- тут выявляться гипергликемия и глю- юзурия, лейкоцитоз. Продолжительность приступа может быть от нескольких шнут (как правило) до нескольких ча- ов (значительно реже). Приступ закан- «ивается обычно внезапно.
Осложнения феохромоцитомы вклю-
»сердечную недостаточность;
• аритмии, тахикардию, АГ в рамках шока или остановку кровообращения во время введения в общую анестезию;
■катехоламиновый шок;
■иврушение мозгового кровообращения;
■почечную недостаточность в рамках
№ гипертоническую энцефалопатию; п ишемический колит;
■расслаивающую аневризму аорты;
■ у беременных: лихорадку, эклампсию.
шок, смерть матери или плода. Возникновение некрозов миокарда, аритмий, повышение уровня кардиоспецифи- ческих ферментов с соответствующими изменениями на ЭКГ и при ЭхоКГ в подавляющем большинстве наблюдений не связаны с изменениями коронарного кровообращения. Причиной изменений является так называемая токсическая катехо- ламиновая миокардиодистрофия.
Длительная гиперкатехоламинемия за счет повышенной постнагрузки и токсического действия катехоламинов на миокард обусловливает развитие гипертрофии миокарда, прогрессирование кардиосклероза, дилатацию камер сердца с появлением в дальнейшем симптомов хронической левожелудочковой недостаточности Гиперкатехоламинемия также служит причиной аритмий, в т.ч. опасных для жизни, и повышенного риска внезапной смерти Катехоламиновый шок сопровождается очень высоким АД в центральных сосудах и нарушением микроциркуляции При феохромоцитоме возможна декомпенсация не выявленного ранее СД или нарушение толерантности к глюкозе
Диагноз и рекомендуемые клинические исследования
Основанием для обязательного обследования для исключения или подтверждения диагноза феохромоцитомы являются следующие симптомы (как изолированные, так и выявленные в любой комбинации).
■ гипертонические кризы с очень высоким АД, обычно проходящие без лечения;
■ АГ у детей:
■ гипертонические кризы, провоцируемые приемом лекарств, наркозом, физической нагрузкой, мочеиспусканием, дефекацией или иными факторами;
■ инциденталома надпочечников,
■ множественные ганглионевромы слизистых оболочек ЖКТ, нейрофиброматоз кожи, гемангиоматоз сетчатки;
■ феохромоцитома в анамнезе у больного или его родственников
Диагностика феохромоцитомы включает лабораторные исследования (определение катехоламинов и/или их метаболитов в крови и моче) и топическую диагностику опухоли.
Лабораторная диагностика
Лабораторная диагностика феохромоцитомы включает1
■ определение концентрации катехоламинов (адреналина, нора дрена л ина) к их метаболитов (ванилилминдальной и гомова нилиновой кислот) в моче, собранной за сутки или за 3 ч, прошедших после начала приступа. Метод недостаточно специфичен: ложноположительные результаты возможны при приеме некоторых ЛС (препаратов рау- вольфии, метилдопы), пищи с высоким содержанием ванилина, после физической и эмоциональной нагрузки, а также у больных с почечной недостаточностью. Все вышесказанное делает метод малоспецифичным;
■ определение свободных катехоламинов в плазме. Перед забором крови больной должен спокойно лежать на спине не менее 30 мин. Метод недостаточно надежен из-за быстрого разрушения катехоламинов (в течение 10— 15 сек), а также из-за низкой специфичности (повышение уровня катехоламинов возможно при тревожности, сниженном ОЦК, ацидоэе, артериальной гипотонии, гипоксии, физической нагрузке, курении, почечной недостаточности, повышенном внутричерепном давлении, ожирении, а также при приеме леводопы, метилдопы, введении гистамина или глюкагона);
■ определение общей концентрации ме- танефринов (метанефрина и нормета- нефрина) в плазме и конъюгированных метанефринов в моче. Это самый надежный метод диагностики феохромоцитомы Даже при невысоком уровне катехоламинов в крови уровень метанефринов в крови при феохромоцитоме всегда повышен. Метанефрины устойчивы в течение 24 ч, поэтому их определение не связано по времени с моментом выброса гормонов опухолью. Метод
и специфичностью (достигают 98%), е пробы. Для подтваУ ормональной активности опухо-
метоклопрамид, физическая нагрузка) и подавляющие (клонидин, фенто*г мин) тесты. (Например, при пробе cm- тамином в/в введение 0,05 мггистамщ,
jIM
3 мин
ние АД, при пробе с фентоламиномв/] введение 5 мг фентоламина через 5 ми° приводит к снижению систолически АД на 35 мм рт. ст. и более, диастолиц* ского АД — на 25 мм рт. ст и более) Эи пробы сопряжены с большим количес- вом осложнений, поэтому использует ся крайне редко.
Топическая диагностика
Локализацию опухоли обычно определи-] ют с помощью УЗИ, КТ, МРТ. Чувстви-J тельность всех методов достаточно ка, составляет 90—96%. Для точной топической диагностики феохромоцитомы обходимо подтвердить ее локализацию - двумя методами (например, УЗИ и КТ или УЗИ и МРТ).
Для установления вненадпоче локализации опухоли или метастазов] злокачественной феохромоцитомы, а также при рецидивах заболевания после оперативного лечения используют ещн тиграфию с мета-ш1-бензилгуанидинш или мета-[37]1-бензилгуанидином.
Дифференциальный диагноз
ррень, головные боли при болезни
Ьсомания (прием амфетаминов, кокала, алкалоидов спорыньи);
Употребление кофеином; мЛС.
повышающие АД (например, з);
пиноподобные JIC; (например, фенил-
а);
ы клонидина, iMAO в сочетании с некоторыми пищевым продуктами и алкоголем; юлевания ЦНС:
^черепно-мозговая травма;
-инсульт, транзиторная ишемичес-
i атака (ТИ А);
• диэнцефальный синдром;
► энцефалит,
•повышенное внутричерепное давление;
^ семейная вегетативная дисфункция; [ — опухоли (нейробластома, ганглионе- врома, ганглионейробластома); ■рциноид;
Ьстоцитоз;
Кроли HI
■йрофиброматоз (болезнь фон Рек- нгхаузена);
; надпочечников, гормонально-неак- ивные опухоли надпочечников,
■ заболевания, сопровождающиеся рез- ими колебаниями АД:
- порфирия;
- отравление свинцом;
-болевые приступы при спинной сухотке;
И столбняк;
- синдром Гийена—Барре.
Клинические рекомендации
Оперативное лечение и лучевая терапия
Самым эффективным и радикальным методом лечения катехоламинпродуциру- ющих опухолей является хирургический. [Необходимым объемом операции при одностороннем поражении является односторонняя адреналэктомия, при двустороннем — тотальная адреналэктомия. Органосохраняющие операции при одностороннем поражении не имеют смысла, при двустороннем поражении — с высокой вероятностью приводят к рецидиву заболевания.
Применяются эндоскопические методы, однако малоинвазивные вмешательства при феохромоцитоме находятся в фазе освоения методики
После тотальной (двусторонней) адре- налэктомии организм лишается источников эндогенных кортикостероидов, и через 5—10 ч после операции развивается надпочечниковая недостаточность. Такие больные нуждаются в пожизненной заместительной терапии кортикостероидными средствами
Лучевая терапия опухолей из хромаф- финных клеток до последнего времени считалась неэффективной. Все более многочисленными становятся сообщения
об успешном лечении метастазов феохро- мопитомы с помощью мета-1-111-бензилгу- анидина.
Предоперационная подготовка
Фармакотерапия изменений, вызванных гиперпродукцией катехоламинов, осуществляется в рамках предоперационной подготовки.
Проведение предоперационной подготовки блокаторами а-адренергических рецепторов показано в группе больных с тяжелой формой феохромоцитомы, т.е. при наличии частых гипертонических кризов, выраженных гиповолемических расстройств, сердечно-сосудистых и церебральных осложнений или нарушении функции почек. Применяются разнообразные селективные и неселективные блокаторы как
а.-, так и Р-адренорецепторов с различной продолжительностью действия. Назначение p-блокаторов возможно после достижения а-блокирующего эффекта При несоблюдении этого условия не исключено парадоксальное повышение АД что связано с устранением вазодилатирующего эффекта адреналина, связанного с его действием на р2-адренорецепторы.
В рамках подготовки к операции или при невозможности хирургического лечения (в этом случае указанные JIC принимают постоянно):
Доксазозин внупгрь 1 мг 1—2 р/сут, при необходимости (сохранение кризов, АД > 160/90 мм рт. ст.) дозу увеличивают на 1—2 мг каждые 1—2 нед до I максимальной дозы 16 мг /сут, перед операцией или пожизненно или I Празозгт внутрь 1 мг 2—3 р/сут, при I необходимости (сохранения кризов,
. АД > 160/90 мм рт. ст.) дозу увеличивают на 1—2 мг 1 р/нед до 3—8 мг
2 р/сут, перед операцией или пожизненно или | Пророксан внутрь 15—30 мг 2 р/сут, при необходимости (сохранение кризов, АД >160/90 мм рт. ст.) дозу | увеличивают 1 р/нед до максимальной — 180 мг/сут, перед операцией I или пожизненно или Феноксибензамин внутрь 10 мг 2 р/сут, при необходимости дозу увеличивают до 20—40 мг 2 р/сут, дозируется по гипотензивному эффекту, перед I операцией или пожизненно
±
1 Атенолол внутрь 12,5—100 мг
2 р/сут, перед операцией или по- [ жизненно или Б-исопролол внутрь 5—10 мг/сут, перед операци ей или пожизненно или Метопролал внутрь 25—100 мг I 2 р/сут, перед операцией или пожизненно или
I Небиволал внутрь 5—10 мг /сут, перед операцией или пожизненно или | Пропранолол внутрь 20—40 мг 4 р/сут,
| перед операцией или пожизненно.
Как правило, только при метастазиру- ющей феохромоцитоме-
I Метирозин внутрь 250 мг 4 р/сут, при необходимости дозу увеличивают до 4 г/сут, перед операцией (доза регулируется по уровню катехоламинов суточной мочи и гипотензивному
I эффекту; перед операцией необходимо принимать J1C не менее 1 нед)
±
| Атенолол внутрь 12,5—100 мг 2 р/сут, перед операцией или
Бисопролол внутрь 5—10 мг/сут, тр*, операцией или Метопролал внупгрь 25—100 т
2 р/сут, перед операциейши Небиволал внутрь 5—10 мг/сут, переи операцией или Пропранолол внутрь 20—40 мг 4 р/г fm I перед операцией.
Терапия при беременности
Основой лечебной стратегии при сочетании феохромоцитомы и беременности должна ' быть адекватная а-адренергическаяблокад да. На фоне правильно проводимого Jiev- ния вопрос о прерывании беременности ия | преждевременном родоразрешенш обьи но возникает при наличии акушерской ил перинатальной патологии Возможно^] одномоментного хирургического вмени тельетва у беременных зависит от стабильности гемодинамических показателей до 1 еле выполнения кесарева сечения. При выполнении адекватной адренергическойбя» I кады пероральными JIC пролонгированию- действия (феноксибензамин, доксазозин. как правило, отмечают неосложненнор. 4 благополучное течение беременности. Необходимо учитывать, что терапия р-адр<- ноблокаторами у беременных перед кес - ревым сечением увеличивает риск гипотъ- нического маточного кровотечения, в связи с чем широкое применение их непосредственно перед и во время операции не показана По жизненным показаниям применяют JIC ультракороткого действия (эсмолол).
Обнаружение феохромоцитомы в первой половине беременности является показанием для прерывания беременности. Наличие феохромоцитомы является абсолютным показанием к проведению кесарева сечения, т.к. этот способ родпраз- решения сопровождается наименьшими перепадами АД и более низкой материнской смертностью.
У беременных при необходимости в добавлении к стандартной терапии а-адре* ноблокаторами Р-адреноблокаторов (при тяжелых аритмиях, выраженной тахикардии) в период подготовки к кесареву сечению назначают:
Эсмолол в/в струйно 500 мкг/кг запер. вую мин введения, затем в/в капелью
а 50 мкг/кг/мин в течение последу- |Н кщих 4 мин, после достижения эф- || фгкта (коррекция. ЧСС, устранение
11 вризпмгш) предо шазот введение со
11 скоростью 25 мкг/кг /мин.
I При недостаточно выраженном эф- 1 фекте к концу 5-й минуты JIC вводят по-
I [38]: 10‘
I Ьсмолал в /е струйно 500 мкг/кг, затем IВ в/в капелъно 100 мкг/кг/мин в тече- § Н ние 4 мин (при повторных попытках IН скорость введения можно повышать
I до 150 мкг/кг /мин. затем до I Щ 200 мкг/кг /мин).
Послеоперационная иместительная терапия
Втигельная терапия после операции русторонней адрсналэктомтг:
Гидрокортизон в /в 25—50 мг через каж-
■ дые 4 чв 1—2-е сут после операции, 25- I ЬОмг каждые 5 ч на 3-и сут, 25—50 мг Н каждые 6 ч на 4-е сут, 25—50 мг каж- Н дые 8чна 5-е сут, 25—50 мг каждые
■ 12чна 6-е сут и 25—50 мг 1 р/сут ут- W рай на 7-е сут, затем J1C отменяют
Гидрокортизон внутрь 10 мг 3 р/сут с Щ 3—4-х сут после операции (после вос- Н становления функций ЖКТ), пожиз-
Флудрокортизон 100 мг 1 р/сут ут- Ш ром, пожизненно.
Оценка эффективности лечения (в т.ч. уменьшение депрессии сегмента ST, урежение аритмий, уменьшение размеров камер сердца, повышение фракции выброса левого желудочка и т.д.).
Осложнения и побочные эффекты лечения
На начальном этапе применения а-адре- ноблокаторов может быть отмечена значительная постуральная артериальная гипотония.
Следует помнить, что пророксан при феохромоцитоме не только значительно менее эффективен, чем другие а-адре- ноблокаторы, но и противопоказан при нарушениях коронарного и церебрального кровообращения, при которых его применение сопряжено с высоким риском побочных эффектов.
Е См. также раздел I.
Ошибки и необоснованные назначения
Неоправданна отмена пролонгированных а-блока торов (феноксибензамина, докса- зозина) или уменьшение их дозы при развитии в начале применения ортостатической артериальной гипотонии. Этот эффект обусловлен исходным, патогенетически обусловленным дефицитом ОЦК, а не прямым действием JIC. В вачале приема указанных средств необходимо соблюдение строгого постельного режима в течение 2—3 дней, после чего происходит компенсация явлений гиповолемии. Дозу JIC необходимо ежедневно постепенно повышать до достижения вышеуказанных критериев эффективности лечения.
Вопреки существующим взглядам о феохромоцитоме как о болезни, проявляющейся только лишь высокими цифрами АД, наиболее тяжелой категорией больных являются пациенты со стойкой артериальной гипотонией или тенденцией к гипотонии в межприступном периоде У этих больных пероральные а-адреноблокаторы пролонгированного действия являются средством выбора, которое позволяет избежать состо
яния «неуправляемой гемодинамики» и ка- техоламинового шока. Тем не менее наличие исходной гипотонии зачастую ошибочно считают противопоказанием к применению а-адреноблокаторов. В качестве аргумента фигурирует опасность усугубления гипотензивного эффекта
При нормальном или умеренно повышенном АД и наличии тахикардии (постоянной или пароксизмальной) типичной ошибкой является назначение Р-адрено- блокаторов без предварите пьного (или одномоментного) приема а-адреноблокато- ров. В результате возможно парадоксальное увеличение тяжести и частоты гипертонических кризов (за счет устранения действия адреналина на (32-адренорецеп- торы).
Нередко встречается гипердиагностика ишемических изменений миокарда у больных с катехоламиновой миокардио- дистрофией, что приводит к существенной задержке оперативного лечения.
Прогноз
В 30—60%- наблюдений диагноз феохромоцитомы устанавливается посмертно. Больные с нераспознанными опухолями умирают, как правило, от последствий тяжелых сосудистых осложнений в бассейне сердечных или мозговых артерий на фоне злокачественно протекающей АГ.
При хирургическом лечении периопе- рационная летальность в специализированных учреждениях составляет 1—4%.
В течение 5 лет после операции выживают обычно более 9Ьсс больных, частота рецидивов не достигает 10®л Наиболее часто рецидив феохромоцитомы развивается у больных, ранее оперированных по поводу множественных эктопированных опухолей, и при семейной форме заболевания.
Литература
2. Казеев К.Н. Доброкачественные и &-■- качественные катеасолалтипродуцт* м рующие опухоли хром аффинной тка ни: Дисс. д.м.н. М., 1974.
3. Неймарк М.И., Калинин А.П Ане-*и- зия и интенсивная терапия в эноо кринной хирургии. Барнаул, 1995. *
4. Николаев О.В., Меншиков В.В., Кали нин А.П. и др Феохромоцитома Медицина, 1965
5. Хирургия надпочечников. Под рес
Н.А. Майстренко. 2000.
6. Райхлин Н.Т., Кветной И.М., Осад чук М.А. APUD-система. Обнинск, 199?
7. Anderson K.J., Lynch Н.Т. Familial ri* for neuroendocrine tumors. Cierr. Opa Oncol. 1993; 5: 75—84.
8. Bravo E.L. Evolving concepts in the pathophysiology, diagnosis, and treat• ment of pheochromocytoma. Endocr. Res 1994; 15: 356-368.
9. Eisenhofer G. Plasma metanephrines a* markers of pheochromocytoma produced by catechol-O-methyltransferase withfr tumors. J. Clin. Endocrinol. iWetab. 199Г, 83(6): 2175—2185.
10. Fudge T.L., et al. Current surgical management of pheochromocytoma dwing pregnancy. Arch. Surg. 1980.
11.Goldfien A. Phaeochromocytoma. Cti* Endocrm. and Metabol. 1981,10 (3): 607— 630.
12. Manger W.M., Gifford R.WJr. Pheochromocytoma. New York: Springer-Verlag, Ш[39]
13.Pears A.G.E Common cytochermcal and ultrastuctural characteristics of ceR prodding polypeptide hormons (of the APU£ series) and ultimobranchial С-cells and calcitonin. Proc. R. Soc. (Biol.) 1968; 170—171.
14. Revillon Y., Daher P., Jan D., Buzsson f Bonnerot V.. Martelli H., Nihoul-FeketeK Pheochromocytoma in children: 15 casi« J. Pediatr. Surg. 1992; 27 (7): 910-911.
15. Sipple J.H The association of pkeochro- mocytoma with carcinoma of thyroid gland. Am. J. Med. 1961; 31: 163 p.
16. Sisson J.C., et al. Scintigraphic localization of pheochrovwcytoma. N. Engl. J Med. 1981.
17. St. John W.M., Gifford R.W. Preivlence of clinically unsuspected pheochromocy toma. Mayo Clin. Proc. 1981.
Глава 39. Задержка полового развития
 Задержка полового развития (ЗПР) — отсутствие вторичных половых признаков у детей, достигших верхнего возрастного предела нормального пубертата.
Задержка полового развития (ЗПР) — отсутствие вторичных половых признаков у детей, достигших верхнего возрастного предела нормального пубертата.
В европейской популяции 95°с мальчиков вступают в пубертат к 14 годам и 95% девочек — к 13 годам
На практике критерием оценки наступления полового созревания у мальчиков является увеличение объема тестикул > 4 мл, у девочек первым проявлением пубертата является увеличение молочных желез.
Таким образом, отсутствие увеличения объема тестикул у мальчиков к 14 годам и отсутствие увеличения молочных желез у девочек к 13 годам расценивается как задержка пубертата.
Следует отметить, что появление вторичного оволосения (лобкового и аксиллярного) не следует считать маркером полового созревания Половое оволосение может быть результатом андрогенной активности надпочечников (адренархе) и наблюдается у пациентов даже с выраженными формами гипогонадизма. Преобладающее большинство подростков, не вступивших в пубертат до 14-летнего возраста, имеют лишь функциональную задержку полового созревания, однако у 0,1% подростков причины задержки полового созревания имеют органическую природу, обусловленную патологией ги- поталамо-гипофизарной системы (гипогонадотршный гипогонадизм) или патологией гонад (гипергонадотроп- ный гипогонадизм).
Классификация задержки полового развития и гипогонадизма:
■ функциональная задержка пубертата:
— конституциональная задержка роста и пубертата;
— задержка роста при хронических системных заболеваниях;
— задержка роста при недостаточном питании и неадекватных энергозатратах;
• гипогонадотропный гипогонадизм:
— врожденные формы гипогона дотропного гипогонадизма:
— синдром Кальмана;
— множественный врожденный дефицит тропных гормонов гипофиза:
генетические дефекты формирования аденогипофиза;
септико-оптическая дисплазия (синдром Мог- sier);
— врожденная гипоплазия надпочечников и гипогонадотропный гипогонадизм у мальчиков (му
СХЕМА ПОЭТАПНОГО ВЕДЕНИЯ ПАЦИЕНТОВ
 Функциональная задержка пубертата
Функциональная задержка пубертата
• У мальчиков допубертатный объем яичек (3-4 мл)
• У девочек’ отсутствие развития молочных желез, менструальной функции
к 13—14 годам
• У подростков обоего пола:
—вторичные половые признаки, вторичное оволосение отсутствуют
—задержка роста, дифференцировки костного скелета
—пропорции тела не нарушены/евнухоидные (на фоне ожирения)
-снижение МПКТ Врожденные формы гипогонадотропного гипогонадизм Синдром Кальмана
• Гипогонадотропный гипогонадизм
• Пороки развития мочеполовой системы:
—агенезия почек
—подковообразная почка
— крмпторхизм, микропенис « Пороки развития ЦНС
-спастические параплегии
—глухота
—горизонтальный нистагм
—нарушения цветного зрения
—незаращения неба и верхней губы
—задержка умственного развития
• Отставание роста и костного возраста
с 13—14 лет, способность к линейному росту сохраняется до 20 лет и более, евнухоидные пропорции тела Множественный врожденный дефицит тропных гормонов гипофиза
• Генетические дефекты формирования аденогипофиза:
—ГР-дефицит (нанизм)
—ТТГ-дефицит (гипотиреоз)
■ Септико-оптическая дисплазия (синдром Morsier):
—односторонняя/двусторонняя атрофия ДЗН
—задержка роста к 2—3 годам
— гипогонадотропный гипогонадизм Врожденная гипоплазия надпочечников и гипогонадотропный гипогонадизм у мальчиков (мутация гена DAX1)
• Глюкокортикоидная недостаточность
• Синдром потери соли
• Гипогонадотропный гипогонадизм
• Семейный анамнез
Окончание схемы поетапного ведения пациентов
ДИАГНОЗ И РЕКОМЕНДУЕМЫЕ КЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ
Диагностический поиск-
(конституциональная )/органическая (гипогонадизм) задержка пубертате —гипо-/гиперго над отроп н ый гипогонадизм
—характер пубертата у родителей -специфические симптомы (аносмия при синдроме Кальмана)
—задержка умственного развития (при синдроме Клайнфельтера)
Осмотр-
-пропорции тела
ч (синдром Клайнф (синдром Прадера—Вилли) —полидактилия (синдром Лоуренса—Муна— Барде—Би для)
-антропометрия
— оценка полового развития по шкале Tanner
—костный возраст
—кариотипирование
— определение базального уровня ЛГ,
ФСГ, Т, Э2
—проба с аналогом ГнРГ (бусерелин, трипторелин)
• Лабораторные исследования
— определение ночной секреции ЛГ, суммарной экскреции ЛГ с мочой
—исследования тиреоидных гормонов, кортизола
— ПРЛ
• Функциональные тесты.
—стимуляция секреции ПРЛ (с ТРГ, метоклопрамидом)
—стимуляция секреции ГР
—тест с ХГ у мальчиков
• Инструментальные исследования-
—рентгенография черепа (краниофарингиомы)
—КТ и МРТ головного мозга
—УЗИ органов малого таза
—офтальмологическое исследование
КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ
—препараты половых гормонов (в т.ч. анаболические стероиды)
—препараты ХГ
—препараты ГР
—дефект рецептора ГнРГ;
—врожденные множественные сочетанные дефекты развития (синдром Прадера—Вилли, синдром Лоуренса—Муна—Барде—-Биддл);
—приобретенные формы гипогонадо- тропного гипогона дизма:
опухоли гипоталамо-гипофизар- ной области (краниофарингиомы, аденомы гипофиза, супраселляр- ные глиомы);
инфекционные поражения ЦНС (менингит, энцефалит); облучение ЦНС;
■ гипергонадотропный гипогонадизм:
— врожденные формы гипергонадот- ропного гипогонадизма:
хромосомные аномалии (синдром Шерешевского—Тернера (СШТ), синдром Клайнфельтера); анорхизм;
дефект рецептора ЛГ/ХГЧ (вызывает синдром резистентных яичников у девочек и гермафродитизм/гипогона дизм мальчиков); нарушения стероидогенеза в гонадах (дефект ферментов Р450с17, StaR-протеинэ вызывают клиниче-
скую картину гипогонадизма у девочек и гермафродитизма у мальчиков):
— приобретенные формы гипергона до- тропного гипогонадизма:
инфекции (эпидемический паротит, краснуха);
травма, перекрут яичка, перекрут яичника;
облучение, противоопухолевая терапия;
аутоиммунный процесс Отсутствие или снижение способности гипоталамуса секретировать ГнРГ или гипофиза секретировать ЛГ, ФСГ приводит к развитию гипогонадотропного гипогонадизма. В его основе лежат врожденные или приобретенные аномалии ЦНС и ги- поталамо-гипофизарных структур, приводящие к:
■ изолированному повреждению гонадотропной секреции,
■ множественному выпадению тройных функций гипофиза;
■ дефектам развития многих органов и систем, сочетающихся с гормональными нарушениями.
Гипергонадотропный гипогонадизм (первичная гонадная недостаточность) сопровождается значительным повышением уровня гонадотропных гормонов вследствие отсутствия негативного подавляющего влияния половых гормонов на гипоталамо- гипофизарные структуры (принцип отрицательной обратной связи) Большинство врожденных форм гипергонадотропного гипогонадизма ассоциировано с хром°^ I ными и генетическими аномалиями и ^ ■ то сопровождается множеством соуш ^ I ских нарушений, описанных в воде I ромов. Наиболее частыми причм^Я и врожденного гипергонадотропного гиш I надизма у детей являются заболей»# I связанные с дефектами половых х£«. сом— делецией или структурными иг- малиями второй Х-хромосомы (СШТ, | дополнительной Х-хромосомой вмужя| кариотипе (синдром Клайнфельищ^ Значительно реже встречаются вроизя- ные формы гипергонадотропного т*г - надизма, ассоциированные с так назьан- мой «чистой» гонадной агенезией. Пола®* отсутствие гонадной дифференцировщ| этих случаях не сопровождается хро#- сомными аномалиями. С некоторыми* «га ворками к парциальным формам гонад*?, недостаточности следует относить вр -- денные аномалии половой дифферж цировки, обусловленные как пато«1Я ей формирования гонады (тестикуля{шЯ дисгенез), так и врожденными дефект**^ биосинтеза половых стероидов или нар\- шениями их клеточного метаболизма I Приобретенные формы гонадной статочности могут быть следствием |м рургического или инфекционного воз,^ ] ствия и проявляться только клиничео^] ми симптомами гипогонадизма. Аутайи мунный характер повреждения функцв гонад может сочетаться с другими ayi • иммунными нарушениями зндокриннвИ и неэндокринного характера.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|