
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
эффекты. Кроме того, гидрокортизон измен»» ■' иммунный ответ организма Гидрокортизон > рошо всасывается из ЖКТ. 41 страница
Нарушения репродуктивной функции
включают симптомы гипогонадизма.
■ первичную либо вторичную аменорею, опсоменорею, олигоменорею, ановуля- цию, укорочение лютеиновой фазы,
■ бесплодие (основная причина обращения к врачу у женщин и мужчин);
■ гипоплазию матки при гинекологическом осмотре;
■ галакторею1 (служит первым симптомом заболевания не более чем у 20% больных и еще реже является основной жалобой, может отсутствовать даже при значительном повышении содержания пролактина),
ность галактореи оценивают по следующей шкале- единичные капли при сильном надавливании (+), обильные капли при сильном надавливании (++), спонтанное отделение молока (+++).
■ патологические изменения молочных желез (инволютивные изменения, фиб- розно-кистозная мастопатия), обусловленные как гипоэстрогенией, так и прогестерон-дефицитным состоянием;
■ у мужчин — снижение либидо и потенции; гинекомастия и галакторея встречаются не всегда.
Психоэмоциональные расстройства при гиперпролактинемии включают.
■ астению;
■ колебания настроения с тенденцией к гипотимии;
■ сужение интересов;
■ психонегативные нарушения;
■ замедление ассоциативного процесса;
■ нарушение концентрации внимания и памяти.
В целом для больных с гиперпролакти- немией характерен особый психоэндокринный синдром: повышенная раздражительность, тревожность, склонность к депрессивным и психовегетативным реакциям, эмоциональная лабильность, стеничность при выполнении узконаправленной деятельности, низкая толерантность к изменениям и аутизация, психосоциальная дезадаптация. Предположительно помимо реакции пациенток на имеющееся бесплодие или нарушения менструального цикла психопатологические сдвиги могут быть связаны с дисфункцией нейромедиаторных систем, обусловленной генетически либо перенесенным в анамнезе психическим стрессом.
К эндокринно-обменным изменениям
относятся:
■ инсулинорезистентиость (типичное проявление заболевания; хотя частота явного СД при ГГ не выше, чем в популяции);
* увеличение массы тела (наблюдается у 60% больных, при этом избыточная масса тела и ожирение I степени встречаются у трети женщин вне зависимости от формы заболевания, в то время как ожирение II—1П степени вдвое чаще развивается при пролактиномах, чем при иди- опатической гиперпролактинемии);
■ изменения липидного спектра крови (повышение содержания атерогенных фракций липидов);
■ снижение МПКТ при длительной не- корригируемой гиперпролактинемии, с развитием остеопении либо остеопороза у больных репродуктивного возраста (потери МПКТ могут достигать 3,8$, в год).
Прочие нарушения: аденомы с инфрасел- лярным ростом вызывают появление ри- нореи или воспалительных процессов основной пазухи, хотя иногда при таком типе инвазии неврологическая симптоматика может отсутствовать.
Наиболее полные клинические формы заболевания — выделение молоко- подобной жидкости из молочных желез, аменорея и бесплодие — чаще встречаются у женщин с пролактино- мами.
При ином генезе заболевания имеют место нарушения менструального цикла преимущественно по типу опсоменореи либо отмечается неполноценность лютеи- новой фазы; обращает внимание обилие жалоб вегетативного характера
Диагноз и рекомендуемые клинические исследования
Основными в диагностике ГГ являются следующие этапы:
■ оценка клинического симптомокомп- лекса (см. выше);
■ подтверждение и оценка выраженности гиперпролактинемии,
■ установление генеза гиперпролактинемии;
■ выявление эндокринно-обменных нарушений.
Подтверждение и оценка выраженности гиперпролактинемии
Вероятность опухолевого генеза гиперпролактинемии увеличивается при значениях пролактина, превышающих 2000— 3000 мкЕД/мл. При небольших отклонениях от нормы («пограничная», «мягкая» гиперпролактинемия) целесообразно проведение двух-<грехкратных исследований во избежание ошибочных заключений, поскольку уже сама манипуляция по забору крови как стрессорный фактор может явиться причиной умеренной гиперпро- Шктинемии.
Установление генеза гиперпролактинемии
Для определения причины гиперпролакти- иемии ранее использовали функциональные пробы (с метоклопрамидом и тироли- Еерином). Однако их результаты неспецифичны и непостоянны. Хотя в целом снижение либо отсутствие реакции на введение тиролиберина и метоклопрамида характерно для больных с пролактиномами, аналогичная реакция может отмечаться и при гиперпролактинемии любого иного генеза. С другой стороны, у 10—15% больных с пролактиномами выявляют нормальную реакцию на фармакологические тесты.
Топическая диагностика
Основными методами, позволяющими выявить или исключить образование гипоталамо-гипофизарной области (ма- кро- либо микроаденомы), являются КТ иМРТ (последняя предпочтительнее). Критерием диагноза идиопатической гиперпролактинемии является стойкое повышение содержания пролактина в сочетании с отсутствием явной патологии гипофиза. Такое заключение можно вынести лишь после исключения всех остальных возможных причин повышения уровня пролактина
Дополнительные методы исследования
В план обследования больных необходимо включать определение в сыворотке крови гонадотропных гормонов и половых стероидов, при избыточной массе тела — уточнение состояния углеводного и жирового обменов, оценку гинекологического, психического и неврологического статусов, определение МПКТ, при наличии макроаденомы — исследование глазного дна и периметрию.
Дифференциальный диагноз
С целью дифференциальной диагностики первичного ГГ с другими формами гиперпролактинемии помимо оценки клинической симптоматики (что в большинстве случаев позволяет отвергнуть наличие иных нейроэндокринных заболеваний) требуется тщательный сбор «лекарственного» анамнеза, проведение лабораторноинструментального обследования, направленного на исключение гипотиреоза, синдрома поликистозных яичнике©; опухолей надпочечников, яичников и яичек, сопровождающихся гиперэстрогенемией; тяжелой патологии печени и почек и других состояний и заболеваний, характеризующихся нарушением синтеза и секреции пролактина (см. «Классификация синдрома гиперпролактинемии») Диагностика феномена макропролактинемии проводится с помощью метода гель-фильтрации.
Клинические рекомендации
При лечении гиперпролактинемии требуется решение следующих задач:
■ нормализация уровня пролактина;
■ восстановление фертильности;
■ удаление, либо достижение регрессии, либо стабилизация роста аденомы при опухолевых формах заболевания;
■ устранение галактореи,
■ нормализация менструального цикла;
■ устранение связанных с гиперпролак- тинемией сосудистых, эндокринно-обменных и эмоционально-личностных нарушений.
Консервативное лечение
При первичном ГГ методом выбора является терапия агонистами дофамина, реже при пролактиномах необходимо проведение оперативного вмешательства либо лучевой терапии. При ином генезе повышения продукции пролактина проводится патогенетическая терапия основного заболевания. При феномене макропролактинемии лечение не требуется.
Основным регулятором (ингибитором) синтеза и секреции пролактина является дофамин В настоящее время выделено, клонировано и охарактеризовано с помощью молекулярно-биологических, биохимических и фармакологических методов 5 подтипов рецепторов дофамина По отношению к рецепторам дофамина 2-го типа, располагающимся на лактотрофах, выделяют неселективные (бромокриптин) и селективные (хинаго- лид, каберголин) агонисты дофамина. Хотя возможны спонтанные ремиссии заболевания, в большинстве случаев медикаментозная терапия проводится длительно, иногда пожизненно' Бромокриптин внутрь 0,625 мг I * Р/сУт на ночь с приемом пищи, в течение 1-й недели дозу увеличивают до 2,5 мг на ночь с приемом пи- 1 щи; при необходимости дальнейшее увеличение дозы проводят на
2.5 мг/нед под контролем уровня I пролактина в крови (основная
цель — достижение нормальных значений гормона) до максимальной дозы 12,5 мг/сут (при дозе более
2.5 мг/сут ЛС назначается дробно,
2— 3 р/сут) или
Каберголин внутрь 0,25—0,50 мг вечером во время еды 2 р/нед; при необходимости дальнейшее увеличение дозы проводят на I 0,5 мг/мес под контролем уровня пролактина в крови (основная цель - достижение нормальных | значений гормона) до максимальной дозы 2 мг 2 р/нед или Хигшголид внутрь 25 мкг 1 р/сут перед сном, с небольшим количеством пищи в 1-е 3 дня, затем постепенно повышают дозу каждые 3 дня на 25 мкг; с 7-го дня I с уточная доза, составляет 7 5 мкг; при необходимости дальнейшее увеличение дозы проводят на
7£ мкг /тес под контролем уровня пролактина в крови (основная цель — достижение нормальных значений гормона) до максимальной
1дозы 150—300 мкг/сут (вся доза назначается однократно).
Дофаминомиметики не только обеспечивают достижение нормопролактинемии, но и обладают антимитотическим эффектом.
В период определения оптимальной дозы дофаминомиметиков уровень пролактина определяют ежемесячно, после достижения нормопролактинемии — 1 раз в 6 месяцев.
Селективные дофаминомиметики в настоящее время не являются ЛС выбора при бесплодии, обусловленном гиперпро- лактинемией. Хинаголид и каберголин применяют при отсутствии жалоб на бесплодие либо при наличии резистентности, непереносимости неселективных дофаминомиметиков у страдающих бесплодием пациентов. Зачатие на фоне селективных дофаминомиметиков не является показанием к прерыванию беременности. Учитывая возможность ремиссии, при идиопати- ческой форме гиперпролактинемии целесообразна ежегодная отмена ЛС сроком на 1—2 месяца под контролем уровня пролактина и оценки клинической симптоматики (в подобных случаях нормальные концентрации пролактина после отмены дофаминомиметиков повышают вероятность восстановления функции нейроэндокринной системы). После достижения нормопролактинемии в течение первых
2лет повторные исследования пролакти- немии осуществляются 1 раз в 4—б месяцев, затем ежегодно. При опухолевом гене- зе заболевания плановая отмена ЛС возможна 1 раз в 2 года. При пролактиномах требуется ежегодное динамическое проведение МРТ головного мозга.
В случае беременности все агонисты дофамина отменяют. Показанием к возобновлению фармакотерапии в этот период является нарастание выраженности клинических проявлений, рост опухоли, подтвержденный результатами периметрии (определения полей зрения) и данными МРТ головного мозга.
Хирургическое лечение
Показаниями к хирургическому вмешательству является неэффективность, непереносимость медикаментозной терапии, апоплексия гипофиза.
Лучевая терапия
Лучевая терапия показана при рецидиве опухоли после оперативного вмешательства, отказе пациента от оперативного вмешательства, тяжелой соматической патологии, не позволяющей провести хи- I рургическое лечение.
Оценка эффективности лечения
Критериями эффективности лечения являются нормализация уровня про- Вактина, восстановление менструального цикла и фертильности у больных репродуктивного возраста, отсутствие роста пролактином при ежегодной МРТ головного мозга.
Осложнения и побочные эффекты течения
^ Также см. раздел I.
Бромокриптин, помимо 02-рецепторов, взаимодействует с D,-рецепторами, ai-ад- ренорецепторами и серотониновыми рецепторами. Этим обусловлено развитие достаточно широкого спектра побочных эффектов на фоне терапии.
Нежелательные эффекты, обусловленные приемом бромокриптина, наблюдаются преимущественно со стороны ЖКТ, сердечно-сосудистой и нервной систем.
Тошнота и рвота беспокоят до 60% больных, запоры —10%, у 25% пациентов возможно развитие постуральной гипотензии и синкопальных состояний, реже отмечается сухость во рту и симптоматика рефлюкс-эзофагита. JIC лучше переносится при приеме основной дозы в вечернее время На фоне назначения больших доз (30—75 мг/сут) у трети больных развивается синдром Рейно, у 10% — судороги в икроножных мышцах, приливы и затруднение носового дыхания (указанные дозы используются преимущественно для лечения болезни Паркинсона, при гиперпролактинемии они практически не применяются).
Побочными эффектами со стороны нервной системы обычно являются головные боли, реже — бессонница, однако при применении высоких доз увеличивается вероятность появления общей слабости, депрессии, слуховых галлюцинаций, диплопии, психозов. Как правило, при использовании режима средних терапевтических доз подавляющее большинство побочных эффектов наблюдается лишь на начальных этапах лечения и может быть сведено до минимума при постепенном наращивании дозы. В среднем побочные эффекты могут наблюдаться у 23% больных в течение первых недель терапии.
Тем не менее до 12% пациентов вынуждены прерывать лечение из-за выраженных побочных реакций. Возможно, возникновение нежелательных эффектов связано с быстрым всасыванием бромокриптина в ЖКТ, что сопровождается выраженными колебаниями концентрации JIC в крови.
Еще одной проблемой, возникающей при использовании бромокриптина, является резистентность к JIC, регистрируемая у 5—17% больных
Каберголин и хинаголид не являются абсолютно селективными по отношению к Б2-рецепторам, избирательность этих JIC определяется лишь константами связывания и диссоциации. По сравнению с бромокриптином частота и выраженность побочных эффектов при применении селективных дофаминомиметиков существенно меньше, тем не менее у ряда больных, получающих эти JIC, также отмечаются затруднение носового дыхания, запоры, артериальная гипотония.
Ошибки и необоснованные назначения
Ошибочным является продолжение терапии дофаминомиметиками в период беременности, после родов — запрет грудного вскармливания и назначение JIC без четких доказательств увеличения размеров опухоли. У здоровых женщин в период беременности под воздействием возрастания концентрации эстрогенов содержание пролактина повышается, что необходимо не только для дальнейшей дифференциации клеток молочной железы, но и для становления иммунной системы плода. Учитывая, что пролактин играет важную роль в синтезе сурфактанта, превентивное назначение агонистов дофамина на протяжении всего срока вынашивания
плода у всех женщин с ГГ нельзя считать оправданным, стремление поддерживать нормопролактинемию может явиться причиной развития у ребенка респираторного дистресс-синдрома.
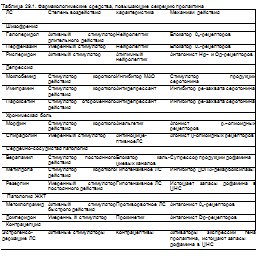
Нецелесообразно использовать у таких больных JIC, вызывающие повышение уровня пролактина (табл. 29.1).
Прогноз
 Применение агонистов дофамина позволяет добиться нормализации уровня пролактина в крови более чем у 80Г6 больных. При пролактиномах под действием этих JIC также отмечается уменьшение размеров опухоли. Даже при исходных нарушениях зрения назначение агонистов дофамина часто вызывает нормализацию зрительной функции После транссфеноидальной резекции ми- кропролактином содержание пролактина нормализуется в течение первых суток у 80—90% больных, но при этом частота рецидивов в ближайшие после успешной рапии годы составляет в среднем 17%, г рез б лет может достигать 40^с -При макро-
Применение агонистов дофамина позволяет добиться нормализации уровня пролактина в крови более чем у 80Г6 больных. При пролактиномах под действием этих JIC также отмечается уменьшение размеров опухоли. Даже при исходных нарушениях зрения назначение агонистов дофамина часто вызывает нормализацию зрительной функции После транссфеноидальной резекции ми- кропролактином содержание пролактина нормализуется в течение первых суток у 80—90% больных, но при этом частота рецидивов в ближайшие после успешной рапии годы составляет в среднем 17%, г рез б лет может достигать 40^с -При макро-
лолактиномах концентрация пролактина [нормализуется у трети пациентов, но час-
Iюта рецидивов у них может достигать 80%.
IЛитература
I.Дедов И.И., Мельниченко Г. А. Персис- тирующая гсигакторея-сипенорея. М.: Медицина, 1985.
2. Романцова Т.И. Особенности клинической симптоматики, диагностики и лечения синдрома гиперпролактине- мии у женщин. Дисс.. . д м.н. М., 2001.
3- Ben-Jonathan JV., Hnasko R. Dopamine as a prolactin inhibitor. Endocrine Reviews 2000; 22 (6): 724—763.
4. Molitch M.E. Prolactinomas. In. The Pituitary. Eds. by S. Melmed. MA, Cambridge: Blacwell Science, 1995; 443—477.
Глава 30. Синдром неадекватной секреции антидиуретического гормона
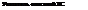 Синдром неадекватной секреции антидиуретического гормона (СНС АДГ) (синдром гиперсекреции АДГ, синдром неадекватной продукции вазопрессииа, перпексический синдром, синдром Пархона, несахар ный антидиабет) — клинический симптомокомп леке, при котором избыточная нерегулируемая реция АДГ либо усиление действия АДГ на кл дистальных отделов нефрона приводит к формиро ванию гипонатриемической (гипоосмолярной) пергидратации.
Синдром неадекватной секреции антидиуретического гормона (СНС АДГ) (синдром гиперсекреции АДГ, синдром неадекватной продукции вазопрессииа, перпексический синдром, синдром Пархона, несахар ный антидиабет) — клинический симптомокомп леке, при котором избыточная нерегулируемая реция АДГ либо усиление действия АДГ на кл дистальных отделов нефрона приводит к формиро ванию гипонатриемической (гипоосмолярной) пергидратации.
Эпидемиология
Частота СНС АДГ не уточнена, заболевание возникает одинаково часто у лиц обоего пола в любом возрасте.
Классификация
СНС АДГ может быть симптоматическим (см. «Этиология») и идиопатичееким (когда причина его развития неизвестна).
Этиология
| » 1оявляются при уровне натрия в плазме крови li 120 ммоль/л I • Увеличение массы тела . Периферические отеки (могут быть не выражены из-за потери натрия) |( Вялость I» Адинамия || »оловные боли ■I голоеокружение | • Анорексия • Тошнота • Нарушение сна • Тремор • Мышечные судороги ■ Симптомы поражения ЦНС: —дезориентация — аритмия |
| |. Лабораторные исследования — биохимический анализ крови (определе- к ние уровня Na, К, CI) ■ | — определение осмолильности крови Ш (снижена) Н J — определение осмоляльности мочи (повышена > 300 мосм/кг) —общий анализ крови — общий анализ мочи —определение уровня холестерина, общего | • Заболевания печени, почек, сердца • Надпочечниковая недостаточность ■ Гипотиреоз ^ • Синдром идиопатических отеков |
| белка, креатинина, кальция сыворотки —определение уровня гормонов в крови (ТТГ, свободный Т4, альдостерон) • Инструментальные исследования: —обзорная боковая рентгенография черепа 1 -КТ/МРТ -ЭКГ —УЗИ почек | |
| • Коррекция неадекватной продукции АДГ лечение основного заболевания . Ограничение потребления жидкости до 800— 1000 мл/сут • Фармакотерапия: —ЛС, блокирующие действие АДГ на собирательные трубочки | — ЛС, блокирующие секрецию АДГ —диуретики — гипертонический раствор натрия хлорида в/в, поваренная соль внутрь |
| НЕМА ПОЭТАПНОГО ВЕДЕНИЯ ПАЦИЕНТОВ |
| синдром неадекватной секреции АДГ |
Патогенез
Гипонатриемия при СНС АДГ обусловлена увеличением объема внеклеточной жидкости и непосредственно зависит от потребления воды. При нормальном или пониженном потреблении жидкости даже очень интенсивная секреция АДГ не приводит к гипонатриемии. При повышенном потреблении жидкости самое незначительное нарушение механизма регуляции секреции АДГ или механизма регуляции концентрирования мочи может вызвать синдром гиперсекреции АДГ У большинства больных с этим синдромом, несмотря на гипоосмоляль- ность внеклеточной жидкости, постоянно секретируются АДГ или АДГ-подоб- ные пептиды
Клинические признаки и симптомы
■ Олигурия.
■ Увеличение массы тела.
■ Периферические отеки (могут быть не выражены из-за потери натрия).
■ Вялость, адинамия.
■ Головные боли, головокружение.
- Анорексия.
■ Тошнота.
■ Нарушение сна.
■ Тремор.
■ Мышечные судороги.
■ Симптомы поражения ЦНС.
К основным относятся жалобы на уменьшение количества мочи и увеличение массы тела. Положительный водный баланс вызывает гиперволемию и симптомы водной интоксикации: олигурию, головные боли, головокружения, анорексию, тошноту, рвоту, нарушения сна. Первые симптомы водной интоксикации появляются после снижения уровня натрия в плазме крови ниже 120 ммоль/л.
При более выраженной гипонатриемии на первый план выходят симптомы поражения ЦНС: дезориентация, судороги, аритмия и коматозное состо- явие.
Диагноз и рекомендуемые клинические исследования
Диагностика СНС АДГ основана на обнаружении гипонатриемии, гипоосмоляль- ности плазмы и гиперосмоляльности мочи (> 300 мосм/кг) При этом всегда необходимо диагностировать основное заболевание и исключить другие состояния, протекающие с подобными клиническими проявлениями (сж. «Дифференциальный диагноз»), для чего проводят целый ряд исследований.
Лабораторные исследования:
■ биохимический анализ крови (определение уровня Na, К, С1);
- определение осмоляльности крови;
■ определение осмоляльности мочи;
■ общий анализ крови;
■ общий анализ мочи;
■ определение уровня холестерина, общего белка, креатинина, кальция сыворотки крови;
■ определение уровня гормонов в крови (ТТГ, свободного Т4, альдостерона).
Инструментальные исследования:
■ обзорная боковая рентгенография черепа;
■ КТ или МРТ головного мозга,
- ЭКГ;
■ УЗИ почек.
Дифференциальный диагноз
Прежде всего при проведении дифференциальной диагностики необходимо исключить заболевания печени, почек, сердца, надпочечниковую недостаточность, гипотиреоз. Часто проблема заключается в том, что основные признаки СНС АДГ — гипонатриемия, низкий уровень альдостерона в крови — могут быть не выражены из-за бесконтрольного приема больными диуретических средств.
Наибольшие трудности возникают при дифференцировке СНС АДГ с синдромом идиопатических отеков — заболеванием, имеющим много клинически сходных симптомов, но иную патофизиологическую природу. Его патогенез связан с рядом нейрогенных, гемодинамиче- ышх и гормональных изменений, ведущих к нарушению регуляции водно-солевого гомеостаза. Этот синдром характеризуется развитием периферических или распространенных отеков; в легких случаях отмечаются лишь небольшие локальные отеки, нередко наблюдаются только предменструальные циклические отеки. АДГ повышен у всех больных с СНС АДГ, тогда как при идиопатических отеках повышение АДГ наблюдается редко. Уровень альдостерона в крови снижен при СНС АДГ и повышен у большинства больных с идиопатическими отеками. Гипонатриемия и гиперволе- мия, характерные для СНС АДГ, никогда не наблюдаются при идиопатических отеках
Клинические рекомендации
Коррекция неадекватной продукции АДГ проводится путем лечения основного заболевания.
Целью лечения является нормализация осмоляльности плазмы и устранение гипергидратации.
Тактика лечения зависит от скорости развития гипонатриемии (острая или хроническая), концентрации натрия в сыворотке крови и состояния больного.
Необходимо подчеркнуть, что в клинической практике, как правило, используют ограничение потребления жидкости до 800—1000 мл/сут как наиболее действенный и безопасный метод лечения.
Если больному трудно ограничивать потребление жидкости, возможно применение ЛС, блокирующих действие АДГ на собирательные трубочки — демеклоцик- лина или лития карбоната (однако последним применяют редко из-за высокой частоты развития побочных эффектов включая раздражение ЖКТ, нарушения ЦНС, сердечной деятельности и функции ЩЖ).
Имеются сообщения об успешном длительном применении фенитоина, который обладает центральным блокирующим действием на секрецию АДГ.
При уровне натрия в крови 115— 125 ммоль/л:
С Демеклоциклин внутрь 0,6 мг 1—
2 р/сут, 5—7 сут (до наступления клинического улучшения) или Фенитоин внутрь 200—500 мг 1—
2 р/сут, 5—7 сут (до наступления клинического улучшения).
После нормализации состояния назначается поддерживающая терапия с использованием мочевины.
Для поддержания нормального уровнв натрия в крови:
С Мочевина внутрь 30 г /сут, длительно или Фенитоин внутрь 200—500 мг I—2 р/сут, длительно.
В остром периоде при выраженных симптомах водной интоксикации первоочередной задачей является повышение уровня натрия в крови. Для этого применяют в/в введение гипертонического (3%) раствора натрия хлорида в сочетании с мочегонными Л С (фуросемидом; особенно это показано больным с гипово- лемией, т.к. терапия фуросемидом вызывает потерю электролитов с мочой и тем самым снижает риск резкого увеличения объема внеклеточной жидкости) и иногда фенитоином Положительный эффект дает также применение фуросеми- да в комплексе с приемом поваренной соли до 3 г/сут.
При выраженных симптомах вод нем интоксикации (уровне натрия в крови < 115 ммоль/л):
С Натрия хлорид, 3% р-р, в /в 200—
500 мл/сут, во наступления клинического улучшения
+
С Фуросемид в /в 40—120 мг /сут, до наступления клинического улучшения
С Фенитоин в/в 100—300 мг /сут, до наступления клинического улучшения.
Синтез новых аналогов АДГ, обладающих антагонистическим действием по отношению к а нтидиуретическому эффекту вазопрессина, даст возможность в ближайшем будущем лечить СНС АДГ более эффективно и направленно.
Оценка эффективности лечения
Критерии эффективности лечения: при острой гипонатриемии — повышение уровня натрия в крови; при хронической гипонатриемии — нормализация уровня натрия в крови* осмоляль- носги плазмы и устранение гипергидратации
Осложнения и поЬочные эффекты лечения
При назначении демеклоциклина необходимо обращать особое внимание на функцию печени, т к. при печеночной недостаточности он оказывает нефротоксическое действие.
Ошибки и необоснованные назначения
Индуцированная СЯС АДГ корригируется лечением основного заболевания
При СНС АДГ, в отличие от синдрома идиопатических отеков, не следует ограничивать потребление соли.
Несмотря на единичные сообщения о благоприятном влиянии бромокриптина при СНС АДГ, в настоящее время его использование не показано. Механизм диуретического эффекта этого ЛС предположительно связан с усилением активности дофамина, улучшающего почечную гемодинамику и/или уменьшающего потенцирующее влияние пролактина на синтез АДГ (в связи с чем бромокриптин применяется при синдроме идиопатических отеков)
Прогноз
Прогноз в целом благоприятный, но зависит от характера основного заболеваниям причины, вызвавшей СНС АДГ. Тяжелые формы идиопатической СНС АДГ могут приводить к летальному исходу в резут- тате тяжелой водкой интоксикации Полиэтиологичноеть синдрома затрудняет его профилактику, однако низкое потребление жидкости является общим фактором, замедляющим появление клинической симптоматики
Литература
1. Мельниченко ГА , Марова Е.И., Дзера- нова JI.K Диагностика и лечение нейроэндокринных заболеваний. М.: Ада- мантъ, 2002.
2.Batcheller J. Syndrome of inappropriate 1 antidturetic hormone secretion. Crit Care Nurs. Clin. North Am. 1994; 6(4): 687—692
3.Coulson J.M., Edgson J.L., Marskall- Jones Z.V., et al. Upstremal stimulatory factor activates the vasopressin promoter via multiple motifs, including a non-canonical E-box. BiochemJ. 2003; 1: 549—561.
4.Decaux G„ Prospert F , Penmwckx R, Namias B., Soupart A. 5-year treatment of the chronic syndrome of mappropriate secretion of ADH with oral urea. Nephron 1993; 63 (4): 468—470.
5.Fndmann A.S., Malott K.A., MemohVA, et ai. Products of vasopressin gene expression in small-cell carcinoma of the lung. Br J. Cancer 1994: 69 (2): 260-263.
6.Kinzie B.J. Management of the syndrome cj inappropriate secretion of antidiuretic hormone. Clin. Pharm. 1987; 6 (S): 625—633.
[____ Глава 31 Гипопитуитаризм
Глава 31. Гипопитуитаризм
Гипопитуитаризм (гипофизарная недостаточность) — Изолированный синдром, обусловленный полным или частичным вы-
гипопитуитаризм падением секреции тройных гормонов аденогипофиза
(недостаточность гормона и проявляющийся недостаточностью функции соот-
Р°ста) - 459 ветствующих органов периферической эндокринной
Недостаточность системы
лютеинизирующего и Изолированный гипопитуитаризм — снижение
фолликулостимулирующего секреции только одного тройного гормона аденогипо- юв (вторичный. физа (например, изолированный гипогонадотропный
погонадотропный, гипогонадизм, изолированная недостаточность гор-
«адизм) 463 мона роста (ГР).
чный Частичный (парциальный) гипопитуитаризм — со-
феоз .470 четанное выпадение секреции двух или трех (но не
чнь,й всех) тропных гормонов гипофиза.
>ртицизм 473 Тотальный гипопитуитаризм (пангипопитуита-
попитуитаризм 478 ризм) — снижение или прекращение секреции всех тропных гормонов аденогипофиза.
Межуточно-гипофизарная недостаточность — сочетание гипопитуитаризма и несахарного диабета.
Врожденный гипопитуитаризм с одинаковой частотой встречается у мужчин и женщин. Частота врожденного гипопитуитаризма составляет в среднем 1 случай на 10 ООО—15 ООО населения. Основной контингент больных с приобретенным гипопитуитаризмом составляют женщины 30—60 лет. Это объясняется тем, что заболевания, приводящие к развитию гипопитуитаризма, чаще встречаются у женщин.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|