
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Нәруыздың төртінші реттік құрылымы
Нә руыздың тө ртінші реттік қ ұ рылымы
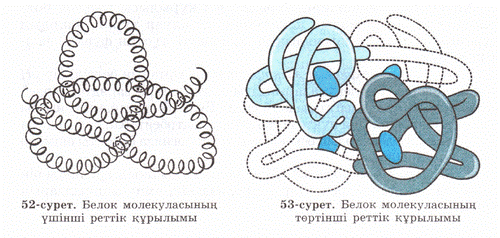
Кейбір нә руыздардың ерекше қ ұ рылымы болады. Олар бір-бірімен байланысқ ан бірнеше пептидтерден қ ұ ралады. Қ ұ рылысы жағ ынан жақ ын бірнеше нә руыздың ү шінші реттік қ ұ рылымының шумақ тү зіп орналасуын нә руыз молекуласының тө ртінші реттік қ ұ рылымы дейді. Тө ртінші реттік қ ұ рылым- бірнеше нә руыз молекулаларының қ осындысы, мысалы, гемоглобин нә руызы тө рт шумақ тан тұ рады. Олар иондық, сутектік байланыстарме, байланысады. Осы тө отінші реттік қ ұ рылыммен жаң а қ асиет нә руыз қ ызметінің реттелуі пайда болады. Тө ртінші реттік қ ұ рылыммен реттелу процестерінің қ ұ пиясын ашқ ан – француз ғ алымы, Нобель сыйлағ ының лауреаты- Жак Моно (1961 ж). Тө ртінші реттік қ ұ рылымда субстратқ а ұ қ самайтын заттар – реттегіштер болады.
26. сұ рақ Нә руыздардың қ асиеттері
Ақ уыздар – жасушаның ең маң ызды макромолекуларының бірі болып табылады. Оның элеметтік қ ұ рамын, қ ұ рылысының теориясын алғ ашқ ылардың бірі болып зерттеген жә не протеин (protein-бірінші) деп атауды ұ сынғ ан Голландия химигі жә не дә рігері Г. Я. Мульдер болатын. Ақ уыз организмдер тіршілігінде олардың қ ұ рылысы дамуы мен зат алмасуына қ атысуы арқ ылы ә ртү рлі жә не ө те маң ызды қ ызмет атқ арады. Ақ уыздар органикалық заттар дамуының ең жоғ арғ ы сатысы жә не жер бетіндегі тіршіліктің негізі. Организмнің тірек, бұ лшық ет, жамылғ ы тканьдері ақ уыздардан қ ұ ралғ ан. Олар организмде ә ртү рлі қ ызмет атқ арады, химиялық реакцияларды жү ргізеді, дене мү шелерінің қ ызметтерін ө зара ү йлестіреді, аурулармен кү реседі, т. б. Ақ уыздар азық тың қ ұ рамына кіреді. Адам тә улігіне, шамамен, — 100 г ақ уыз қ абылдауы керек. Азық пен тү скен ақ уыз ә уелі асқ азанда, сосын ішектегі ферменттердің ә серінен гидролизденіп, аминқ ышқ ылдарына дейін ыдырайды.
Қ ұ рамы мен қ ұ рылысы кү рделі болғ андық тан, ақ уыздардың қ асиеттері де алуан тү рлі. Олардың қ ұ рамында ә ртү рлі химиялық реакцияларғ а тү сетін функционалдық топтары бар.
Белок мө лшері аминқ ышқ ылдарының санына қ арай жә не молекулалық массасына қ арай дальтон бірлігі негізінде ө лшенеді. Орташа шамамен ашытқ ы саң ырауқ ұ лақ тарының қ ұ рамы - 466 аминқ ышқ ылынан тұ рса, массасы -53кДа, ең ү лкен белок – титин. Ол бұ лшық ет сарокмерлерінде кездесетін белок. Молекулалық массасы -3000-3700 кДа ө згеріп отырады, ұ зындығ ы 38 138 амин қ ышқ ылдарынан тұ рады.
1. Белоктар амфотерлік қ асиетке ие, яғ ни олар амин қ ышқ ылының радикалдары бойынша анық талатын негіздік те қ ышқ лыдық та қ асиетке ие.
2. Сонымен бірге ерігіш жә не ерімейтін белоктар болады, олар механикалық қ ызмет атқ арады (фиброин, кератин, коллаген).
3. Ерекше химиялық активті (ферменттер) жә не активті емес белоктар болады.
4. Қ оршағ ан ортаның ә ртү рлі факторларына тө зімді жә не тө зімсіз белоктар болады (температураның ө згеруі, ортаның тқ здық қ ұ рамы, рН, радиация). Аталғ ан факторлар белок молекуласының структуралық қ ұ рылымын бұ зады. Денатурация.
1. Ақ уыздар — екідайлы электролиттер. Ортаның белгілі бір рН мә нінде олардың молекулаларындағ ы оң жә не теріс зарядтар бірдей (изоэлектрлік нү кте деп аталады) болады. Бұ л — ақ уыздардың маң ызды қ асиеттерінің бірі. Бұ л нү ктеде ақ уыздар электрбейтарап болып, суда еруі азаяды. Ақ уыздардың осы қ асиеті технологияда ақ уызды ө німдер алуғ а қ олданылады.
2. Ақ уыздардың гидролизі. Сілті немесе қ ышқ ыл ерітінділерін қ осып қ ыздырғ анда, ақ уыздар гидролизденіп, аминқ ышқ ылдарын тү зеді: 
3. Ақ уыздардың тү сті реакциялары. Белоктарды сапалық анық тау ү шін тү сті реакциялар қ олданылады.
· а) Ксантопротеинреакциясымен (грек. ксанты — сары) қ ұ рамында бензол ядросы бар ақ уыздар концентрлі азот қ ышқ ылымен сары тү с береді.
· ә ) Биурет реакциясы. Мыс (II) гидроксидінің сілтідегі ерітіндісімен ақ уыздарғ а ә сер еткенде, ашық кү лгін тү с пайда болады. Бұ л реакция ақ уызтардың қ ұ рамындағ ы пептидтік байланыстарды анық тайды.
· б) Қ ұ рамында кү кірті бар ақ уыздарғ а қ орғ асын ацетатын жә не сілті қ осып қ ыздырғ анда, қ орғ асын сульфидінің қ ара тұ нбасы тү зіледі. [1]
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|