| Italics indicates desiccated thyroid extract.
Reprinted with adaptations with permission from Taylor & Francis Ltd. from Jonklaas (104).
| Курсивом обозначен высушенный экстракт щитовидной железы.
Перепечатано с изменениями с разрешения Taylor & Francis Ltd. из Йонклааса (104).
|
| D2 polymorphisms, and the effects of LT4 monotherapy versus combination therapy
The impact of D2 polymorphisms in mice
Since the first description of the Thr92Ala polymorphism of the type 2 deiodinase gene (DIO2) (Thr92Ala-DIO2) in humans as a gene variant associated with increased body mass index and insulin resistance (18), Thr92Ala-DIO2 has also been found to be important for TH action. Studies in cells show profound effects of polymorphisms in the DIO2 on the action of TH. Transfection studies in cultures of mouse pituitary cells from DIO2-null mice resulted in less TSH suppression in cells expressing the DIO2 Ala/Ala homozygote, as compared with cells expressing wild type Thr92-DIO2 (19). Furthermore, HEK-293 cells stably expressing Thr92Ala-DIO2 produced ∼20% less T3 over time than cells expressing Thr92-DIO2 (20).
Studies comparing human and rodents should bear in mind interspecies differences. On one hand, the rodent thyroid produces relatively more T3 than the human thyroid, theoretically placing LT4-treated hypothyroid mice at a higher risk of developing low serum T3 levels. On the other hand, the D2 pathway has a much greater role in humans than in rodents, placing humans at a higher risk of exhibiting low tissue and serum T3 levels due to a D2 defect. Nonetheless, despite these differences in TH economy, it is notable that in both rodents and humans, treatment with LT4 monotherapy normalizes serum TSH while serum T3 is either in the lower part of the normal range or below the normal range.
Although intact mice homozygous for the Thr92Ala polymorphism had normal serum T3 levels, they did not engage in as much physical activity, slept more, and required more time to memorize objects than their wild type counterparts (21). Studies on T3-responsive genes within different brain areas indicate that T3 actions in the brains of Thr92Ala-DIO2 mice are reduced, perhaps pointing to localized “hypothyroidism.” The previously mentioned alterations in activity, sleep, and cognition were intensified when the homozygous mice were rendered hypothyroid by adding methimazole to their drinking water. Moreover, these deficits were better redressed in these hypothyroid mice when they received treatment with combination therapy as compared with treatment using monotherapy with LT4 (21). These studies shed light on the reduced catalytic activity of the Thr92Ala-D2 enzyme and suggest that TH action in tissues that rely on D2-generated T3 (e.g., brain) is at risk during treatment with LT4. This conclusion is applicable to both small rodents and humans. Thus, while advancements have been made toward understanding the impact of the Thr92Ala-DIO2 in the rodent model, further investigations of human carriers of this polymorphism are needed before major conclusions and recommendations could be formulated for hypothyroid patients.
| Полиморфизм D2 и эффекты монотерапии LT4 по сравнению с комбинированной терапией
Влияние полиморфизма D2 на мышей
С момента первого описания полиморфизма Thr92Ala гена дейодиназы типа 2 (DIO2) (Thr92Ala-DIO2) у людей в качестве варианта гена, связанного с повышенным индексом массы тела и инсулинорезистентностью (18), было обнаружено, что Thr92Ala-DIO2 также является важно для действия TH. Исследования на клетках показывают глубокое влияние полиморфизма DIO2 на действие TH. Исследования трансфекции в культурах клеток гипофиза мышей от DIO2-нулевых мышей привели к меньшей супрессии ТТГ в клетках, экспрессирующих гомозиготу DIO2 Ala / Ala, по сравнению с клетками, экспрессирующими Thr92-DIO2 дикого типа (19). Кроме того, клетки HEK-293, стабильно экспрессирующие Thr92Ala-DIO2, продуцировали на ~ 20% меньше T3 с течением времени, чем клетки, экспрессирующие Thr92-DIO2 (20).
В исследованиях, сравнивающих человека и грызунов, следует учитывать межвидовые различия. С одной стороны, щитовидная железа грызунов производит относительно больше Т3, чем щитовидная железа человека, теоретически подвергая мышей с гипотиреозом, получавших лечение LT4, более высокий риск развития низких уровней Т3 в сыворотке. С другой стороны, путь D2 играет гораздо большую роль у людей, чем у грызунов, подвергая людей более высокому риску проявления низких уровней Т3 в тканях и сыворотке крови из-за дефекта D2. Тем не менее, несмотря на эти различия в экономике TH, примечательно, что как у грызунов, так и у людей лечение монотерапией LT4 нормализует сывороточный ТТГ, в то время как сывороточный T3 находится либо в нижней части нормального диапазона, либо ниже нормального диапазона.
Хотя интактные мыши, гомозиготные по полиморфизму Thr92Ala, имели нормальные уровни Т3 в сыворотке, они не участвовали в такой большой физической активности, больше спали и требовали больше времени для запоминания объектов, чем их коллеги дикого типа (21). Исследования генов, реагирующих на Т3, в различных областях мозга показывают, что действия Т3 в мозге мышей Thr92Ala-DIO2 снижены, что, возможно, указывает на локализованный «гипотиреоз». Ранее упомянутые изменения активности, сна и познания усилились, когда гомозиготным мышам сделали гипотиреоз путем добавления метимазола в питьевую воду. Более того, эти дефициты были лучше восполнены у этих мышей с гипотиреозом, когда они получали лечение комбинированной терапией, по сравнению с лечением с использованием монотерапии LT4 (21). Эти исследования проливают свет на сниженную каталитическую активность фермента Thr92Ala-D2 и предполагают, что действие TH в тканях, которые зависят от T3, генерируемого D2 (например, в головном мозге), подвергается риску во время лечения LT4. Этот вывод применим как к мелким грызунам, так и к человеку. Таким образом, несмотря на то, что были достигнуты успехи в понимании влияния Thr92Ala-DIO2 на модели грызунов, необходимы дальнейшие исследования носителей этого полиморфизма на людях, прежде чем можно будет сформулировать основные выводы и рекомендации для пациентов с гипотиреозом.
|
| Preliminary data regarding D2 polymorphism in humans
Human genetic association studies of single nucleotide polymorphisms (SNPs) explain only a limited proportion of phenotypic variation among individuals. This could reflect interference from structural and epigenetic variants, alleles with additive effects, or synergistic interactions. Therefore, not surprisingly, data obtained in different populations across the world regarding the significance of the Thr92Ala-DIO2 polymorphism with respect to the treatment of hypothyroidism in humans are preliminary and conflicting. A post hoc analysis in the United Kingdom showed that although this polymorphism had no impact on serum TH levels, it did predict the response to the therapy chosen for hypothyroidism (22). Those that were homozygous for the polymorphism had less psychological well-being (as measured by the General Health Questionnaire [GHQ] 12) while taking LT4, and more improvement when combination therapy was used, compared with participants carrying the wild type allele. Using stored samples from one of the combination therapy trials from 2009 (23), a 2017 analysis showed that patients with either the monocarboxylate transporter (MCT)10 polymorphism or both the MCT10 and Thr92Ala polymorphism preferred combination therapy (p-values 0.018 and 0.009, respectively) (24). However, a more recent study in the Netherlands did not find any impact of Th92Ala-DIO2 genotype on the response to LT4 monotherapy in terms of health-related QoL or cognitive function or an effect in the general population (25). Notably, an Italian study with a relatively small number of participants revealed that LT4-treated thyroidectomized carriers of at least one Thr92Ala-DIO2 allele exhibited lower serum T3 levels, despite a normal serum TSH (19). If replicated, these data could indicate that alterations in DIO2 may, in fact, affect circulating T3 levels in those who are athyreotic and treated with LT4.
| Предварительные данные о полиморфизме D2 у человека
Исследования генетической ассоциации человека с однонуклеотидными полиморфизмами (SNP) объясняют только ограниченную часть фенотипических вариаций среди людей. Это может отражать вмешательство структурных и эпигенетических вариантов, аллелей с аддитивными эффектами или синергетических взаимодействий. Поэтому неудивительно, что данные, полученные в разных популяциях по всему миру, относительно значения полиморфизма Thr92Ala-DIO2 в отношении лечения гипотиреоза у людей являются предварительными и противоречивыми. Апостериорный анализ, проведенный в Соединенном Королевстве, показал, что, хотя этот полиморфизм не влиял на уровни ТГ в сыворотке, он действительно предсказывал ответ на терапию, выбранную для лечения гипотиреоза (22). Те, которые были гомозиготными по полиморфизму, имели меньшее психологическое благополучие (по данным опросника общего состояния здоровья [GHQ] 12) при приеме LT4 и большее улучшение при использовании комбинированной терапии по сравнению с участниками, несущими аллель дикого типа. Используя сохраненные образцы из одного из испытаний комбинированной терапии от 2009 г. (23), анализ 2017 г. показал, что пациенты с полиморфизмом транспортера монокарбоксилата (MCT) 10 или одновременно с полиморфизмом MCT10 и Thr92Ala предпочитают комбинированную терапию (значения p 0,018 и 0,009, соответственно) (24). Однако более недавнее исследование в Нидерландах не обнаружило какого-либо влияния генотипа Th92Ala-DIO2 на ответ на монотерапию LT4 с точки зрения качества жизни, связанного со здоровьем, когнитивной функции или эффекта в общей популяции (25). Примечательно, что итальянское исследование с относительно небольшим количеством участников показало, что подвергнутые лечению LT4 тиреоидэктомированные носители по крайней мере одного аллеля Thr92Ala-DIO2 демонстрируют более низкие уровни Т3 в сыворотке, несмотря на нормальный уровень ТТГ в сыворотке (19). При воспроизведении эти данные могут указывать на то, что изменения в DIO2 могут фактически повлиять на уровни циркулирующего T3 у тех, кто страдает атиреозом и лечится LT4.
|
Summary statements
| Summary statements
| | •In vitro, increasing T4 levels inhibits D2 activity except in cell lines derived from the pituitary, suggesting that a high fT4/fT3 ratio may lead to a “normal” TSH while reducing T3 generation in peripheral tissues.
| | In • hypothalamic extracts, D2 inactivation is a much less efficient process as compared with other tissues. This would reinforce a predominant role of T4 and localized T3 production in the hypothalamus–pituitary unit to mediate the TSH feedback mechanism.
| | Hypothyroid • rats treated with LT4 to restore serum TSH have lower T3 levels in the serum and in some tissues than control rats, but T3 levels are restored with combination therapy that adds LT3.
| | Tissue • markers of TH action (serum cholesterol, T3-responsive genes) in LT4-treated thyroidectomized rats with normal serum TSH indicate residual hypothyroidism; no differences compared with control rats were observed in the thyroidectomized rats treated with LT4/LT3.
| | Mice • homozygous for the Thr92Ala-DIO2 polymorphism have a hypothyroid-like pattern of T3-responsive genes in certain areas of the central nervous system (CNS) when compared with wild type mice.
| | Mice • homozygous for the Thr92Ala-DIO2 polymorphism engage in less physical activity, sleep more, and have short-term memory problems when compared with wild type mice.
| | Physical • activity, sleep patterns, and short-term memory in hypothyroid Thr92Ala-DIO2 homozygous mice improve more with LT4/LT3 than with LT4 therapy alone.
| | The • impact of the Thr92Ala-DIO2 polymorphism on the clinical treatment benefit of combination therapy for hypothyroidism in humans is currently unclear.
| Summary statements
Summary statements
• In vitro, increasing T4 levels inhibits D2 activity except in cell lines derived from the pituitary, suggesting that a high fT4/fT3 ratio may lead to a “normal” TSH while reducing T3 generation in peripheral tissues.
• In hypothalamic extracts, D2 inactivation is a much less efficient process as compared with other tissues. This would reinforce a predominant role of T4 and localized T3 production in the hypothalamus–pituitary unit to mediate the TSH feedback mechanism.
• Hypothyroid rats treated with LT4 to restore serum TSH have lower T3 levels in the serum and in some tissues than control rats, but T3 levels are restored with combination therapy that adds LT3.
• Tissue markers of TH action (serum cholesterol, T3-responsive genes) in LT4-treated thyroidectomized rats with normal serum TSH indicate residual hypothyroidism; no differences compared with control rats were observed in the thyroidectomized rats treated with LT4/LT3.
• Mice homozygous for the Thr92Ala-DIO2 polymorphism have a hypothyroid-like pattern of T3-responsive genes in certain areas of the central nervous system (CNS) when compared with wild type mice.
• Mice homozygous for the Thr92Ala-DIO2 polymorphism engage in less physical activity, sleep more, and have short-term memory problems when compared with wild type mice.
• Physical activity, sleep patterns, and short-term memory in hypothyroid Thr92Ala-DIO2 homozygous mice improve more with LT4/LT3 than with LT4 therapy alone.
• The impact of the Thr92Ala-DIO2 polymorphism on the clinical treatment benefit of combination therapy for hypothyroidism in humans is currently unclear.
| Сводные заявления
Сводные заявления
• In vitro повышение уровня Т4 подавляет активность D2, за исключением клеточных линий, происходящих из гипофиза, что позволяет предположить, что высокое соотношение fT4 / fT3 может привести к «нормальному» ТТГ при одновременном снижении генерации T3 в периферических тканях.
• В экстрактах гипоталамуса инактивация D2 - гораздо менее эффективный процесс по сравнению с другими тканями. Это может усилить преобладающую роль Т4 и локализованного производства Т3 в гипоталамус-гипофизарном блоке, чтобы опосредовать механизм обратной связи ТТГ.
• Гипотироидные крысы, получавшие LT4 для восстановления сывороточного TSH, имеют более низкие уровни T3 в сыворотке и в некоторых тканях, чем контрольные крысы, но уровни T3 восстанавливаются с помощью комбинированной терапии, которая добавляет LT3.
• Тканевые маркеры действия TH (холестерин сыворотки, T3-чувствительные гены) у крыс, подвергнутых тиреоидэктомии, получавших LT4, с нормальным уровнем ТТГ в сыворотке указывают на остаточный гипотиреоз; у тиреоидэктомированных крыс, получавших LT4 / LT3, различий по сравнению с контрольными крысами не наблюдалось.
• Мыши, гомозиготные по полиморфизму Thr92Ala-DIO2, имеют гипотиреоидный паттерн T3-чувствительных генов в определенных областях центральной нервной системы (ЦНС) по сравнению с мышами дикого типа.
• Мыши, гомозиготные по полиморфизму Thr92Ala-DIO2, менее активны, больше спят и имеют проблемы с кратковременной памятью по сравнению с мышами дикого типа.
• Физическая активность, режим сна и кратковременная память у мышей с гипотиреозом, гомозиготными по Thr92Ala-DIO2, улучшаются больше при использовании LT4 / LT3, чем при терапии только LT4.
• Влияние полиморфизма Thr92Ala-DIO2 на клинический эффект комбинированной терапии гипотиреоза у людей в настоящее время неясно.
|
| Topic 2: Noncanonical actions of TH (presenter at live conference: L.C.M., topic summarizer: C.M.D.)
Different pathways of TH action
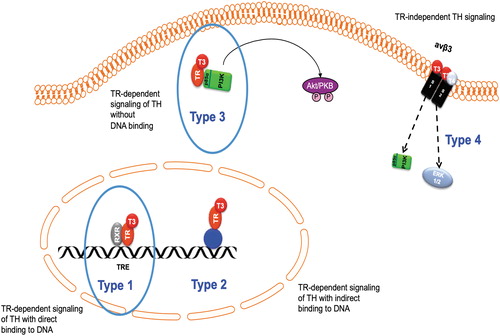
TH, in the form of T3, has classically been considered to act by binding to cytosolic TH receptors (TR) (TRα1, TRβ1, and TRβ2) that bind to TH response elements on the DNA and regulate expression of TH target genes (canonical TH/TR action) (26,27). However, there is now evidence of additional noncanonical mechanisms of TH action, and four types of TH signaling have recently been defined: Type 1 (canonical) = TR-dependent signaling of TH with direct binding to DNA; Type 2 = TR-dependent signaling of TH with indirect binding to DNA; Type 3 = TR-dependent signaling of TH without DNA binding, for example, through PI3K; Type 4 = TR-independent TH signaling, for example, through integrin αvβ3 (Fig. 2) (28).
| Тема 2: Неканонические действия TH (ведущий на живой конференции: L.C.M., составитель темы: C.M.D.)
Различные пути действия TH
Классически считалось, что TH в форме T3 действует путем связывания с цитозольными рецепторами TH (TR) (TRα1, TRβ1 и TRβ2), которые связываются с элементами ответа TH на ДНК и регулируют экспрессию генов-мишеней TH (канонический TH / TR действие) (26,27). Однако теперь есть доказательства дополнительных неканонических механизмов действия TH, и недавно были определены четыре типа передачи сигналов TH: Тип 1 (канонический) = TR-зависимая передача сигналов TH с прямым связыванием с ДНК; Тип 2 = TR-зависимая передача сигналов TH с непрямым связыванием с ДНК; Тип 3 = TR-зависимая передача сигналов TH без связывания ДНК, например, через PI3K; Тип 4 = TR-независимая передача сигналов TH, например, через интегрин αvβ3 (Fig. 2) (28).
|