
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Table 2. Characteristic of Clinical Trials of Synthetic Combination Therapy 1 страница
Стр 1 из 7Следующая ⇒
| Evidence-Based Use of Levothyroxine/Liothyronine Combinations in Treating Hypothyroidism: A Consensus Document[1],[2] Jacqueline Jonklaas , Antonio C. Bianco , Anne R. Cappola , Francesco S. Celi , Eric Fliers , Heike Heuer , Elizabeth A. McAninch , Lars C. Moeller , Birte Nygaard , Anna M. Sawka , Torquil Watt , and Colin M. Dayan Published Online:12 Feb 2021https://doi.org/10.1089/thy.2020.0720 | Доказательное использование комбинаций левотироксина и лиотиронина в лечении гипотиреоза: согласованный документ | ||
| Abstract Background: Fourteen clinical trials have not shown a consistent benefit of combination therapy with levothyroxine (LT4) and liothyronine (LT3). Despite the publication of these trials, combination therapy is widely used and patients reporting benefit continue to generate patient and physician interest in this area. Recent scientific developments may provide insight into this inconsistency and guide future studies. Methods: The American Thyroid Association (ATA), British Thyroid Association (BTA), and European Thyroid Association (ETA) held a joint conference on November 3, 2019 (live-streamed between Chicago and London) to review new basic science and clinical evidence regarding combination therapy with presentations and input from 12 content experts. After the presentations, the material was synthesized and used to develop Summary Statements of the current state of knowledge. After review and revision of the material and Summary Statements, there was agreement that there was equipoise for a new clinical trial of combination therapy. Consensus Statements encapsulating the implications of the material discussed with respect to the design of future clinical trials of LT4/LT3 combination therapy were generated. Authors voted upon the Consensus Statements. Iterative changes were made in several rounds of voting and after comments from ATA/BTA/ETA members. Results: Of 34 Consensus Statements available for voting, 28 received at least 75% agreement, with 13 receiving 100% agreement. Those with 100% agreement included studies being powered to study the effect of deiodinase and thyroid hormone transporter polymorphisms on study outcomes, inclusion of patients dissatisfied with their current therapy and requiring at least 1.2 μg/kg of LT4 daily, use of twice daily LT3 or preferably a slow-release preparation if available, use of patient-reported outcomes as a primary outcome (measured by a tool with both relevant content validity and responsiveness) and patient preference as a secondary outcome, and utilization of a randomized placebo-controlled adequately powered double-blinded parallel design. The remaining statements are presented as potential additional considerations. Discussion: This article summarizes the areas discussed and presents Consensus Statements to guide development of future clinical trials of LT4/LT3 combination therapy. The results of such redesigned trials are expected to be of benefit to patients and of value to inform future thyroid hormone replacement clinical practice guidelines treatment recommendations. | Абстрактный Актуальность темы: четырнадцать клинических испытаний не продемонстрировали стойкого преимущества комбинированной терапии левотироксином (LT4) и лиотиронином (LT3). Несмотря на публикацию этих исследований, комбинированная терапия широко используется, и пациенты, сообщающие о ее преимуществах, продолжают вызывать интерес у пациентов и врачей в этой области. Недавние научные разработки могут пролить свет на это несоответствие и послужить ориентиром для будущих исследований. Методы: Американская тироидная ассоциация (ATA), Британская тироидная ассоциация (BTA) и Европейская тироидная ассоциация (ETA) 3 ноября 2019 г. провели совместную конференцию (прямая трансляция между Чикаго и Лондоном) для обзора новых фундаментальных научных данных и клинических данных. относительно комбинированной терапии с презентациями и мнениями 12 экспертов по содержанию. После презентаций материал был синтезирован и использован для разработки Резюме текущего состояния знаний. После обзора и пересмотра материалов и сводных заявлений было достигнуто согласие о том, что есть основания для нового клинического испытания комбинированной терапии. Были сформированы консенсусные заявления, в которых излагается значение обсуждаемого материала в отношении дизайна будущих клинических испытаний комбинированной терапии LT4 / LT3. Авторы проголосовали за согласованные утверждения. Итерационные изменения были внесены в несколько туров голосования и после комментариев членов ATA / BTA / ETA. Результаты: из 34 утверждений о консенсусе, доступных для голосования, 28 получили согласие не менее 75%, а 13 - 100%. Те, у кого было 100% согласие, включали исследования, направленные на изучение влияния полиморфизмов дейодиназы и транспортеров тироидных гормонов на результаты исследований, включение пациентов, неудовлетворенных их текущей терапией и требующих не менее 1,2 мкг / кг LT4 в день, использование LT3 два раза в день или предпочтительно препарат с медленным высвобождением, если таковой имеется, использование результатов, сообщаемых пациентами, в качестве первичного результата (измеряемого инструментом, имеющим как релевантную достоверность содержания, так и отзывчивость) и предпочтение пациента в качестве вторичного результата, а также использование рандомизированного плацебо-контролируемого адекватно мощного двойная слепая параллельная конструкция. Остальные утверждения представлены как возможные дополнительные соображения. Обсуждение: в этой статье суммируются обсуждаемые области и представлены консенсусные утверждения, которые помогут разработать будущие клинические испытания комбинированной терапии LT4 / LT3. Ожидается, что результаты таких измененных исследований принесут пользу пациентам и будут полезны для информирования будущих клинических рекомендаций по заместительной гормональной терапии. | ||
| Introduction Endocrinologists are frequently asked to consult on adult patients with hypothyroidism taking levothyroxine (LT4) who are dissatisfied with their therapy. Once other nonthyroid-related causes of these symptoms have been fully excluded, the patient and their physician may wish to explore alternative therapies for optimization of health and well-being. However, the use of combination therapy with both LT4 and liothyronine (LT3) remains highly controversial with conflicting results from published clinical trials (1), with two studies showing benefit in most measures and two showing benefit in some measures. Recent scientific studies have provided new mechanistic insight into issues such as the complex relationship between serum and tissue thyroid hormone (TH) levels (1), providing a rationale for reconsideration of the design of future LT4/LT3 combination therapy clinical trials by incorporating features that might increase the likelihood of showing efficacy. Thus, our aim in this consensus document was that consideration of mechanism might provide a path toward better designed trials, also focusing on clinically relevant outcomes, including patient-centered outcomes. The American Thyroid Association (ATA), British Thyroid Association (BTA), and European Thyroid Association (ETA) held a joint conference on November 3, 2019 (live streamed between Chicago and London) to review this new evidence with presentations and input from 12 leaders in the field followed by local workshops in Chicago and London. The 12 individuals were selected based on their content expertise in basic, translational, and clinical aspects of TH therapy for hypothyroidism. To incorporate input from as many relevant stakeholders as possible, the presenters and moderators included endocrinologists, an epidemiologist, a psychologist, basic scientists, translational scientists, and two patient representatives. This article summarizes the areas discussed and presents a position statement to guide future clinical trials of LT4/LT3 combination therapy. | Вступление Эндокринологов часто просят проконсультироваться со взрослыми пациентами с гипотиреозом, принимающими левотироксин (LT4), которые недовольны своей терапией. После того, как другие причины этих симптомов, не связанные со щитовидной железой, будут полностью исключены, пациент и его врач могут пожелать изучить альтернативные методы лечения для оптимизации здоровья и благополучия. Однако использование комбинированной терапии как с LT4, так и с лиотиронином (LT3) остается весьма спорным из-за противоречивых результатов опубликованных клинических испытаний (1): два исследования показали пользу по большинству показателей, а два - по некоторым параметрам. Недавние научные исследования позволили по-новому взглянуть на такие проблемы, как сложная взаимосвязь между сывороточными и тканевыми уровнями гормона щитовидной железы (TH) (1), что послужило основанием для пересмотра дизайна будущих клинических испытаний комбинированной терапии LT4 / LT3 путем включения особенностей, которые может увеличить вероятность проявления эффективности. Таким образом, наша цель в этом согласованном документе состояла в том, чтобы рассмотрение механизма могло обеспечить путь к более продуманным испытаниям, также сосредоточив внимание на клинически значимых исходах, включая исходы, ориентированные на пациента. Американская тироидная ассоциация (ATA), Британская тироидная ассоциация (BTA) и Европейская тироидная ассоциация (ETA) 3 ноября 2019 г. провели совместную конференцию (прямая трансляция между Чикаго и Лондоном), чтобы рассмотреть эти новые доказательства с презентациями и мнениями 12 участников. лидеры в этой области, за которыми последовали местные семинары в Чикаго и Лондоне. 12 человек были отобраны на основе их опыта в базовых, трансляционных и клинических аспектах терапии гипотиреоза с помощью ТГ. Чтобы включить вклад как можно большего числа заинтересованных сторон, в число докладчиков и модераторов вошли эндокринологи, эпидемиолог, психолог, фундаментальные ученые, ученые-переводчики и два представителя пациентов. В этой статье кратко излагаются обсуждаемые области и излагается позиция, которой будут руководствоваться будущие клинические испытания комбинированной терапии LT4 / LT3. | ||
| Methods Following the presentations, the associated question-and-answer periods, and the local workshops, the material available was broken down into nine topics. Two authors (J.J. and C.M.D.) then each summarized the content and discussion for half of these topic areas, and then combined the material. This synthesis of material also included formulating Summary Statements to encapsulate the material, and generation of Consensus Statements to capture the direction suggested by the material for the design of future clinical trials of LT4/LT3 combination therapy. The resulting document was then reviewed by the remaining 10 authors. After the conference and during the review process, 2 additional topics emerged based on authors feedback (Topics 4 and 9), which had been covered, in part, within the initial topics, thus bringing the total number of topics to 11. Topic 11 did not relate to future clinical trials and no Consensus Statements were generated for this topic. For the Consensus Statements, the authors were provided with these in tabular form and were asked to vote yes or no as to whether they agreed with the statement or not. They were also asked to provide comments regarding each of the statements as desired. The consensus document, Summary Statements, and Consensus Statements were then modified and returned to the writing group for further adjustments and suggestions. A second round of voting was requested for the modified Consensus Statements. A third round of voting was obtained for six Consensus Statements that had undergone modifications after the second review. Further discussion and a fourth round of voting were not pursued to try and obtain a greater degree of consensus. After the third set of modifications, final versions of the article and Consensus Statements were produced and provided to the group for ultimate approval. Input from the two patient representatives involved in the conference and input from patients attending the conference were considered in the topic discussions and summaries, but these stakeholders were not formally members of the writing group. Conflicts of interest were collected for each of the 12 participants before the presentations on November 3, 2019. Some declared conflicts were deemed to not be relevant to the material being discussed. Five authors had relevant conflicts and their input was not solicited for the applicable material within the document and Summary Statements, and their vote was not ascertained for the Consensus Statement drawn from this topic material (such votes were marked as abstentions). The exclusions were as follows: A.C.B.: Topic 6: Target T3 and TSH levels and Slow-Release T3 (section 6.3) and Topic 9: Trial Design Considerations (section 9.4 on therapies to be studied), F.S.C.: Topic 9: Trial Design Considerations (section 9.4 on therapies to be studied), T.W.: Topic 7: Psychological and Quality of Life Measures (section 7.1, 7.2, 7.3) and Topic 9: Trial Design Considerations (section 9.4 on therapies to be studied), and Topic 10: Incorporation of Patient Experiences (section 10.3). E.F.: Topic 9: Trial Design Considerations (all sections), B.N.: Topic 9: Trial Design Considerations (all sections). Eighteen abstentions for the 408 votes on all 34 Consensus Statements were recorded in total. Approval for the joint conference was provided in advance by the relevant committees and leadership of the ATA, BTA, and ETA according to society policies. The concept for this Consensus Document was approved by the ATA Board of Directors, and the ATA Guidelines and Statements Committee, who also reviewed and approved the conflict of interest management plan. The near-final article was approved by the relevant committees of the ATA, BTA, and ETA and also made available for comments from the membership of all three societies for a comment period of 30 days. Although the relevant literature was extensively reviewed, no formal systematic review or grading of evidence was undertaken. The consensus statements were compiled based on expert opinion and are not graded recommendations. | Методы После презентаций, соответствующих периодов вопросов и ответов и местных семинаров доступный материал был разбит на девять тем. Затем два автора (J.J. и C.M.D.) суммировали содержание и обсуждение половины этих тематических областей, а затем объединили материалы. Этот синтез материала также включал формулировку сводных заявлений для инкапсуляции материала и генерацию утверждений консенсуса для отражения направления, предлагаемого материалом для дизайна будущих клинических испытаний комбинированной терапии LT4 / LT3. Полученный документ был затем рассмотрен оставшимися 10 авторами. После конференции и во время процесса обзора на основе отзывов авторов возникли 2 дополнительные темы (темы 4 и 9), которые были частично рассмотрены в рамках исходных тем, в результате чего общее количество тем достигло 11. Тема 11 была затронута. не относятся к будущим клиническим испытаниям, и по этой теме не было составлено никаких согласованных заявлений. Что касается утверждений о консенсусе, авторам предоставили их в табличной форме и попросили проголосовать за или против, согласны ли они с утверждением или нет. Их также попросили предоставить комментарии по каждому из заявлений по желанию. Документ о консенсусе, Сводные заявления и Консенсусные заявления были затем изменены и возвращены группе написания для дальнейших корректировок и предложений. Второй раунд голосования был запрошен для измененных заявлений о консенсусе. Третий раунд голосования был проведен для шести утверждений о консенсусе, которые претерпели изменения после второго обзора. Дальнейшее обсуждение и четвертый раунд голосования не проводились для достижения большей степени консенсуса. После третьего набора изменений были подготовлены окончательные версии статьи и Консенсуса, которые были представлены группе для окончательного утверждения. Вклад двух представителей пациентов, участвовавших в конференции, и вклад пациентов, присутствовавших на конференции, были учтены в обсуждениях темы и резюме, но эти заинтересованные стороны формально не входили в состав группы авторов. Конфликты интересов были собраны для каждого из 12 участников перед презентацией 3 ноября 2019 г. Некоторые заявленные конфликты были сочтены не имеющими отношения к обсуждаемому материалу. У пяти авторов возникли соответствующие конфликты, и их мнения не были запрошены для применимых материалов в документе и Сводных заявлениях, и их голос не был подтвержден за Заявление о консенсусе, составленное на основе этого тематического материала (такие голоса были отмечены как воздержавшиеся). Были исключены следующие исключения: ACB: Тема 6: Целевые уровни T3 и ТТГ и T3 с медленным высвобождением (раздел 6.3) и Тема 9: Соображения по дизайну исследования (раздел 9.4 о методах лечения, которые необходимо изучить), FSC: Тема 9: Соображения по дизайну исследования. (раздел 9.4 о методах лечения, которые необходимо изучить), TW: Тема 7: Психологические показатели и показатели качества жизни (разделы 7.1, 7.2, 7.3) и Тема 9: Соображения по дизайну исследования (раздел 9.4 о методах лечения, которые необходимо изучить), и Тема 10: Учет опыта пациентов (раздел 10.3). E.F .: Тема 9: Соображения по дизайну исследования (все разделы), B.N .: Тема 9: Соображения по дизайну исследования (все разделы). Всего было зарегистрировано 18 воздержавшихся при 408 голосах по всем 34 заявлениям о консенсусе. Утверждение совместной конференции было заранее предоставлено соответствующими комитетами и руководством ATA, BTA и ETA в соответствии с политикой общества. Концепция этого согласованного документа была одобрена Советом директоров ATA и Комитетом по рекомендациям и заявлениям ATA, которые также рассмотрели и одобрили план управления конфликтом интересов. Почти финальная статья была одобрена соответствующими комитетами ATA, BTA и ETA, а также предоставлена для комментариев членам всех трех обществ в течение 30 дней. Несмотря на то, что соответствующая литература была тщательно изучена, формального систематического обзора или классификации доказательств не проводилось. Заявления о консенсусе были составлены на основе мнений экспертов и не являются рекомендациями по оценке. | ||
Results: Topics Summaries, Summary Statements, and Consensus Statements
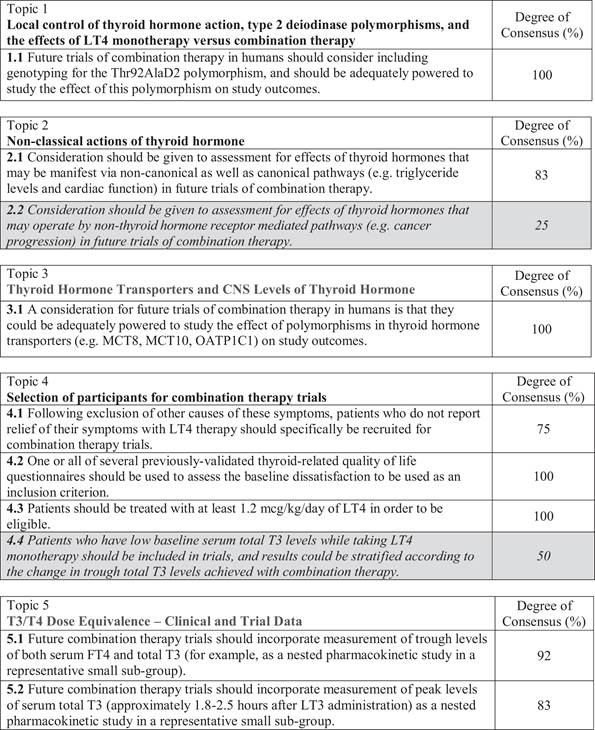
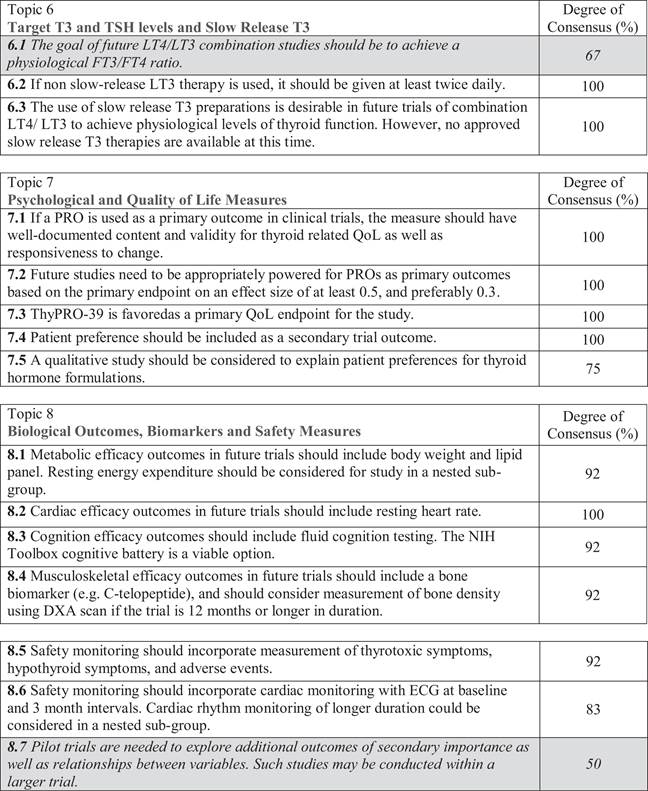
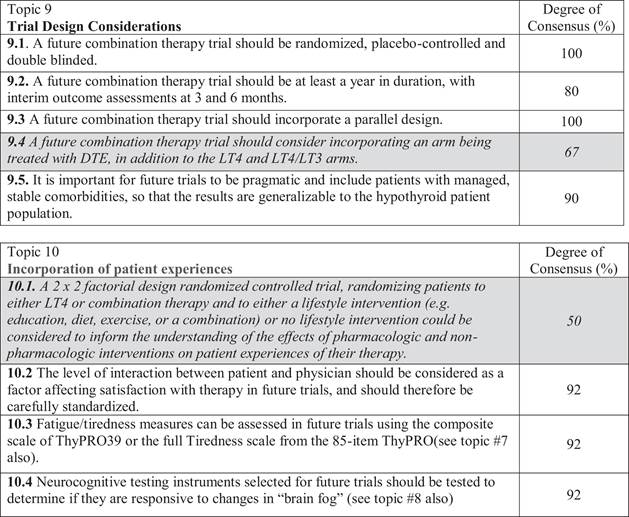
Consensus Statements encapsulating the implication of the material with respect to the design of future clinical trials were generated. After mutually agreed upon modifications, 34 Consensus Statements were available for voting. There were 28 Consensus Statements upon which there was consensus from at least 75% of the group (9 out of 12 individuals), with lesser degrees of consensus regarding the remaining 6 Consensus Statements. Thus, a consensus among at least 75% of authors was achieved for the majority of Consensus Statements. The Consensus Statements with at least 75% agreement are presented in this document as important considerations for the design of future clinical trials of combination therapy (Table 1). Out of those 28 statements with at least 75% agreement, there were 13 statements for which 100% consensus was achieved. The Consensus Statements with <75% agreement are in italics and could be considered if future studies provide additional rationale.
| Результаты: резюме тем, итоговые заявления и консенсусные заявления Были выработаны консенсусные заявления, в которых излагается значение материала для дизайна будущих клинических испытаний. После взаимно согласованных изменений на голосование были представлены 34 заявления о консенсусе. Было 28 утверждений о консенсусе, по которым было достигнуто согласие по крайней мере 75% группы (9 из 12 человек), с меньшей степенью согласия в отношении остальных 6 утверждений о консенсусе. Таким образом, консенсус среди как минимум 75% авторов был достигнут по большинству утверждений консенсуса. Консенсусные утверждения с согласием не менее 75% представлены в этом документе как важные соображения при планировании будущих клинических испытаний комбинированной терапии (Таблица 1). Из этих 28 утверждений, по которым согласие не менее 75%, было 13 утверждений, по которым был достигнут 100% консенсус. Заявления о консенсусе со степенью согласия <75% выделены курсивом и могут быть рассмотрены, если будущие исследования дадут дополнительное обоснование. Таблица 1. Консенсусные утверждения, организованные по темам 1–10 |
Таб 1
Таб 1 продолжение.
Окончание табл.1
| CNS, central nervous system; DXA, dual-energy X-ray absorptiometry; ECG, electrocardiogram; LT3, liothyronine; LT4, levothyroxine; PRO, patient-reported outcome; T3, triiodothyronine; T4, thyroxine; ThyPRO, Thyroid-specific Patient Reported Outcome; TSH, thyrotropin; QoL, quality of life. Topic 1: Local control of TH action, type 2 deiodinase polymorphisms, and the effects of LT4 monotherapy versus combination therapy (presenter at live conference: A.C.B., topic summarizer: J.J.) Local control of TH action: the consequence of monotherapy versus combination therapy The consequence of monotherapy versus combination therapy in rodent models The rationale for treatment with LT4 is that two deiodinase pathways, the type 1 deiodinase (D1) and the type 2 deiodinase (D2), convert thyroxine (T4) to triiodothyronine (T3), restoring the pool of T3 and clinical euthyroidism. Seminal studies from the Escobar-Morreale group first showed that LT4 therapy given to hypothyroid rats did not achieve normal serum T3 levels, nor did it result in normal T3 levels in all tissues sampled (2). They also showed restoration of normal tissue levels of THs with combination therapy with both LT4 and LT3 in rats (3). Later studies in LT4-treated rats discovered that the hypothalamus (4) and thyrotroph cell lines (5) convert T4 to T3 more efficiently than other tissues due to relatively less T4-induced inactivation of D2 through ubiquitination. Figure 1 illustrates the relative roles of the D1 and D2 pathways in the thyrotropin (TSH) feedback mechanism during treatment with LT4 (4–8). Thus in rodent models, TSH secretion is normalized before T3 levels are fully restored in the plasma and other tissues, resulting in low circulating T3 levels and “tissue hypothyroidism.” Use of combination therapy with both LT4 and LT3 in hypothyroid rats also normalized serum TSH but additionally allowed the T3 deficit in peripheral tissues to be redressed (4). In keeping with this, markers of euthyroidism, such as serum cholesterol levels, mitochondrial content, and enzymatic activity within liver and skeletal muscle, better approximated values in control rats when sustained delivery of both LT4 and LT3 was employed. Likewise, the pattern of T3-responsive genes in the brain was more similar to that of control rats when combination therapy was employed (4). | ЦНС, центральная нервная система; DXA, двухэнергетическая рентгеновская абсорбциометрия; ЭКГ, электрокардиограмма; LT3, лиотиронин; LT4, левотироксин; PRO, исход, сообщаемый пациентом; Т3, трийодтиронин; Т4, тироксин; ThyPRO, результат, сообщаемый пациентом, специфичным для щитовидной железы; ТТГ, тиреотропин; QoL, качество жизни. Тема 1: Местный контроль действия TH, полиморфизм дейодиназы 2 типа и эффекты монотерапии LT4 по сравнению с комбинированной терапией (докладчик на прямой конференции: A.C.B., обобщающий тему: J.J.) Местный контроль действия TH: последствия монотерапии по сравнению с комбинированной терапией Последствия монотерапии по сравнению с комбинированной терапией на моделях грызунов Основанием для лечения LT4 является то, что два пути дейодиназы, дейодиназа 1 типа (D1) и дейодиназа 2 типа (D2), превращают тироксин (T4) в трийодтиронин (T3), восстанавливая пул T3 и клинический эутиреоз. Семенные исследования группы Эскобара-Морреале сначала показали, что терапия LT4, проводимая гипотиреозным крысам, не приводила к нормальным уровням Т3 в сыворотке и не приводила к нормальным уровням Т3 во всех отобранных тканях (2). Они также показали восстановление нормальных уровней TH в тканях при комбинированной терапии LT4 и LT3 у крыс (3). Более поздние исследования на крысах, получавших LT4, обнаружили, что линии клеток гипоталамуса (4) и тиреотрофов (5) превращают T4 в T3 более эффективно, чем другие ткани, из-за относительно меньшей T4-индуцированной инактивации D2 посредством убиквитинирования. Рисунок 1 иллюстрирует относительную роль путей D1 и D2 в механизме обратной связи с тиреотропином (ТТГ) во время лечения LT4 (4-8). Таким образом, на моделях грызунов секреция ТТГ нормализуется до того, как уровни Т3 полностью восстановятся в плазме и других тканях, что приводит к низким уровням циркулирующего Т3 и «тканевому гипотиреозу». Использование комбинированной терапии как с LT4, так и с LT3 у крыс с гипотиреозом также нормализовало сывороточный ТТГ, но дополнительно позволило компенсировать дефицит Т3 в периферических тканях (4). В соответствии с этим маркеры эутиреоза, такие как уровни холестерина в сыворотке, содержание митохондрий и ферментативная активность в печени и скелетных мышцах, лучше приближались к значениям у контрольных крыс, когда использовалась длительная доставка как LT4, так и LT3. Аналогичным образом, паттерн T3-чувствительных генов в головном мозге был более похож на таковой у контрольных крыс при использовании комбинированной терапии (4). |
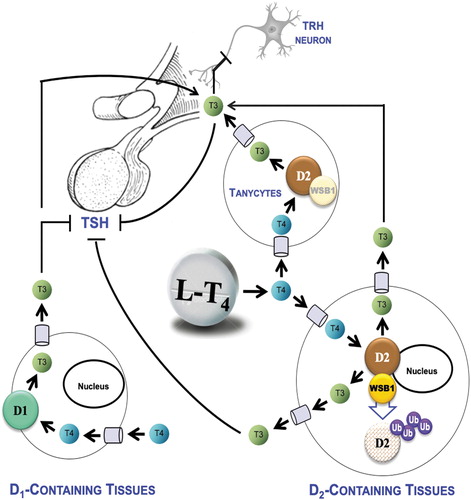
| FIG. 1. Relative roles of the D1 and D2 pathways in the TSH feedback mechanism during treatment with LT4. In LT4-treated thyroidectomized patients to achieve normal serum TSH levels, the D2 pathway contributes with ∼80% of the circulating T3 (6). Studies performed in rats revealed how plasma T4 is taken up by the hypothalamic tanycytes and the pituitary thyrotrophs, and locally converted to T3 through the D2 pathway (8). The net effect of the D2 activity in these two sites is a reduction in TSH secretion. As the goal of therapy with LT4 is to normalize serum TSH, a progressive increase in LT4 dose increases circulating T3 levels (predominantly through D2) and simultaneously reduce TSH secretion (predominantly through D2). Studies performed in rodents demonstrated that the D2 pathway is negatively regulated by T4, that is, D2 is ubiquitinated by WSB-1 and inactivated as it converts T4 to T3 (7). However, this process occurs at a much slower rate in the hypothalamus (4). Also in pituitary thyrotrophs, the loss of D2 activity caused by T4 is a much slower process (5). As a result, D2-mediated T3 production is a more efficient process in the hypothalamus/pituitary unit when compared with other D2-containing tissues. Thus, while increasing the LT4 replacement dose to treat hypothyroidism, normalization of serum TSH levels will occur before full normalization of serum T3 levels. The role played by D1 is secondary, mainly because its affinity for T4 is three orders of magnitude less than D2, and its expression is positively regulated by plasma T3. Thus, D1 activity was never fully normalized in LT4-treated hypothyroid rats, only when a combination of LT4 and LT3 was used was serum T3 restored (4). D1, type 1 deiodinase; D2, type 2 deiodinase; LT4, levothyroxine; T3, triiodothyronine; T4, thyroxine; TSH, thyrotropin; WSB-1, gene encoding the WD repeat and SOCS box-containing protein 1. | ФИГУРА. 1. Относительные роли путей D1 и D2 в механизме обратной связи ТТГ во время лечения LT4. У пациентов с тиреоидэктомией, леченных LT4, для достижения нормального уровня ТТГ в сыворотке, путь D2 составляет ~ 80% циркулирующего T3 (6). Исследования, проведенные на крысах, показали, как Т4 в плазме поглощается таницитами гипоталамуса и тиреотрофами гипофиза и локально превращается в Т3 по пути D2 (8). Чистым эффектом активности D2 в этих двух сайтах является снижение секреции ТТГ. Поскольку целью терапии LT4 является нормализация сывороточного ТТГ, постепенное увеличение дозы LT4 увеличивает уровни циркулирующего Т3 (преимущественно через D2) и одновременно снижает секрецию ТТГ (преимущественно через D2). Исследования, проведенные на грызунах, показали, что путь D2 негативно регулируется T4, то есть D2 убиквитинируется WSB-1 и инактивируется, поскольку он превращает T4 в T3 (7). Однако в гипоталамусе этот процесс происходит гораздо медленнее (4). Также у тиреотрофов гипофиза потеря активности D2, вызванная T4, является гораздо более медленным процессом (5). В результате D2-опосредованная продукция T3 является более эффективным процессом в гипоталамусе / гипофизе по сравнению с другими D2-содержащими тканями. Таким образом, при увеличении заместительной дозы LT4 для лечения гипотиреоза нормализация уровня ТТГ в сыворотке будет происходить до полной нормализации уровня Т3 в сыворотке. Роль, которую играет D1, вторична, главным образом потому, что его сродство к T4 на три порядка меньше, чем D2, и его экспрессия положительно регулируется плазменным T3. Таким образом, активность D1 никогда не была полностью нормализована у крыс с гипотиреозом, леченных LT4, только при использовании комбинации LT4 и LT3 сывороточный T3 восстановился (4). D1, дейодиназа 1 типа; D2, дейодиназа 2 типа; LT4, левотироксин; Т3, трийодтиронин; Т4, тироксин; ТТГ, тиреотропин; WSB-1, ген, кодирующий повтор WD и SOCS-бокс-содержащий белок 1. |
| The consequence of monotherapy versus combination therapy in humans It has been well established that there are two changes in TH levels that occur in patients being treated for hypothyroidism with LT4 monotherapy. These changes are an increase in T4 or free T4 (fT4) levels, an increase in fT4/T3 ratios, associated with a decline in T3 or free T3 (fT3) levels. Depending on the study, mean serum T3 or fT3 levels may be in the lower half of the normal range, and levels may even be below the normal range in up to 15% of athyreotic individuals (9–12). These differences all occur despite comparable serum TSH levels. In fact, in a cross-sectional study based on the U.S. National Health and Nutrition Examination Survey data base, serum T3 and fT3 levels were 10% lower in LT4-treated patients than in a control group matched for sex, age, ethnic background, and TSH levels (13). While LT4 therapy is very effective in normalizing serum TSH levels, it fails to restore euthyroidism in some tissues based on an array of metabolic parameters such as serum cholesterol levels and other biomarkers that remain abnormal in LT4-treated patients, despite a normal serum TSH (14–16). In the 14 trials of combination therapy for hypothyroidism in humans (Table 2), the TSH levels and T3 levels achieved during LT4/LT3 combination therapy were varied, with not all studies maintaining comparable TSH levels during combination therapy as were seen with LT4 monotherapy, or even achieving higher T3 levels during combination therapy (although this could be a consequence of the timing of blood sampling) (Supplementary Table S1) (9). As would be expected based on a lowering of the LT4 dose, fT4 levels were universally lower with combination therapy. However fT4/T3 ratios achieved in combination therapy do not replicate the native euthyroid state that is characterized by higher fT4/T3 ratios than those seen with combination therapy (10,17). Assessment of objective TH-dependent metabolic effects varied among these trials, which focused primarily on cognition, mood, and quality of life (QoL) (Supplementary Table S2). | Последствия монотерапии по сравнению с комбинированной терапией у людей Было хорошо установлено, что у пациентов, получающих лечение от гипотиреоза с помощью монотерапии LT4, происходят два изменения уровней TH. Эти изменения представляют собой повышение уровней Т4 или свободного Т4 (fT4), увеличение соотношения fT4 / T3, связанное со снижением уровней T3 или свободного T3 (fT3). В зависимости от исследования, средние уровни Т3 или fT3 в сыворотке могут быть в нижней половине нормального диапазона, а уровни могут даже быть ниже нормального диапазона у 15% лиц с атиреозом (9–12). Все эти различия возникают, несмотря на сопоставимые уровни ТТГ в сыворотке. Фактически, в перекрестном исследовании, основанном на базе данных Национального исследования здоровья и питания США, уровни Т3 и fT3 в сыворотке были на 10% ниже у пациентов, получавших LT4, чем в контрольной группе, соответствующей по полу, возрасту, этническому происхождению, и уровень ТТГ (13). Хотя терапия LT4 очень эффективна в нормализации уровня ТТГ в сыворотке, она не может восстановить эутиреоз в некоторых тканях на основании ряда метаболических параметров, таких как уровень холестерина в сыворотке и других биомаркеров, которые остаются ненормальными у пациентов, получавших LT4, несмотря на нормальный уровень ТТГ в сыворотке ( 14–16). В 14 испытаниях комбинированной терапии гипотиреоза у людей (таблица 2) уровни ТТГ и Т3, достигнутые во время комбинированной терапии LT4 / LT3, варьировались, при этом не во всех исследованиях поддерживались сопоставимые уровни ТТГ во время комбинированной терапии, как при монотерапии LT4. или даже достижение более высоких уровней Т3 во время комбинированной терапии (хотя это может быть следствием времени забора крови) (дополнительная таблица S1) (9). Как и следовало ожидать, основываясь на снижении дозы LT4, уровни fT4 были повсеместно ниже при комбинированной терапии. Однако соотношения fT4 / T3, достигаемые при комбинированной терапии, не воспроизводят нативное эутиреоидное состояние, которое характеризуется более высокими соотношениями fT4 / T3, чем при комбинированной терапии (10,17). Оценка объективных TH-зависимых метаболических эффектов варьировалась в этих испытаниях, в которых основное внимание уделялось когнитивным функциям, настроению и качеству жизни (QoL) (дополнительная таблица S2). |
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|