
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
4.Коллоидты ерітінділердің тұрақтылығы
Дисперстік жү йелердің тұ рақ тылығ ы деп олардың қ асиеттерінің (дисперстігінің, дисперстік ортада біркелкі таралуының, фазааралық ә рекеттесудің ) уақ ыт ө ту барысында ө згеріссіз қ алуын (тұ ракты болуын) айтады. Демек, тұ рақ тылық деп дисперстік жү йелердің ірілену жә не шө гу қ ұ былыстарына қ арсы тұ ра алу қ абілетін айтады. Дисперстік жү йенің тұ рақ тылығ ының теориялық жә не практикалық маң ызы бар.
Песковтың ұ сынысы бойынша дисперстік жү йелердің тұ рақ тылығ ын екіге бө ліп: 1) шө гу қ ұ былысына қ арсы тұ ра алу жә не 2) бө лшектердің бірігіп, ірілену қ ұ былысына қ арсы тұ ра алу қ абілеті деп қ арастырғ ан жө н. Бірінші тұ рақ тылық ты седиментациялық тұ рақ тылық деп атайды. Екіншісін - агрегаттық тұ рақ тылық деп атайды. Агрегаттық тұ рақ тылық тың ө зі термодинамикалық жә не кинетикалық тұ рақ тылық болып екіге бө лінеді.
Термодинамикалық тұ рақ ты жү йелер бір фаза екінші фазаның кө лемінде ұ сақ бө лшектер (тамшылар) тү рінде ө з бетімен таралуы нә тижесінде тү зіледі. Термодинамикалық тұ рақ ты жү йелерді лиофилъдік жү йелер деп атайды. Бірақ термодинамикалық тұ рақ сыз жү йелер кинетикалық тұ рғ ысынан тұ рақ ты болуы мү мкін. Мұ ндай жү йелерді кинетикалық тұ рақ ты жү йелер деп атайды. Кинетикалық тұ рақ ты жү йелерді лиофобтық жү йелер деп атайды. Лиофобтық жү йелер белгілі бір уақ ыт аралығ ында ғ ана тұ рақ ты болады, одан кейін оның агрегаттық тұ рақ тылығ ы бұ зылады.
Қ атты бө лшектердің бір-бірімен байланысып іріленуін коагуляция деп, ал тамшылардың қ осылып іріленуін коалесценция деп атайды. Бө лшектердің (тамшылардың ) іріленуі, сонымен бірге, изотермиялық айдау барысында да байқ алады. Изотермиялық айдау деп тұ рақ ты температурада кіші бө лшектердің еріп, тамшылардың буланып, ү лкен бө лшектерге (тамшыларғ а) конденсациялануы нә тижесінде бө лшектердің одан ә рі қ арай ірілену қ ұ былысын айтады.
Лиофобтық жү йелердің агрегаттық тұ рақ тылығ ы коагуляция жылдамдығ ы арқ ылы сипатталады. Б. В. Дерягинның кө зқ арасына сә йкес агрегаттық тұ рақ тылыктың негізі болып сынама қ ысым (П) саналады. Сынама қ ысым (1-сурет) екі бө лшек (1) бір-біріне жакындағ анда арасындағ ы дисперстік ортаның (қ абыршақ тың ) (2) қ атты жұ қ аруының нә тижесінде пайда болады.
Сынама қ ысым деп жұ қ а қ абыршақ тағ ы тепе-тең дік кү йді сақ тап қ алу ү шін қ абыршақ қ а тү сірілетін қ ысымды айтады. Сынама қ ысым екі бө лшек арасындағ ы қ абыршақ тағ ы қ ысымнан ( 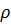 ) дисперстік ортаның кө леміндегі қ ысымды (
) дисперстік ортаның кө леміндегі қ ысымды ( 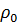 ) алып тастағ анғ а тең:
) алып тастағ анғ а тең:
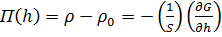 (1)
(1)
Мұ ндағ ы һ - қ абыршақ тың қ алың дығ ы; S - жанасушы бет ауданы. 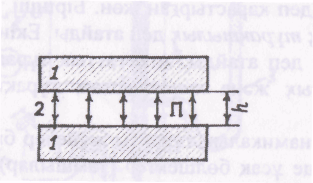
1-сурет. Сынама қ ысымның пайда болуының сызба-нұ скасы
Сынама қ ысым бө лшектер арасындағ ы тартылыс (теріс қ ұ раушы бө лігі) жә не тебіліс (оң қ ұ раушы бө лігі) кү штерінен қ ұ ралады. Сондық тан оның мә ні оң немесе теріс те болуы мү мкін. Сынама қ ысымның теріс қ ұ раушы бө лігін фазалардағ ы атомдар мен молекулалар арасындағ ы тартылыс кү штері кұ райды. Тартылыс кү штерінің ішіндегі кең тарағ аны Ван-дер-Ваальс кү штері.
Оң қ ұ раушы бө лігін бө лшектер арасындагы электростатикалық тебіліс кү штері қ ұ райды. Электростатикалық тебіліс кү штері бө лшек пен дисперстік ортаның арасында қ ос электрлік қ абаттың тү зілуі нә тижесінде пайда болады.
Жалпы термодинамикалық жә не кинетикалық тұ рақ тылық тарды қ амтамасыз ететін мынадай факторлар бар:
1. Электростатикалық фактор, ол Қ ЭҚ -тың болуымен қ амтамасыз етіледі;
2. Адсорбциялық -солъваттық фактор, ол бө лшектің дисперстік ортамен ә рекеттесуі нә тижесінде фазааралық керілудің кемуімен қ амтамасыз етіледі;
3. Энтропиялық фактор, ол тек ультрамикрогетерогенді жү йелерге ғ ана тә н жә не жылулық қ озғ алыстың нә тижесінде бө лшектердің дисперстік ортада біркелкі таралуына ұ мтылысымен қ амтамасыз етіледі;
4. Қ ұ рылымдық -механикалық фактор, ол фазааралық бө лу бетінде серпімділік жә не беріктік қ асиеттері бар адсорбциялық қ абаттардың тү зілуімен қ амтамасыз етіледі;
5. Гидродинамикалық фактор, ол бө лшектердің беттік қ абатындағ ы дисперстік ортаның тұ тқ ырлығ ының артуымен қ амтамасыз етіледі;
6. Аралас факторлар. Ол жоғ арыдағ ы факторлардың бірнешеуінің бір мезгілде ә сер етуі нә тижесінде іске асады.
Коагуляция кинетикасы
Коагуляция деп дисперстік бө лшектердің ө зара жанаса бірігіп ірілену қ ұ былысын айтады. Коагуляция лиофобтық жү йелерге тә н. Коагуляция жылдамдығ ы жү йенің агрегаттық тұ рақ тылығ ының ө лшемі болып саналады. Коагуляция жылдамдығ ы ә ртү рлі болуы мү мкін. Сондық тан коагуляция кинетикасын қ арастырғ анда оны жылдам жә не баяу коагуляция жылдамдық тары деп екіге бө ліп қ арастырады.
Жылдам коагуляция кезінде бө лшектердің ө зара кез-келген соқ тығ ысуы олардың бірігуіне ә келеді. Оның кинетикасын зерттеген М. Смолуховский (1916 ж. ). Ол коагуляцияның жылдамдығ ын бимолекулалық реакцияның кинетикалық тең деуін пайдалана отырып сипаттады:
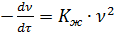 (2)
(2)
Мұ ндағ ы 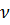 - бө лшектердің сандық концентрациясы;
- бө лшектердің сандық концентрациясы; 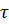 - уақ ыт; Кж- коагуляция жылдамдығ ының константасы, ол Кж =
- уақ ыт; Кж- коагуляция жылдамдығ ының константасы, ол Кж = 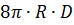 - ғ а тең (
- ғ а тең ( 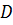 -диффузия коэффициенті,
-диффузия коэффициенті, 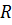 -бө лшектер арасындағ ы қ ашық тық.
-бө лшектер арасындағ ы қ ашық тық. 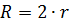 ,
, 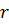 - бө лшектің радиусы). Жоғ арыдағ ы тендеуді интегралдасақ мынадай тендеу аламыз:
- бө лшектің радиусы). Жоғ арыдағ ы тендеуді интегралдасақ мынадай тендеу аламыз:
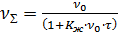 (3)
(3)
Мұ ндагы 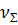 - жү йедегі бө лшектердің жалпы сандық концентрациясы;
- жү йедегі бө лшектердің жалпы сандық концентрациясы; 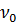 - бө лшектердің бастапқ ы сандық концентрациясы. Бұ л тең деу - М. Смолуховскийдің жылдам коагуляция кинетикасының тең деуі деп аталады.
- бө лшектердің бастапқ ы сандық концентрациясы. Бұ л тең деу - М. Смолуховскийдің жылдам коагуляция кинетикасының тең деуі деп аталады.
М. Смолуховский тең деуі коагуляция жылдамдығ ы бө лшектердің сандық концентрациясы мен броундық қ озғ алысының интенсивтігіне байланысты деген қ ағ идағ а негізделіп қ орытылғ ан. Коагуляция жылдамдығ ының константасын теория бойынша анық тау қ иын, сондық тан М. Смолуховский жартылай коагуляция уақ ыты (коагуляцияның жартылай периоды) (Ө ) деген ұ ғ ым енгізді. Коагуляцияның жартылай периоды деп бө лшектердің бастапқ ы сандық концентрациясы екі есеге азаятын уақ ытты айтады. Демек, 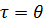 болғ анда,
болғ анда, 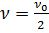 , олай болса жоғ арыдағ ы М. Смолуховский тең деуін былай жазуғ а болады:
, олай болса жоғ арыдағ ы М. Смолуховский тең деуін былай жазуғ а болады:
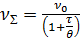 (4)
(4)
Мұ ндағ ы 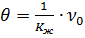 .
.
Жылдам коагуляцияның жылдамдық константасын графикалық жолмен анық тауғ а болады. Ол ү шін М. Смолуховский тең деуінің тү зу сызық ты тү рін жазады:
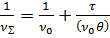 (5)
(5)
Сонан сон  шамасының уақ ытқ а (
шамасының уақ ытқ а ( 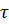 ) тә уелдігі графигін тұ рғ ызады. Бұ л байланыс тү зу сызық ты (2-сурет). Графиктен
) тә уелдігі графигін тұ рғ ызады. Бұ л байланыс тү зу сызық ты (2-сурет). Графиктен 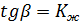 табады. Ал тү зу сызық тың ордината ө сімен қ иылысқ ан нү ктесі
табады. Ал тү зу сызық тың ордината ө сімен қ иылысқ ан нү ктесі 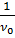 шамасына тең.
шамасына тең.
Коагуляция барысында жеке (біріншілік) бө лшектер бірігіп екіншілік, олар ө зара бірігіп ү штік, тө рттік бө лшектерге айналады. Сонда m-ретті (біріншілік, екіншілік, ү штік жә не тө рттік) бө лшектердің сандық концентрациялары мына тең деу арқ ылы анық талады:
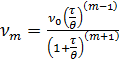 (6)
(6)
Мұ ндағ ы т - бө лшектің ө лшемдік дә режесі (т =1 болса бірлік, т=2 болса екіншілік бө лшектер).
Сонда біріншілік бө лшектер ү шін: 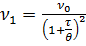 ;
;
екіншілік бө лшектер ү шін:  ;
;
ү штік бө лшектер ү шін 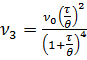 .
.
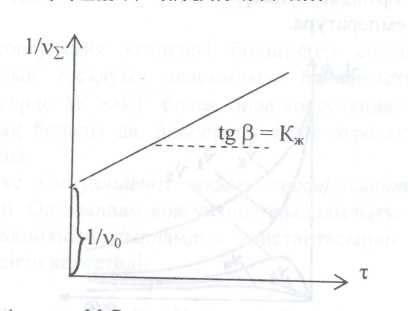
2-сурет. М. Смолуховский тең деуінің тұ рақ тыларын графикалық ә діспен анық тау
Біріншілік бө лшектердің сандық концентрациясы уақ ыт ө ткен сайын кемиді. Ал екіншілік, ү штік жә не тө рттік бө лшектердің концентрациялары бастапқ ыда артады да, сонан соң азаяды. Бө лшектердің сандық концентрацияларының уақ ытқ а байланысты ө згерістері 3-суретте кө рсетілген.
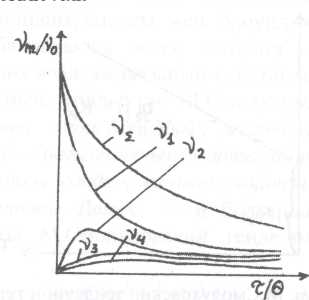
3-сурет. Бө лшектердің сандық концентрацияларының уақ ыт бойынша ө згерістері
Жалпы коагуляция жылдамдығ ының константасы потенциалдық тосқ ауылғ а (  Е) жә не бө лшектердің соқ тығ ысу кезінде кең істікте бір-біріне ың ғ айлы бағ ытталып орналасу кө бейткішіне (Р) тә уелді:
Е) жә не бө лшектердің соқ тығ ысу кезінде кең істікте бір-біріне ың ғ айлы бағ ытталып орналасу кө бейткішіне (Р) тә уелді:
Кж = 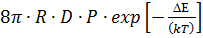 (7)
(7)
Жылдам коагуляция жағ дайына бө лшектердің ө зара кез-келген соқ тығ ысуы коагуляцияғ а ә келеді, яғ ни потенциалдық тосқ ауыл нольге тең (  Е=0), ал бө лшектер соқ тығ ысу кезінде кең істікте ың ғ айлы бағ ытталып орналасады (Р=1) деп карастырылады. Олай болса шар тә різдес бө лшектің диффузия коэффициенті (D) мен радиусы (r) арасындағ ы байланысты (Эйнштейн тендеуін) ескере отырып, жылдам коагуляция константасының тендеуін былай жазуғ а болады:
Е=0), ал бө лшектер соқ тығ ысу кезінде кең істікте ың ғ айлы бағ ытталып орналасады (Р=1) деп карастырылады. Олай болса шар тә різдес бө лшектің диффузия коэффициенті (D) мен радиусы (r) арасындағ ы байланысты (Эйнштейн тендеуін) ескере отырып, жылдам коагуляция константасының тендеуін былай жазуғ а болады:
Кж = 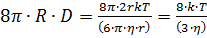 (8)
(8)
Мұ ндағ ы 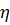 - ортаның тұ тқ ырлығ ы;
- ортаның тұ тқ ырлығ ы; 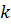 - Больцман тұ рақ тысы; Т -абсолюттік температура.
- Больцман тұ рақ тысы; Т -абсолюттік температура.
Ал коагуляцияның жартылай периодын Кж арқ ылы ө рнектейтін болсақ тө мендегідей тең деу аламыз:
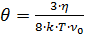 (9)
(9)
Демек, жылдам коагуляция жылдамдығ ының константасы ортаның температурасына тура, ал тұ тқ ырлығ ына кері пропорционал байланысты. Жартылай коагуляция периоды ортаның температурасы мен тұ тқ ырлығ ына жә не бө лшектердің бастапқ ы сандық концентрациясына кері, ал ортаның тұ тқ ырлығ ына тура пропорционал тә уелді.
Баяу коагуляция кезінде бө лшектердің ө зара соқ тығ ысуы барысында коагуляция бола бермейді, ягни коагуляция жү ру ү шін бө лшектердің ө зара соқ тығ ысуы жеткіліксіз (Р 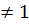 ). Коагуляция жү ру ү шін бө лшектердің бойында «потенциалдық тосқ ауылды» (
). Коагуляция жү ру ү шін бө лшектердің бойында «потенциалдық тосқ ауылды» ( 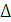 Е
Е 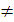 О) асып ө ту ү шін қ ажетті энергияның артық мө лшері болуы тиіс. Сондық тан баяу коагуляция ү шін жылдамдық константасының (Кб) мә нін былай ө рнектеуге болады:
О) асып ө ту ү шін қ ажетті энергияның артық мө лшері болуы тиіс. Сондық тан баяу коагуляция ү шін жылдамдық константасының (Кб) мә нін былай ө рнектеуге болады:
Кб - КжРехр [- 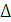 Е /(
Е /( 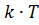 )],
)],
немесе Кб = 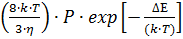 . (10)
. (10)
Баяу коагуляция кезіндегі бө лшектер соқ тығ ысуы мен энергетикалық тосқ ауыл арасындағ ы байланысты Н. А. Фукс кө рсетті. Егерде 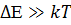 болса, онда коагуляция жылдамдыгы нольге жуық болады да, дисперстік жү йе агрегаттық тұ рақ ты кү йде болады.
болса, онда коагуляция жылдамдыгы нольге жуық болады да, дисперстік жү йе агрегаттық тұ рақ ты кү йде болады.
Н. А. Фукс коагуляцияны тежеу коэффициенті ( 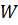 ) деген ұ ғ ым енгізді. Ол жылдам коагуляция жылдамдығ ы константасы баяу коагуляцияның жылдамдық константасынан қ анша есеге артық екендігін кө рсетеді:
) деген ұ ғ ым енгізді. Ол жылдам коагуляция жылдамдығ ы константасы баяу коагуляцияның жылдамдық константасынан қ анша есеге артық екендігін кө рсетеді:
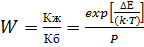 (11)
(11)
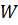 -ді кейде тұ рақ тылық факторы немесе тұ рақ тылық коэффициенті деп те атайды.
-ді кейде тұ рақ тылық факторы немесе тұ рақ тылық коэффициенті деп те атайды.
Бө лшектердің коагуляциясы электролиттердің қ атысында да байқ алады. Электролиттерді индифферентті жә не индифферентті емес деп екі топқ а бө леді. Индифферентті электролиттің иондары беттің зарядын ө згерте алмайды. Оларды коллоидтық ерітіндіге қ осқ анда қ ос электрлік қ абаттың диффузиялық бө лігі сығ ылады да, электрокинетикалық потенциалдың шамасы азаяды. Соның нә тижесінде энергетикалық тосқ ауыл азайып, электролиттің концентрациясының белгілі бір мә нінде коагуляция жү реді.
Индифферентті емес электролиттердің қ арсы иондары бө лшектің бетіне ерекше (спецификалық ) кү штер арқ ылы адсорбциялана алады, соның нә тижесінде беттің заряд таң басы ө згеруі мү мкін.
Коагуляция жү ру ү шін қ ажетті электролиттің минимальді концентрациясын коагуляция табалдырығ ы деп атайды. Коагуляция табалдырығ ы қ арсы ионның валенттігі мен радиусына байланысты. Ионның валенттігі ө скен сайын оның коагуляциялау қ абілеті артады, яғ ни электролиттің коагуляция табалдырығ ы азаяды.
ДЛФО теориясына сә йкес коагуляция табалдырыгы (ск) мен қ арсы ион валенттігінің (z) алты дә режесі арасында кері байланыс бар:
Ск = 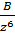 (12)
(12)
Мұ ндағ ы В - тұ рақ ты шама.
(12) тең деу Дерягиннің " алтыншы дә реже" заң ының тең деуі деп аталады. Сонда бір, екі жә не ү ш валентті катиондардың (мысалы, Nа+, Са2+ Аl3+) коагуляция табалдырық тарының ө зара қ атынасы мынадай болады:
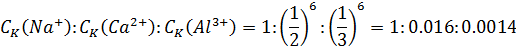
Щульце-Гарди ережесіне сә йкес дә л осы қ арсы иондардың коагуляция табалдырық тарының ө зара қ атынасы мынадай болуы тиіс:
 1: 0. 05: 0. 002
1: 0. 05: 0. 002
Валенттіктері бірдей иондарды қ арастыратын болсақ, ионның радиусы артқ ан сайын оның коагуляциялау қ абілеті артады, яғ ни коагуляция табалдырығ ы кемиді. Оның себебі ионның радиусы ө скен сайын оның гидратациялануы нашарлайды. Гидратациялану кемісе, ионның еріткішпен ә рекеттесуі ә лсіреп, бетпен ә рекеттесуі кү шейе тү седі. Сонда тө мендегі лиотроптық қ атарда ионның коагуляциялау қ абілеті солдан оң ғ а қ арай кемуі тиіс:
Cs+> Rb+> K+> Na+> Li+
Сол сияқ ты, аниондар қ атарында да олардың радиусы артқ ан сайын, коагуляциялау қ абілеті нашарлайды:
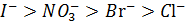
Потенциалдың аз мә нінде диффузиялық қ абаттың потенциалы ( 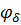 ) мен қ алың дығ ы (
) мен қ алың дығ ы ( 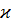 кр) арасындағ ы байланыс Эйлерс-Корфтың эмпирикалық ережесі арқ ылы ө рнектеледі:
кр) арасындағ ы байланыс Эйлерс-Корфтың эмпирикалық ережесі арқ ылы ө рнектеледі:
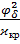 = B= соnst (13)
= B= соnst (13)
Мұ ндағ ы 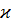 кр - критикалық диффузиялық қ абаттың қ алындығ ына кері шама.
кр - критикалық диффузиялық қ абаттың қ алындығ ына кері шама.
Демек, электролит қ осқ анда диффузиялық қ абаттың потенциалы мен қ алың дығ ы кемиді. Электрокинетикалық потенциалдың абсолюттік шамасы 20 ÷ 40 мВ-қ а тең болғ анда коллоидтық бө лшектердің арасындағ ы тартылыс кү ші тебіліс кү шінен басым болады да, коагуляция жү реді.
Коагуляцияғ а кері қ ұ былысты, яғ ни коллоидтық бө лшектердің қ айтадан тұ рақ тылық қ а ие болу қ ұ былысын пептизация деп атайды. Пептизация коагулюмдерді (коагуляция нә тижесінде тү скен тұ нбаларды) таза еріткішпен немесе басқ а электролиттің ерітіндісімен жуғ анда байқ алады.
Негізгі тү сініктер: гранула, мицелла, адсорбциялық қ абат, диффузиялық қ абат, броундық қ озғ алыс, диффузия, осмостық қ ысым, седиментация, коагуляция, жылдам коагуляция, баяу коагуляция, коагуляциянытежеу коэффициенті, коагуляция табалдырығ ы, пептизация
Ө зін-ө зі бақ ылау сұ рақ тары:
1. Мицелла, гранула ұ ғ ымына тү сінік бер.
2. Броундық қ озғ алыс туралы тү сінік.
3. Диффузия туралы тү сінік.
4. Осмостық қ ысым туралы тү сінік.
5. Седиментация туралы тү сінік.
6. Коагуляция жә не пептизация ұ ғ ымдары.
Қ олданылғ ан ә дебиет:
Мұ сабеков Қ. Б., Ә бдиев Қ. Ж. Коллоидтық химия: Оқ улық. -Алматы: 2011. -10-24 б.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|