
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
4. ТЕМІР СПЕКТРІМЕНТАНЫСУ ЖӘНЕ СПЕКТРЛIК СЫЗЫҚТАРДЫҢ ТОЛҚЫН ҰЗЫНДЫҚТАРЫН
4. ТЕМІР СПЕКТРІМЕНТАНЫСУ ЖӘ НЕ СПЕКТРЛIК СЫЗЫҚ ТАРДЫҢ ТОЛҚ ЫН Ұ ЗЫНДЫҚ ТАРЫН
Ө ЛШЕУ Ә ДIСТЕРI
4. 1. Жұ мыстың мақ саты мен мазмұ ны
Заттың атомдық спектрін бақ ылап, зерттеуді ү йрену. Темір спектрімен (эталондық салыстыру спектрі) танысу, оның кез келген бө лігін дә л анық тай білуді, заттың атомдық спектріндегі спектрлік сызық тардың толқ ын ұ зындық тарын дә л анық тай білуді игеру. Химиялық элементтердің спектрлік сызық тары кестелерін, спектрлік сызық тардың атласын зерттеу жү ргізгенде пайдалана білуге дағ дылану.
Спектрлiк сызық тардың белгiлi сызық тарғ а қ атысты орнын ө лшеу ү шiн МИР-12 микроскопы пайдаланылады[4, 11, 12, 19-23].
4. 2. Қ ысқ аша теориялық кiрiспе
1. Электромагниттiк сә уле спектрi. Кө рiнетiн сә уле мен радиотолқ ындар, рентген ультракү лгiн, инфрақ ызыл жә не g-сә улелерi-бұ лар бiр-бiрiнен толқ ын ұ зындығ ы (жиiлiгi) бойынша ө згеше электромагниттiк сә уле тү рлерi. Толқ ын ұ зындығ ының (жиiлiгiнiң ) ө суi бойынша орналастырғ анда бұ лар электромагниттiк толқ ындардың толық спектрiн қ ұ райды, сонда толқ ын ұ зындығ ы нанометрдiң бө лiгiнен бастап бiрнеше км-ге дейiн ө згеретiн ө те кең аралық ты алып жатады (4. 1-кесте).
4. 1-кесте
Электромагниттiк толқ ындар спектрi
| Электромагниттiк сә уле тү рi | Толқ ын ұ зындық тар диапазоны |
| g-сә уле | £ 10-2 нм |
| рентген | 10-2 - 1 нм |
| ультракү лгiн | 5 – 400 нм |
| кө рiнетiн сә уле (жарық ) | 400-750 нм |
| инфрақ ызыл | 760 нм-300 мкм |
| микротолқ ындар | 300 мкм-300 мм |
| радиотолқ ындар | 300 мм-ден бiрнеше км-ге дейiн |
2. Заттың шығ ару спектрi мен жұ тылу спектрiнiң пайда болуы ә рқ ашанда оның атомдары мен молекулаларының iшкi энергиясының ө згеруiмен байланысты. Iшкi энергия қ оры ең аз бө лшектер (атом, молекула) қ озбағ андеп, ал бұ лардың тұ рғ ан кү йi қ алыпты, немесе негiзгi деп аталады. Сырттан ә сер ету арқ ылы зат бө лшектерiне (атомына, молекуласына) қ осымша энергия беруге болады; мұ ны жұ тып олар қ алыпты (негiзгi) кү йден қ озғ ан кү йге кө шедi. Атомдар мен молекулалардың iшкi энергиясы ү здiксiз ө згере алмайды, ол тек секiрмелi тү рде, дискреттi ө згередi. Ә рбiр элементтiң атомдары ү шiн, ә рбiр заттың молекулалары ү шiн ө здерiне тә н энергетикалық кү йлердiң мү мкiн дискреттi қ атары болады. Сондық тан да олар энергияны белгiлi қ атаң энергия ү лестерi (кванттары) тү рiнде ғ ана шығ арып жә не жұ та алады. Энергия ү лесiн жұ тқ анда немесе шығ арғ анда бө лшек (атом, молекула) бiр мү мкiн энергетикалық кү йден басқ а кү йге кө шедi [4, 11, 12, 19-23].
Атомдар мен молекулалардың энергетикалық кү йлерi шартты тү рде горизонтал тү зулер - энергетикалық дең гейлер (4. 1-сурет) тү рiнде кескiнделедi. Ең тө менгi дең гей–негiзгiЕ1 дең гей микробө лшектiң негiзгi кү йiне сә йкес келедi. Бұ дан жоғ ары Е2, Е3, Е4,... жә не т. б. дең гейлерi орналасады; бұ лардың ә рқ айсысы нақ ты қ озғ ан кү йге сә йкес келедi. Жә не де жоғ арырақ (биiгiрек) энергетикалық дең гейге атомның не молекуланың iшкi энергиясының молырақ қ оры сә йкес келедi.
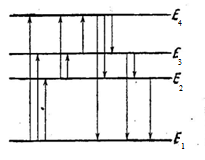
Сурет 4. 1. Атомның энергиялық дең гейлерi схемасы
Стрелкалармен мү мкiн болатын ауысулар кө рсетiлген
Микробө лшектi негiзгi дең гейден қ озғ ан дең гейге ауыстыру ү шiн микробө лшекке берiлетiн энергия қ оздыру энергиясы деп аталады. Қ оздыру энергиясы кө бiнесе электрон-вольтпен (эВ) ө лшенедi.
Зат бө лшектерiнiң энергияны жұ ту процесi жоғ ары бағ ытталғ ан стрелкалармен, ал энергия шығ ару процесi-тө мен бағ ытталғ ан стрелкалармен белгiленедi (4. 1-сурет).
Зат бө лшектерi энергияны екi дең гей энергиясының айырмасына тең энергия ү лестерiмен (кванттар) жұ тып жә не шығ ара алады.
Электромагниттiк сә уле кванттары (фотондар) тү рiнде энергия жұ тылғ ан жә не шығ арылғ ан кезде бұ ғ ан сә йкес заттың жұ тылу жә не шығ ару спектрлерi алынады. Сонда энергиясы екi энергетикалық дең гей энергияларының айырмасына тең кванттар (фотондар) ғ ана жұ тылады жә не шығ арылады. Мысалы, атом Е1 дең гейден Е2 дең гейге Е2-Е1айырмасына тең hn1, 2 квантты, ал Е2 дең гейден Е3дең гейге hn2, 3=Е3–Е2 квантты жұ тып ауысады.
Ә рбiр ауысу нақ ты жиiлiгi бар квантты қ ажет етедi, ал оны араларында ауысу болатын дең гейлердiң энергиясы белгiлi болса есептеп табуғ а болады. Мысалы, 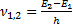 ;
; 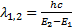 .
.
Берiлген заттың дең гейлерi арасында қ анша кванттық ауысу мү мкiн болса, ол теория жү зiнде жиiлiктерi ә ртү рлi сонша квантты жұ та алады. Осы жиiлiктер жиынтығ ы заттың жұ тылу спектрiн бередi. Заттың шығ ару спектрi осы заттың атомдары (молекулалары) жоғ арырақ дең гейлерден тө менiрек дең гейлерге ауысқ ан кезде шығ ара алатын барлық жиiлiктердiң (толқ ын ұ зындық тарының ) жиынтығ ы болып табылады. Заттың шығ ару спектрiндегi жиiлiктер оның жұ тылу спектрiндегi жиiлiктермен дә л келетiндiгi айтпаса да тү сiнiктi.
Ә рбiр заттың ө зiнiң дең гейлер саны жә не дең гейлер энергияларының айырмасы бойынша басқ а заттардан ө згеше энергетикалық дең гейлер жиынтығ ы болады. Сондық тан ә р тү рлi заттың спектрлерi шығ аратын немесе жұ тылатын кванттарының (фотондарының ) жиiлiктерi бойынша да, бұ лардың саны бойынша да бiрiнен-бiрi ө згеше болады. Осы жағ дай зат спектрiн зерттеп оның химиялық қ ұ рамы жө нiнде қ орытынды жасауғ а мү мкiндiк бередi.
3. Спектр тү рлерi: сызық тық, жолақ жә не тұ тас.
Сызық тық спектрлер бiр-бiрiнен бiршама қ ашық тық тарда орналасқ ан жеке-жеке сызық тардан тұ рады. Сызық тық спектрлер молекулағ а бiрiкпеген жә не бiр-бiрiмен ә серлеспейтiн жеке атомдар жарық шығ арғ ан жағ дайда алынады. Сызық тық спектр беретiн кө п тарағ ан жарық кө здерi: солғ ын, доғ алық жә не ұ шқ ындық разрядтар, жалын.
Жолақ спектрлер ә рқ айсысы ө те жиi орналасқ ан, кей жағ дайда бiрiгiп кеткен сызық тар жиынтығ ы болып табылатын енi ү лкенiрек немесе кiшiрек болып келетiн жолақ тардан тұ рады. Жолақ спектрлер молекулаларғ а тә н.
Ү здiксiз (тұ тас) спектр тұ тас кең жолақ тү рiнде бiр-бiрiмен қ осылып кеткен ө те кө п сызық тар болып табылады. Тұ тас спектр қ ыздырылғ ан қ атты немесе сұ йық зат шығ аратын сә уленi толқ ын ұ зындық тары бойынша жiктеген кезде алынады.
4. Заттың шығ ару спектрiн алу ү шiн оның бө лшектерiне қ осымша энергия берiп қ оздыру керек. Осы мақ сатта зат ү лгiсi жарық кө зiне ендiрiледi. Мұ нда ү лгi қ ыздырылып, буғ а айналады, зат молекулалары атомдарғ а жiктеледi (диссоциацияланады), жекелеген атомдар мен иондардың қ оздырылуы iске асырылады. Зат бө лшектерi қ озғ ан кү йде ө те қ ысқ а уақ ыт (10-7-10-8с) болады, содан ө здiгiнен қ алыпты кү йге оралып, артық энергияларын жарық кванттары тү рiнде шығ арады, ал бұ лар зат ү лгiсiнiң шығ ару спектрiн қ ұ райды. Егер ү лгiдегi барлық элемент атомдары бiр мезгiлде қ оздырылатын болса, онда спектрде бұ лардың ә рқ айсысына сә йкес жиiлiктер (толқ ын ұ зындық тар) - сызық тар алынатын болады.
Зат ү лгiсiнiң тiркелген спектрiн талдау керек болады. Ө йткенi ә рбiр элементтiң жә не ә рбiр заттың ө зiнiң нақ ты толқ ын ұ зындық тарына сә йкес сызық тардан немесе жолақ тардан тұ ратын сипаттауыш спектрi болады. Сондық тан спектрлiк талдау жү ргiзгенде сызық тардың (жолақ тардың ) толқ ын ұ зындық тары анық талады жә не бұ лардың қ андай элементтердiкi екендiгi анық тама ә дебиет арқ ылы тағ айындалады.
Зат ү лгiсi спектрiн зерттеудi жә не талдауды мү мкiн ету ү шiн жиiлiктерi ә ртү рлi кванттарды кең iстiкте бiр-бiрiнен ажырату керек, басқ аша айтқ анда, электромагниттiк сә уленi жиiлiк (толқ ын ұ зындық ) бойынша жiктеу керек. Осы процесс жарық ты спектрге жiктеудеп аталады. Бұ л спектрлiк аспаптарда iске асырылады.
Толқ ын ұ зындық тары бойынша жiктелген сә уле ә йтеуiр бiр амалмен тiркелуi керек. Бұ л ү шін жарық ты тiркеудiң ә р тү рлi ә дiстерi қ олданылады, кө п тарағ аны фотографиялық жә не фотоэлектрлiк ә дiстер.
Фотографиялық тiркеу ә дiсi фотопленка немесе фотопластинкағ а тү скенде жарық бұ лардың қ араюын тудыруына негiзделген. Шығ ару спектрi осы жағ дайда пластинканың (ә йнектiң ) бетiнде қ ара сызық тар (сызық тық спектр) немесе қ ара жолақ тар (жолақ спектр) тү рiнде алынады.
5. Атомдық спектрлер. Атомдар электромагниттiк сә уленi шығ арғ ан жә не жұ тқ ан жағ дайда сә уле жұ тқ ан немесе шығ арғ ан ә рбiр атомның iшкi энергиясы ө згередi.
Атомның iшкi энергиясы оның ядросының энергиясы мен электрондарының энергиясынан қ ұ ралады. Егер атомғ а сырттан ә сер етiлмесе, онда оның ядросы мен электрондары атомның iшкi энергиясы ең аз болатындай энергетикалық кү йлерге жайғ асады, яғ ни атом қ озбағ ан болады. Бiр элементтiң барлық атомдарының iшкi энергиялары бiрдей болады.
Атомды оғ ан сырттан қ осымша энергия беру арқ ылы ғ ана қ оздыруғ а болады. Ядроны қ оздыру ү шiн 105 эВ шамасындағ ы ү лкен энергия қ ажет, бұ л g-сә улесi кванттарына сә йкес келедi. Оптикалық жә не рентген спектрлерi алынатын жағ дайларда атом ядроларының энергиясы ө згермейдi де, атомдардың iшкi энергиясы тек электрондардың энергетикалық кү йлерiне тә уелдi болады.
Ядромен берiк байланысқ ан толғ ан iшкi электрондық қ абық тағ ы электронды қ оздыру немесе жұ лып шығ ару ү шінедә уiр жоғ ары мө лшерде (жү здеген эВ болатын) энергия қ ажет. Iшкi электрондық қ абық тар ө згерiске ұ шырағ анда атомдар рентген сә улесi кванттарын жұ тып немесе шығ аратын болады, бұ лар элементтiң рентгендiк спектрiнқ ұ райды.
Атомның сыртқ ы жә не толмағ ан iшкi электрондық қ абық тарының электрондары ядромен едә уiр ә лсiз байланысқ ан. Бұ ларды қ оздыру ү шiн, тiптi жұ лып шығ ару ү шiн бар болғ аны бiрнеше эВ энергия жеткiлiктi. Кө рiнетiн, ультракү лгiн, инфрақ ызыл сә уле фотондарының энергиясы осы шамалас болады жә не де осындай энергияны атомдар доғ алық, ұ шқ ындық разряд сияқ ты жарық кө здерiнде қ абылдай алады.
Сонымен, оптикалық спектрлер алынатын жағ дайларда атом энергиясының ө згерiсi тек оптикалық электрондар энергиясының ө згеруiне байланысты болады. Сыртқ ы жә не толмағ ан iшкi қ абық тардағ ы электрондар осылай аталады. Химияда осы электрондар валенттiкдеп аталады, ө йткенi бұ лар химиялық байланысқ а қ атысады жә не элементтердiң валенттiлiгiн анық тайды.
Мысалы, натрийдің қ оздырылмағ ан атомында 11Na 1s22s22p63s1 сыртқ ы қ абық тын3sкү йдегi электрон оптикалық болып табылады.
Алюминий атомында ү ш оптикалык электрон бар: Al 1s22p22p63s23p1.
Бұ лардың бә рi сыртқ ы қ абық та, бiрақ екеуi 3s кү йде (n=3, l=0), ал бiреуi 3p кү йде (n=3, l=1).
6. Химиялық элементтердiң атомдық спектрi сызық тық. Ә рбiр элементтiң басқ а элементтердiң спектрлерiнен сызық саны жә не бұ лардың толқ ын ұ зындығ ы басқ аша ө зiне тә н спектрi болады. Элемент спектрiнiң қ ұ рылымы оның атомдарының iшкi энергиясының мү мкiн мә ндерiмен анық талады. Оптикалық спектрлердi алу жағ дайларында атомның iшкi энергиясы оптикалық электрондардың энергиясына ғ ана тә уелдi, басқ а iшкi энергия тү рi сияқ ты ол тек дискреттiө згере алады.
Мысалы, қ оздырылмалғ ан натрий атомындағ ы оптикалық электрон 3s кү йде орналасқ ан, ал атом қ оздырылғ ан кезде ол 3s кү йден 3p, 4s, 3d, 4p, 5s жә не т. б. кү йлерiне кө ше алады.
Оптикалық электронның ә рбiр кү йiне атомның нақ ты iшкi энергиясы, нақ ты энергетикалық дең гейi сә йкес келедi. Сондық тан, оптикалық электронның бiр мү мкiн кү йден басқ а мү мкiн кү йге кө шуi атомның энергетикалық дең гейiнiң тиiстi ө згерiсiмен қ атар жү редi. Оптикалық электрондардың энергетикалық кү йлерiнiң саны жә не бұ лардың энергиясы, демек спектр қ ұ рылымы тү гелдей атомның қ ұ рылысына: ядро зарядына, iшкi электрондық қ абық тар қ ұ рылысына, оптикалық электрондардың саны мен кү йiне тә уелдi.
Бiр элемент атомдарының қ ұ рылысы бiрдей, сондық тан да оптикалық электрондарының мү мкiн болатын кү йлерiнiң жиынтығ ы да бiрдей болады. Ал ә ртү рлi элемент атомдарының қ ұ рылысы ә ртү рлi, сондық тан да бұ лардың дең гейлерi мен спектрлерi бiр-бiрiнен ө згеше болады.
Шығ ару (эмиссиялық ) спектрiндегi ә рбiр сызық қ озу энергиясымен (немесе қ озу потенциалымен) сипатталады. Мә селен, сутегiнiң бiрiншi резонанстық сызығ ының қ озу энергиясы 10, 2эВ (4. 2-кесте). Сутегi спектрiндегi сызық тардың бә рi серияларғ а топтасады. Бiр серияғ а жататын сызық тардың бә рiнiң тө менгi дең гейi бiрдей, ал жоғ арғ ы дең гейлерi ә ртү рлi болады.
Бiр серияғ а жататын сызық тар спектрдiң қ ысқ а толқ ынды бө лiгiне қ арай бiр-бiрiне жақ ындай бередi де, толқ ын ұ зындық тың едә уiр аумағ ын алып жататын тұ тас спектрге ауысады.
Сутегi тә рiздi иондар, яғ ни бiр электроны бар иондар (Не+, Li2+, Be3+, B4++,... ) спектрi қ ұ рылымы бойынша сутегi спектрiне ұ қ сас, сызық тардың толқ ын ұ зындығ ында ғ ана айырмашылық болады. Не+, Li2+,... қ атарында ядро заряды ө скен кезде жалғ ыз электрон мен ядро арасындағ ы байланыс энергиясы артады да осығ ан сә йкес энергиясы ө седi. Сондық тан ионның заряды неғ ұ рлым ү лкен болса соғ ұ рлым оның дең гейлерiнiң ара қ ашық тығ ы ү лкен, ал спектрiндегi сызық тардың толқ ын ұ зындығ ы қ ысқ а болады (4. 2-кесте).
4. 2-кесте
| Атом, ион | Е2 дең гейдiң қ озу энергиясы DЕ, эВ | 1-резонанстық сызық тың толқ ын ұ зындығ ы l, нм |
| 1H 2He+ 3Li2+ 4Be3+ 5B4+ | 10, 2 40, 6 91, 4 162, 4 253, 7 | 121, 60 30, 38 13, 50 7, 59 4, 86 |
Сутегi атомынан басқ а элемент атомдарында екi (гелий атомы) жә не одан да кө п электрон болады. Атомның барлық электрондары ә рi ядромен ә рi бiр-бiрiмен ә серлеседi. Оптикалық электрондардың энергиясы бұ лардың ядромен ә серлесу сипатына жә не басқ а электрондармен ә серлесу сипатына тә уелдi болады. Ядромен ә серлесуi, сутегi атомындағ ы сияқ ты, n бас кванттық сан мә нiмен анық талады. Электрондар арасындағ ы ә серлесулер кү рделiә рқ илы. Бұ лар атомдағ ы электрондардың жалпы санына жә не бұ лардың қ андай кү йлерде тұ рғ анына тә уелдi болады. Мә селен, ә ртү рлi электронаралық ә серлесу салдарынан n мә нi бiрдей электрондардың энергиясы бұ лардың қ андай кү йде - s, p, d, f (яғ ни бұ лардың ℓ орбиталық кванттық сандары қ андай болуына қ арай) кү йде болғ андық тарына қ арай ә ртү рлi болады. Мысалы, алюминий атомында (13Al - 1s22s2p63s2p1) 3s2 оптикалық электрондардың энергиясы 3p1 электрон энергиясынан тө мен болады. Бұ дан басқ а алюминийдiң ә р тү рлi атомдарындағ ы 3p-кү йдегi электрон спиндiк кванттық санының мә нims=1/2 немесе ms=-1/2 болуына байланысты, айырмашылығ ы аз болса да, ә р тү рлi энергияғ а ие болады.
Сонымен, кө п электронды атомдардағ ы электрондар арасында ә серлесудiң болуы оптикалық электрондардың мү мкiн энергетикалық кү йлер санының кө беюiне, демек атомның энергетикалық дең гейлерi санының кө беюiне ә келiп соғ ады.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|