
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
«Бейорганикалық химия» пәнінен 7 страница
E) SiO2 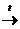
F) FeSO4 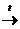
G) Na2O3 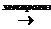
H) P2O5 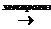
119$$$. Зертханада хлорды мына реакция бойынша алады:
A) HCl(конц) + MnO2 →
B) HCl + KMnO4 →
C) NaCl(раствор) 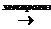
D) HClO →
E) HCl + KOH + HClO3 →
F) K2MnO4 + NaCl →
G) Ba(ClO3)2 + H2SO4→
H) KClO3 + H2C2O4 Ba(ClO3
120$$$. Fe + H2SO4(конц) →.. реакциясында тү зілетін ө німдер:
A) Fe2(SO4)3
B) SO2
C) H2O
D) Cu3N2
E) SO3
F) H2FeO4
G) FeSO4
H) FeS2
121$$$. Cu + HNO3(суйыт) → …
A) Cu(NO3)2
B) NO
C) H2O
D) Cu3N2
E) NO2
F) Cu(NO2)2
G) N2O4
H) NH3
122$$$. Cu + H2SO4(конц) → … реакциясында тү зілетін ө німдер:
A) CuSO4
B) SO2
C) H2O
D) CuS
E) SO3
F) SO
G) CuH2
H) Н2S
123$$$. Аммоний дихроматының термиялық ыдырауында тү зіледі:
A) N2
B) Cr2O3
C) H2O
D) N2O
E) Cr(OH)3
F) NH2NO3
G) HNO2
H) N2H4
124$$$. Металлдарғ а тә н қ асиет:
A) Электрө ткізгіштік
B) жылуө ткізгіштік
C) майырылғ ыштық
D) Конденсация
E) Кристалдануы
F) бағ ыталғ ыштық
G) қ анық қ ыштық
H) Полярланғ ыштық
125$$$. Металлдарғ а тә н қ асиет:
A) Механикалық беріктігі
B) Жоғ ары балқ у температурасы
C) Жоғ ары беріктілік
D) Сутектік байланыс тү зуі
E) Кристалдануы
F) бағ ыталғ ыштық
G) қ анық қ ыштық
H) Полярланғ ыштық
126$$$. Қ айтымсыз реакция:
A) NH4NO3 → N2O + H2O
B) Fe(OH)3 → Fe2O3 + H2O
C) (NH4)2Cr2O7 → N2 + Cr2O7 + H2O
D) CO + H2 → CO2 + H2
E) 2NO2 → 2NO + O2
F) FeO + CO → Fe + CO2
G) H2 + Br2 → 2HBr
H) CO + H2O → CO2 + H2
127$$$. Қ айтымды реакция:
A) N2 + 3H2 = 3NH2
B) H2 + I2 = 2HI
C) CO + H2 = CO2 + H2
D) NаОH + HCl = NaСl + H2О
E) ВаСl2 + H2SO4 = BaSO4 + HCl
F) KNO3 = KNO2 + O2
G) Hg(NO3)2 + HI = HgI2 + HNO3
H) HNO3 + KOH = KNO3 + H2O
128$$$. Қ айтымды реакция:
A) H2O = H+ + OH-
B) HCO 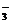 = H+ + CO
= H+ + CO 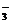
C) 2SO2 + O2 = 2SO3
D) NаОH + HCl = NaСl + H2О
E) ВаСl2 + H2SO4 = BaSO4 + HCl
F) KNO3 = KNO2 + O2
G) Pb(NO3)2 + HI = PbI2 + HNO3
H) HNO3 + KOH = KNO3 + H2O
129$$$. Суда еритін тұ здар:
A) Mg3(PO4)2
B) CaSiO3
C) PbS
D) Ca(CH3COO)2
E) NaF
F) Ba(NO3)2
G) AgCN
H) KCl
130$$$. Суда ерімейтін тұ здар:
A) CaSiO3
B) PbI2
C) HgCl2
D) Ca(CH3COO)2
E) NaF
F) Ba(NO3)2
G) Zn(NO3)2
H) NaCl
131$$$. Суда ерімейтін тұ здар:
A) СuCO3
B) Bi2S3
C) NiS
D) Ca(CH3COO)2
E) NaF
F) Ba(NO3)2
G) Zn(NO3)2
H) NaCl
132$$$. Фосфат-аниондармен тұ нба тү зетін катиондар:
A) Ag+
B) Mg2+
C) Ba2+
D) Na+
E) K+
F) Rb+
G) H+
H) Cs+
133$$$. Катионы, необразующие с фосфат-анионами осадок:
A) K+
B) Rb+
C) Cs+
D) Ag+
E) Mg2+
F) Ba2+
G) Mn7+
H) Fe3+
134$$$. К3[Fe(CN)6] кешенді қ осылысында кешентү зушінің d-орбиталдарының тармақ талу энергиясы жұ птасқ ан энергиядан жоғ ары. Аталғ ан кешен:
A) тө менгіспинді
B)парамагнитті
C)октаэдрлі
D) жоғ арыспинді
E)диамагнитті
F)химиялық белсенді
G)тетраэдрлі
135$$$. Келтірілегн фазалық ауысудан эндотермиялық болатыны:
A) Hg(с) = Hg(г)
B) Na(қ ) = Na(г)
C) SO3(с) = SO3(г)
D) I2(г) = I2(қ )
E) H3PO4(с) = H3PO4(қ )
F) TiCl4(г) = TiCl4(с)
G) H2(г) = Н2(қ )
136$$$. Келтірілегн фазалық ауысудан эндотермиялық болатыны:
A) I2(қ ) = I2(г)
B) S(ромб. ) = S(г)
C) NaOH(қ ) = NaOH(г)
D) H3PO4(с) = H3PO4(қ )
E) TiCl4(г) = TiCl4(с)
F) Hg(г) = Hg(с)
G) H2(г) = Н2(қ )
137$$$. Термодинамика ғ ылыми пә н ретінде:
A)энергияның бір формадан басқ ағ а ауысуы, жү йенің бір бө ліктен басқ ағ а ауысуы
B) химиялық жә не физикалық ү рдістермен жү ретін энергетикалық тиімділік
C) ү рдістердің ө здігінен жү ру бағ ыты мен мү мкіндігі
D) химиялық жә не физикалық ү рдістердің жылдамдығ ы
E)заттардың қ асиеттеріне молеклалар қ ұ рылысының ә сері
F) бейорганикалық жә не органикалық заттар молекуласындағ ы химиялық байланыс табиғ атын
G) электролиттік диссоциация ү рдісі
138$$$. Жү йенің энтропиясы ө седі:
A) Қ атты зат балқ ығ анда
B) Газ таралғ анда
C) Сұ йық тың қ айнау ү рдісінде
D) конденсация кезінде
E) газ сығ ымдалғ анда
F) ерітінділерден кристалғ анда
G) кө лем ұ лғ айғ анда
139$$$. 2NO2(г) = N2O4(г); ∆ H< 0 тепе-тең дік жү йесінде:
A) бастапқ ы заттар жағ ына
B) кө лем ұ лғ аюы жағ ына
C) N2O4 концентрациясының тө мендеуі жағ ына
D) ө нім тү зілу жағ ына
E) кө лем сығ ылу жағ ына
F) N2O4 концентрациясының кө беюі жағ ына
G) ығ ыспайды
140$$$. Реакциялық қ оспағ а катализаторды ендіру:
A) белсендіру энергиясын тө мендетеді
B) химиялық тепе-тең дікке ә сер етпейді
C) тура жә не кері реакциялардың жылдамдығ ын арттырады
D) белсендіру энергиясын арттырады
E) тек тура реакцияның жылдамдығ ын арттырады
F) реакциялардың жылдамдығ ын ө згертпейді
G) тек кері реакцияның жылдамдығ ын тө мендетеді
141$$$. Реакция ө здігінен жү реді, егер:
A) Δ Н < 0
B) Δ S > 0
C) Δ G < 0
D) Δ Н > 0
E) Δ S < 0
F) Δ G > 0
G) Kp = 0
H) Δ G = 0
142$$$. Реакция ө здігінен жү рмейді, егер:
A) Δ Н > 0
B) Δ S < 0
C) Δ G > 0
D) Δ Н < 0
E) Δ S > 0
F) Δ G < 0
G) Δ G = 0
H) 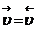

143$$$. 0< Δ Н; FeCl3 + 3KSCN = Fe(SCN)3 + 3KCl; Δ Н< 0 реакциясында тепе-тең дік оң жақ қ а ығ ысады, егер:
A) FeCl3 концентрациясын жоғ арылату
B) KSCN концентрациясын жоғ арылату
C) Fe(SCN)3 концентрациясын тө мендету
D) Еріткіш қ осу
E) Қ ышқ ыл қ осу
F) Сілті қ осу
G) Температураны жоғ арылату
H) Қ ысымды жоғ арылату
144$$$. 0< Δ Н; FeCl3 + 3KSCN = Fe(SCN)3 + 3KCl; Δ Н< 0 реакциясында тепе-тең дік сол жақ қ а ығ ысады, егер:
A) КCl концентрациясын жоғ арылату
B) Fe(SCN)3 концентрациясын жоғ арылату
C) Температураны жоғ арылату
D) Еріткіш қ осу
E) Қ ышқ ыл қ осу
F) Сілті қ осу
G) Қ ысымды тө мендету
H) Н2О концентрациясын тө мендету
145$$$. Δ Н= +566 кДж; 2CO + O2 = 2CO2; Δ Н= -566 кДж 0 реакциясында тепе-тең дік оң жақ қ а ығ ысады, егер:
A) O2 концентрациясын жоғ арылату
B) CО концентрациясын жоғ арылату
C) Температураны тө мендету
D) Қ ысымды тө мендету
E) СО2 концентрациясын жоғ арылату
F) Температураны жоғ арылату
G) Реактордың кө лемін ұ лғ айту
H) Ингибитор қ осу
146$$$. Δ Н= -180 кДж; N2 + O2 = 2NO; Δ Н= +180 кДж реакциясында тепе-тең дік оң жақ қ а ығ ысады, егер:
A) O2 концентрациясын жоғ арылату
B) N2 концентрациясын жоғ арылату
C) Температураны жоғ арылату
D) Температураны тө мендету
E) Қ ысымды жоғ арылату
F) NО концентрациясын жоғ арылату
G) Реактордың кө лемін ұ лғ айту
H) Катализатор қ осу
147$$$. Δ Н= +483 кДж; 2Н2 + O2 = 2Н2O; Δ Н= -483 кДж реакциясында тепе-тең дік сол жақ қ а ығ ысады, егер:
A) Н2O концентрациясын жоғ арылату
B) Қ ысымды тө мендету
C) Температураны жоғ арылату
D) Н2O концентрациясын тө мендету
E) Қ ысымды жоғ арылату
F) О2 концентрациясын жоғ арылату
G) Н2 концентрациясын жоғ арылату
148$$$. Қ ысымды жоғ арылату реакцияларда ө німнің шығ ымын жоғ арылатады:
A) 2NO(г) + O2(г) = 2NO2(г)
B) PCl3(г) + Cl2(г) = PCl5(г)
C) 6HF(г) + N2(г) = 2NF3(г) + 3H2(г)
D) ZnS(т) + H2(г) = Zn(т) + H2S(г)
E) 2NO2(г) = 2NO(г) + O2(г)
F) NO2(г) + SO2(г) = SO3(г) + NO(г)
G) C(т) + 2N2O(г) = CO2(г) + 2N2(г)
H) 2Cl2(г) + 2H2O(г) = 4HCl(г) + O2(г)
149$$$. C + CO₂ ↔ 2CO жү йенің тепе-тең дік тұ рақ тысының ө рнектелуін жә не егер CO₂ концентрациясын 4 есе тө мендеткенде жә не жү йеде қ ысымды жоғ арылатқ анда тура реакцияның жылдамдығ ы қ алай ө згеретінін кө рсетің із:
А) 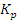
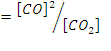
В) 4 есе тө мендейді
C) 2 есе жоғ арылайды
D) Kp=[ CO₂ ][C][ CO₂ ]
E) 0, 25 есе тө мендейді
F) Kp=R[ CO]₂
G) 8 есе жоғ арылайды
H) 3 есе тө мендейді
150$$$. FeCl3+3KCNS=3KCl+Fe(CNS)3 реакциясында KCNS концентрациясын 2, 3, 4 есе жоғ арылату тура реакция жылдамдығ ын ө сіреді:
A) 8 есе
B) 27 есе
C) 81 есе
D) 256 есе
E) 9 есе
F) 15 есе
G) 2 есе
H) 3 есе
151$$$. Температуаны 100, 200, 300 жоғ арылату реакция жылдамдығ ын ө сіреді (ɣ =2):
A) 2
B) 4
C) 8
D) 30
E) 240
F) 2187
G) 6551
H) 16
152$$$. Температуаны 200, 300, 400 жоғ арылату реакция жылдамдығ ын ө сіреді (ɣ =3):
A) 27
B) 81
C) 3
D) 30
E) 40
F) 240
G) 2187
153$$$. Температуаны 200, 300, 400 жоғ арылату реакция жылдамдығ ын ө сіреді (ɣ =4):
A) 16
B) 64
C) 256
D) 30
E) 40
F) 1024
G) 4
H) 20
154$$$. Еріген затты еріткішке қ осу мынағ ан алып келеді:
А) ерітіндінің қ айнау температурасын жоғ арылатады
B) еріткіштің қ анық қ ан бу қ ысымын тө мендетеді
C) осмостық қ ысымды кө тереді
D) қ айнау температурасын тө мендетеді
E) қ ату температурасын жоғ арылатады
F) еріткіштің қ анық қ ан бу қ ысымын жоғ арылатады тө мендетеді
G) осмостық қ ысымды тө мендетеді
155$$$. рН 6, 2- ге тең ерітіндідегі [H⁺ ], [OH⁻ ] жә не судың иондық кө бейтіндісінің мә ні:
A) 6, 3 ∙ 10⁻ 7
B) 1, 6 ∙ 10⁻ 8
C) 10-14
D) 3 ∙ 10⁻ ²
E) 5, 4 ∙ 10⁻ ⁸
F) 4, 5∙ 10-7
G) 4 ∙ 10⁻ ³
H) 10-7
156$$$. 0, 2 М бір негізді ә лсіз қ ышқ ыл етітіндісінің α =0, 03. [H⁺ ], рН жә не Кw мә ндері тең:
A) 6 ∙ 10⁻ ³
B) 2, 22
C) 10⁻ 14
D) 9, 78
E) 3 ∙ 10⁻ ²
F) 5, 4 ∙ 10⁻ ⁸
G) 10⁻ 7
H) 6, 6 ∙ 10⁻ ⁵
157$$$. Кү шті электролиттер:
A) Na2SO4
B) HCl
C) Cu(NO3)2
D) NH4OH
E) CH3COOН
F) HF
G) H2O
H) HNO2
158$$$. Кү шті электролиттер:
A) HNO3
B) HCl
C) HI
D) H2CO3
E) CH3COOH
F) NH4OH
G) H3BO3
H) HNO2
159$$$. Кү шті электролиттер:
A) K2SO4
B) KNO3
C) NaCl
D) H3PO3
E) H2O
F) CH3COOH
G) H2SO3
H) H2C2O4
160$$$. Ә лсіз электролиттер:
A) HCOOH
B) H2SiO3
C) H2S
D) HNO3
E) H2SO4
F) Al(NO3)3
G) HI
H) HCl
161$$$. Ә лсіз электролиттер:
A) HNO2
B) H3BO3
C) H3PO3
D) HClO4
E) H2SO4
F) HNO3
G) HCl
H) HI
162$$$. Ә лсіз электролиттер:
A) H2S
B) H2SO3
C) H2CO3
D) KNO3
E) NaNO3
F) Na2SO4
G) KCl
H) NaCl
163$$$. Ә лсіз қ ышқ ыл тұ здары:
A) KCN
B) Na2C2O4
C) K2SO3
D) KI
E) NaCl
F) Ca(NO3)2
G) CuSO4
H) ZnSO4
164$$$. Ә лсіз қ ышқ ыл тұ здары:
A) Na2B4O7
B) CH3COONa
C) K2S
D) KNO3
E) KI
F) K2SO4
G) NaClO4
H) KClO4
165$$$. рН > 7 тұ здар ерітінділерінде:
A) Na3PO4
B) K2CO3
C) LiNO2
D) CrCl₃
E) MnSO₄
F) Cr(NO₃ )₃
G) MnCl₂
H) FeSO₄
166$$$. рН > 7 тұ здар ерітінділерінде:
A) NaH2PO4
B) KHCO3
C) LiCN
D) CrCl₃
E) MnSO₄
F) Cr(NO₃ )₃
G) FeSO₄
H) ZnCl2
167$$$. рН < 7 тұ здар ерітінділерінде:
A) ZnCl2
B) MnSO4
C) Fe(NO3)2
D) Na3PO4
E) K2CO3
F) LiNO2
G) Na2SO3
H) Rb2SiO3
168$$$. рН < 7 тұ здар ерітінділерінде:
A) Zn(NO3)2
B) FeSO4
C) FeCl3
D) Na3PO4
E) K2CO3
F) LiNO2
G) Na2SO3
H) Rb2SiO3
169$$$. рН = 7 тұ здар ерітінділерінде:
A) KNO3
B) Li2SO4
C) NaCl
D) Rb2SiO3
E) ZnCl2
F) MnSO4
G) Fe(NO3)2
H) Na3PO4
170$$$. рН = 7 тұ здар ерітінділерінде:
A) Rb2SO4
B) NaCl
C) KNO3
D) ZnCl2
E) MnSO4
F) Fe(NO3)2
G) Na3PO4
H) K2CO3
171$$$. FeCl3 гидролизі кү шейеді:
A) Сілті қ осқ анда
B) Температурны жоғ арылатқ анда
C) FeCl3 концентрациясын жоғ арылатқ анда
D) Қ ысымды жоғ арылатқ анда
E) Катализаторды қ осқ анда
F) Қ ышқ ылды қ осқ анда
G) Ингибиторды қ осқ анда
H) Гидролиз ұ зақ тығ ын арттырғ анда
172$$$. Na2CO3 гидролизі кү шейеді:
A) Қ ышқ ылды қ осқ анда
B) Температурны жоғ арылатқ анда
C) Na2CO3 концентрациясын жоғ арылатқ анда
D) Қ ысымды жоғ арылатқ анда
E) Катализаторды қ осқ анда
F) Сілті қ осқ анда
G) Ингибиторды қ осқ анда
H) Гидролиз ұ зақ тығ ын арттырғ анда
173$$$. FeCl3 гидролизі ә лсірейді:
A) Қ ышқ ылды қ осқ анда
B) FeCl3 концентрациясын тө мендеткенде
C) Температурны тө мендеткенде
D) Қ ысымды жоғ арылатқ анда
E) Катализаторды қ осқ анда
F) Сілті қ осқ анда
G) Ингибиторды қ осқ анда
H) Гидролиз ұ зақ тығ ын арттырғ анда
174$$$. Al(NO3)3 гидролизі ә лсірейді:
A) Қ ышқ ылды қ осқ анда
B) Al(NO3)3 концентрациясын тө мендеткенде
C) Температурны тө мендеткенде
D) Қ ысымды жоғ арылатқ анда
E) Катализаторды қ осқ анда
F) Сілті қ осқ анда
G) Ингибиторды қ осқ анда
H) Гидролиз ұ зақ тығ ын арттырғ анда
175$$$. Сірке қ ышқ ылының диссоциациялану тұ рақ тысы 1, 8 ∙ 10⁻ 5 . 0, 1 М калий ацетаты ерітіндісінде гидролиздену тұ рақ тысы, гидролиздену дә режесі жә не [OH-] тең:
A) 5, 56 ∙ 10-10
B) 7, 5 ∙ 10⁻ ⁵
C) 7, 5 ∙ 10⁻ 6
D) 9, 59 ∙ 10⁻ 3
E) 6, 8 ∙ 10⁻ 6
F) 4, 5 ∙ 10⁻ ⁴;
G) 8, 33; 2, 1 ∙ 10⁻ ¹
H) 2, 1 ∙ 10⁻ ¹
176$$$. Қ ышқ ыл орта мына тұ здар ерітінділерінде:
A) NH4Cl
B) FeCl2
C) Cu SO4
D) NaCH3COO
E) Na2СО3
F) NaCl
G) K2S
H) Са(NO2)2
177$$$. Сілтілік орта мына тұ здар ерітінділерінде:
A) Nа 2S
B) K2CO3
C) Na2SO3
D) NaNO3
E) KCl
F) Na2SO4
G) KI
H) KNO3
178$$$. Сулы ерітінділерінде гидролизденеді:
A) натрий сульфиті
B) натрий сульфиді
C) натрий нитриті
D) натрий нитраты
E) натрий хлориді
F) сульфат натрия
G) калий сульфаты
179$$$. Сулы ерітінділерінде қ айтымсыз гидролизденеді:
A) алюминий сульфиді
B) фосфор (V) хлориді
C) бор хлориді
D) натрий фосфаты
E) цезий нитраты
F) темір (III) нитраты
G) калий сульфаты
180$$$. Тек тотық тырғ ыш қ асиет кө рсетеді:
A) KMnO4
B) K2Cr2O7
C) HNO3
D) MnO₂
E) FeSO₄
F) NaH
G) Ca(NO2)2
181$$$. Тек тотық тырғ ыш қ асиет кө рсетеді:
A) HNO3
B) K2CrO4
C) H2O2
D) MnO2
E) Cr2(SO4)3
F) KNO2
G) FeSO4
182$$$. Тек тотық сыздандырғ ыш қ асиет кө рсетеді:
A) K2S
B) FeSO4
C) HCl
D) H2Cr2O7
E) K2MnO4
F) PbO2
G) HNO3
H) H2SO4(конц)
183$$$. Тек тотық сыздандырғ ыш қ асиет кө рсетеді:
A) H2S
B) Mg
C) CO
D) MnCl2
E) Cr(NO2)2
F) HCl
G) Pb
H) CO
184$$$. Тотық тырғ ыштық -тотық сыздандырғ ыштық қ асиет кө рсетеді:
A) MnO2
B) Cr2(SO4)3
C) H2O2
D) Na2S
E) CO2
F) Mn(NO3)2
G) K2FeO4
H) HclO
185$$$. Молекулаішілік тотығ у-тотық сыздану реакциясы:
A) (NH4)2Cr2O7 = N2 + Cr2O3 + 4H2O
B) 2Cu(NO3)2 = 2CuO + 4NO2 + O2
C) CH4 = C + 2H2
D) P + 5HNO3 = H3PO4 + 5NO2 + H2O
E) PCl3 + Cl2 = PCl5
F) KOH + HCl = KCl + H2O
G) 2Na + 2H2O = 2NaOH + H2
H) 2Al(OH)3 = Al2O3 + 3H2O
186$$$. Молекулаішілік тотығ у-тотық сыздану реакциясы:
A) 3AuF = AuF3 + 2Au
B) 2KMnO4 = K2MnO4 + MnO2 + O2
C) 2KNO3 = 2KNO2 + O2
D) CaCO3 = CaO + CO2
E) 2Fe(OH)3 = Fe2O3 + 3H2O
F) Zn + HCl → ZnCl₂ +H₂
G) CH₄ + H₂ O→ CO + H₂
H) CO + H₂ O→ CO + H₂
187$$$. Диспропорциялану реакциясы:
A) 3S + 6NaOH = 2Na2S + Na2SO3 + 3H2O
B) 2NO2 + H2O = HNO3 + HNO2
C) 3H2MnO4 = MnO2 + 2HMnO4 + 2H2O
D) (NH4)2Cr2O7 = N2 + Cr2O3 + 4H2O
E) 2Al(OH)3 = Al2O3 + 3H2O
F) C + O2 + H2O = CO + H2
G) KOH + HCl = KCl + H2O
H) 2KNO3 = 2KNO2 + O2
188$$$. Диспропорциялану реакциясы:
A) 3CrO2 = Cr2O3 + CrO3
B) 4KClO3 = KCl + 3KClO4
C) NH4NO2 = N2 + 2H2O
D) CH4 + H2O = CO + H2
E) CO + H2O = CO + H2
F) 2H2O = 2H2 + O2
G) 2Al(OH)3 = Al2O3 + 3H2O
H) CaCO3 = CaO + CO2
189$$$. Азот мына қ осылыстарда теріс тотығ у дә режесін кө рсетеді:
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|