
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
«Бейорганикалық химия» пәнінен 3 страница
E) J2 тү зілу жағ ына
165$. Егер 2SO2 + O2 = 2SO3, [SO2]=0. 04, [SO3]=0. 02, [O2]=0. 06 тепе-тең дік концентрациясы тең болса, жү йедегі тепе-тең дік константасын кө рсет:
A) 4, 17
B) 25, 2
C) 44, 2
D) 8, 2
E) 5, 5
166$. Тепе-тең дікте тұ рғ ан жү йеде катализатор ендірсе:
A) тепе-тең дік кү йге ә сер етпейді
B)экзотермиялық реакция жағ ына ығ ыстырады
C) эндотермиялық реакция жағ ына ығ ыстырады
D) реакция ө німдері жағ ына ығ ыстырады
E) бастапқ ы заттар жағ ына ығ ыстырады
167$. k1 жә не k2 – тура жә не кері химиялық реакциялардың жылдамдық константасы 
Химиялық тепе-тең дік кү йіне жеткен кезінде тепе-тең дік тұ рақ тысы К =... :
A) k1/k2
B) k1 - k2
C) k2 - k1
D) k1+ k2
E) k2/k1
168$. Тепе-тең дік кү йдегі жү йелердің жә не қ ысымды кө теру кезінде тепе-тең діктің ығ ысуы мен бағ ытталуы арасындағ ы сә йкестікті анық таң дар
| N2O(г) + C(графит) = N2(г) + CO2(г) | |
| H2(г) + Cl2(г) = 2HCl(г) | |
| N2(г) + 2C(граф. ) = C2N2(г) | |
| 3Fe(тв) + 4H2O(ж) = Fe3O4(тв) + 4H2(г) | |
| 3H2(г) + N2(г) = 2NH3(г) |
A) 1-солғ а, 2-қ ысым ә сер етпейді, 3-қ ысым ә сер етпейді, 4-солғ а, 5-оң ғ а
B) 1- қ ысым ә сер етпейді, 2-солғ а, 3-қ ысым ә сер етпейді, 4-оң ғ а, 5-солғ а
C) 1-солғ а, 2-оң ғ а, 3-қ ысым ә сер етпейді, 4-қ ысым ә сер етпейді, 5-қ ысым ә сер етпейді
D) 1-оң ғ а, 2-солғ а, 3- қ ысым ә сер етпейді, 4-қ ысым ә сер етпейді, 5- қ ысым ә сер етпейді
E) 1-қ ысым ә сер етпейді, 2-қ ысым ә сер етпейді, 3-оң ғ а, 4-солғ а, 5-оң ғ а
169$. 2SO2(г) + O2(г) = 2SO3(г) реакциясы V2O5 қ атысында жү реді. Бұ л реакция мынаның мысалы:
A) гетерогенді катализдің
B) гомогенді катализдің
C) каталитикалық емес реакцияның
D) қ ышқ ылды-негізді катализдің
E) тізбекті реакция
170$. Тепе-тең дік тұ рақ тысының физикалық мә ні (Кр):
A) Кр жоғ алы болғ ан сайын, реакция ө німнің шығ ымы жоғ ары
B) Кр жоғ ары болғ ан сайын, реакция ө німдері шығ ымы тө мен болады
C) Кр тө мен болғ ан сайын, реакция ө німдері шығ ымы жоғ ары болады
D) Кр тө мен болғ ан сайын, химиялық реакция жылдамдығ ы жоғ ары
E) Кр тө мен болғ ан сайын, химиялық реакция жылдамдығ ы тө мен
171$. Химиялық тепе-тең дік кү йдегі Гиббс энергиясының ө згерісі:
A) G=0
B) G> > 0
C) G < < 0
D) G > 0
E) G < 0
172$. Стандартты Гиббс энергиясының ө згерісі мен байланысты химиялық тепе-тең дік тұ рақ тысының қ атынасы 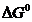 =... :
=... :
A) -RT lnK
B) R lnK
C) -R lgK
D) RT lgK
E) -RT lgK
173$. Ә детте гетерогенді катализ фазалардың беттік шекарасында жү реді:
А) қ атты- сұ йық немесе қ атты- газ
В) қ атты-қ атты
С) сұ йық -сұ йық
D) газ-газ
Е) қ атты-сұ йық немесе газ-газ
174$. Ерітіндінің молярлығ ы-бұ л сан:
A) 1 кг еріткіште еріген заттың молі
B) 1 кг ерітіндіде еріген заттың молі
C) 1 мл ерітіндіде еріген заттың грамы
D) 1 л еріткіште еріген зат молі
E) 1 л ерітіндіде еріген зат молі
175$. 1 мл ерітіндіде еріген заттың грамм саны –бұ л:
A) титр
B) мольдік ү лес
C) массалық ү лес
D) моляльдық
E) мольдік
176$. Ерітіндінің молярлығ ы-бұ л сан:
A) 1 л ерітіндіде еріген заттың молі
B) 1 кг ерітіндіде еріген заттың молі
C) 1 мл ерітіндіде еріген заттың грамы
D) 1 л еріткіште еріген заттың молі
E) 1 кг еріткіште еріген заттың молі
177$. Ерітіндінің нормальдылығ ы-бұ л сан:
A) 1 л ерітіндіде еріген зат эквивалентінің молі
B) 1 кг ерітіндіде еріген заттың молі
C) 1 мл ерітіндіде еріген заттың грамы
D) 1 л еріткіште еріген заттың молі
E) 1 кг еріткіште еріген заттың молі
178$. Температура жоғ арылағ анда газдардың суда ерігіштігі:
A ) тө мендейді
B) ө згермейді
C) максимум арқ ылы ө теді
D) минимум арқ ылы ө теді
E) газ табиғ атына тә уелді ә ртү рлі ө згереді
179$. Қ ысымды жоғ арылатқ анда газдардың суда ерігіштігі:
A) артады
B) ө згермейді
C) максимумнан ө теді
D) минимумнан ө теді
E) газ табиғ атына тә уелді ә ртү рлі ө згереді
180$. Ерітінді бетіндегі қ анық қ ан бу қ ысымы:
A) таза ерітінді бетінен тө мен
B) еріген зат табиғ атына тә уелді жоғ арылайды немесе тө мендейді
C) еріткіш табиғ атына тә уелді жоғ арылайды немесе тө мендейді
D) концентрацияғ а тә уелді жоғ арылайды немесе тө мендейді
E) температурағ а тә уелді жоғ арылайды немесе тө мендейді
181$. Ерітіндінің қ айнау температурасы:
A) еріткіштің қ айнау температурасынан жоғ ары
B) еріткіштің қ айнау температурасынан тө мен
C) еріткіштің қ айнау температурасына тең
D) еріткіш табиғ атына тә уелді ә ртү рлі ө згереді
E) еріген зат табиғ атына тә уелді ә ртү рлі ө згереді
182$. Раульдің бірінші заң ына сә йкес:
A) (po- p1)/po = N1
B) ∆ tкип = Еm
C) ∆ tкрист = Кm
D) pосм. = C(x)RT
E) pосм. = iC(x)RT
183$. Вант-Гоффтың заң ына сә йкес:
A) pосм. = C(x)RT
B) ∆ tкип = Еm
C) ∆ tкрист = Кm
D) (po- p1)/po = N1
E) pосм. = iC(x)RT
184$. Тұ з ерітінділерін қ осқ ан кезде газ жә не сұ йық тың суда ерігіштігінің тө мендеуі былай аталады:
A) тұ зсыздандыру
B) осмоспен
C) экстракциямен
D) сілтісіздендіру
E) кристалданумен
185$. 0, 03 М темірдің (III) сульфаты ерітіндісіндегі сульфат иондардың концентрациясы тең :
A) 0, 09 моль/л
D) 0, 01 моль/л
C) 0, 02 моль/л
D) 0, 03 моль/л
E) 0, 06 моль/л
186$. 0, 02 М бірнегізді ә лсіз қ ышқ ылдың диссоциация дә режесі 3 %. -і қ ұ райды. Осы қ ышқ ылдың диссоциация тұ рақ тысы:
A)1, 8*10-5
B)3, 0*10-3
C)2, 0*10-4
D)6, 0*10-4
E)1, 2*10-5
187$. Электролиттер-дегеніміз:
A) ерітінділерінде иондарғ а ыдырайды
B) электр тогын ө ткізбейді
C) реакция жылдамдығ ын тө мендетеді
D) реакция жылдамдығ ын кө тереді
E) ерімейтін тұ нба тү зеді
188$. Электролиттік диссоциация –бұ л:
A) ерітінді молекулаларының ә серінен электролит молекулаларының иондарғ а ыдырауы
B) электр тогы ә серінен электролит молекуласының иондарғ а ыдырауы
C) тотық тырғ ыштағ ы электрондардың қ осылуы
D) Тотық сыздандырғ ышқ а электрондардың берілуі
E) электролиттердің иондарғ а ыдырау кезінде жылу сің іруі
189$. Диссоциациялану дә режесі-бұ л:
A) иондарғ а ыдырағ ан молекула санының еріген молекулалардың жалпы санына қ атынасы
B) электролиттер молекуласының 100% ыдырағ ан иондар саны
C) диссоциацияғ а ұ шырамағ ан электролит молекуласының саны
D) еріген электролит молекулалар санының иондар тү зген санғ а қ атынасы
E) электролиттің еріген зат массасының ерітінді массасына қ атынасы
190$. Электролиттік диссоциация тұ рақ тысы (Кд) анық тайды:
A) ә лсіз электролит кү шін
B) реакция ө німінің шығ ымын
C) кү шті электролит кү шін
D) иондардың тү зілу жылдамдығ ын
E) иондардың диссоциациялану жылдамдығ ын
191$. рН + рOH қ осындысы тең:
A) 14
B) 10
C) 12
D) 8
E) 6
192$. Судың иондық кө бейтіндісі:
A) КВ = [H+][OH-]
B) КВ = 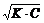
C) КВ = [H+]-[OH-]
D) КВ = 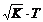
E) КВ = [H+]+[OH-]
193$. Ортаның сутектік кө рсеткіші тең:
A) рН = -lg[H+]
B) рН = [H+]+[OH-]
C) рН = -lg[OH-]
D) рН =[OH-]-[H+]
E) рН=[H+][OH-]
194$. Ә лсіз электролиттің диссрциациялану дә режесі мен диссоциациялану тұ рақ тысы арасындағ ы тә уелділік:
A) a= 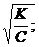
B) DG=-RTlnK
C) a= 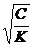 ;
;
D) a= 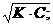
E) a= 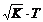
195$. Кальций сульфатының қ анық қ ан ерітіндісі тепе-тең дік
CaSO4(тв)↔ Ca2+ (р) + SO42- (р)
Кальций сульфатының еріткіштік кө бейтіндісі тең:
А) ПР CaSO4=[ Ca2+]·[ SO42-]
В) ПР CaSO4=[ Ca2+]
С) ПР CaSO4=[ SO42-]
D) ПР CaSO4=[ Ca2+]2·[ SO42-]2
Е) ПР CaSO4=[ Ca2+]3·[ SO42-]3
196$. 20°C-та кальций сульфатының еріткіштігі 1, 5·10-2 моль/л. Тең. Бұ л тұ здың еріткіштік кө бейтіндісі:
А) 2, 25·10-4
В) 1, 5·10-2
С) 4, 5·10-4
D) 4, 5·10-8
Е) 2, 25·10-8
197$. ЕКPbS= 1·10-28.
PbS(тв)↔ Pb2+(р) + S2-(р) литрдегі мольге шақ қ анда тұ здың ерігіштігі:
А) қ орғ асын сульфатының еріткіштігі 1·10-14 моль/л
В) қ орғ асын сульфатының еріткіштігі 2·10-28 моль/л
С) қ орғ асын сульфатының еріткіштігі 1·10-28 моль/л
D) қ орғ асын сульфатының еріткіштігі 1·10-4 моль/л
Е) қ орғ асын сульфатының еріткіштігі 1·10-2 моль/л
198$. Аррениус ұ станымына сә йкес қ ышқ ыл дегеніміз:
А) сулы ерітінділерінде Н+ протонын босататын
В) сулы ерітінділерінде Н- протонын босатанын
С) сулы ерітінділерінде Н+ электронын босататын
D) сулы ерітінділерінде Н-
электронын босататын
Е) сулы ерітінділерінде Н+ нейтрон босататын
199$. Аррениус ұ станымына сә йкес негіз дегеніміз:
А) сулы ерітінділерінде ОН- иондарын босататын
В) сулы ерітінділерінде Н- протонын босататын
С) сулы ерітінділерінде Н+ электронын босататын
D) сулы ерітінділерінде Н- гидроксид ионын босататын
Е) сулы ерітінділерінде ОН+ иондарын босататын
200$. Аррениус анық тамасының шектеулігінің мә ні неде:
А) бір ғ ана еріткішпен-сумен байланысты
В) бір ғ ана еріткішпен байланысты
С) бір ғ ана еріткішпен – аммиакпен байланысты
D) бір ғ ана еріткішпен-этил спиртімен байланысты
Е) бір ғ ана еріткіш-органикалық затпен байланысты
201$. Қ ай зат Льюис қ ышқ ылы жә не Льюис негізі болып табылады: MgO+CO2→
А) MgO – негіз, CO2 – қ ышқ ыл
В) MgO – қ ышқ ыл, CO2 – негіз
С) MgO, CO2 – қ ышқ ыл
D) MgO, CO2 – негіз
Е) MgCO3 – қ ышқ ыл
202$. Қ ай зат Льюис қ ышқ ылы жә не Льюис негізі болып табылады: Na2O+SO2→
А) Na2O – негіз, SO2 - қ ышқ ыл
В) Na2O – қ ышқ ыл, SO2 – негіз
С) Na2O, SO2 – қ ышқ ыл
D) Na2O, SO2 – негіз
Е) Na2CO3 – қ ышқ ыл
203$. Льюис ұ станымына сә йкес қ ышқ ылғ а анық тама бер:
А) қ ышқ ыл-электрон жұ бын беретін акцептор
В) қ ышқ ыл-электрон жұ бын беретін донор
С) қ ышқ ыл-протон беретін акцептор
D) қ ышқ ыл-нейтрон беретін акцептор
Е) қ ышқ ыл-электрон жұ бын беретін донор жә не акцептор
204$. Льюис ұ станымына сә йкес негізге анық тама бер:
А) негіз-электрон жұ бын беретін донор
В) негіз-электрон жұ бын беретін акцептор
С) негіз-протон беретін акцептор
D) негіз-нейтрон беретін акцептор
Е) негіз-электрон жұ бын беретін донор жә не акцептор
205$. Льюис теориясында негіз ретінде алынатын ү рдіс:
А) электрон жұ бының рө лін ерекшелейді
В) нейтронның рө лін ерекшелейді
С) протонның рө лін ерекшелейді
D) электрон жұ бы мен нейтрон рө лін ерекшелейді
Е) электрон жұ бы мен протон рө лін ерекшелейді
206$. Бренстед-Лаури ұ станымы бойынша қ ышқ ыл дегеніміз:
А) протондардың донор босатуғ а қ абілеттілігі
В) электрондардың донор босатуғ а қ абілеті
С) нейтрондардың донор босатуғ а қ абілеті
D) протон мен электрондардың донор босатуғ а қ абілеті
Е)нейтрон мен протондардың донор босатуғ а қ абілеті
207$. Бренстед-Лаури ұ станымы бойынша қ ық ыл дегеніміз:
А) протондардың акцепторлармен қ осылу қ абілеті
В) нейтрондардың акцепторларымен қ осылуғ а қ абілеті
С) электронның акцепторлармен қ осылу қ абілеті
D) протон мен нейтронның акцепторлармен қ осылу қ абілеті
Е) протон мен электронның акцепторлармен қ осылу қ абілеті
208$. Бренстед-Лаури ұ станымы бойынша тұ з дегеніміз:
А) кейбір бейтараптану реакцияларында иондар агрегатын тү зуші
В) қ осылу реакциясында иондар агрегатын тү зуші
С) ыдырау (айырылу) реакциясында иондар агрегатын тү зуші
D) ыдырау жә не қ осылу реакциясында иондар агрегатын тү зуші
Е)орынбасу реакцияларында иондар агрегатын тү зуші
209$. Бренстед-Лаури теориясында негіз ретінде алынғ ан ү рдіс:
А) бір заттан протонның басқ ағ а ауысуы
В)электронның бір заттан басқ ағ а ауысуы
С) нейтронның бір заттан басқ ағ а ауысуы
D) электрон мен нейтронның бір заттан басқ ағ а ауысуы
Е) протон мен нейтронның бір заттан басқ ағ а ауысуы
210$. Бренстед-Лаури теориясы бойынша HCl қ атысында су:
А) су-протондардың акцепторы, яғ ни-негіз болып табылады
В) су-протондардың доноры, яғ ни-негіз болып табылады
С) су-протондар акцепторы, яғ на-қ ышқ ыл болып табылады
D) су-протондар доноры яғ ни қ ышқ ыл болып табылады
Е) су-протондар акцепторы, яғ на негіз жә не қ ышқ ыл болып табылады
211$. Бренстед-Лаури теориясы бойынша аммиактың қ атысында басталды:
А) су-протондар доноры яғ ни қ ышқ ыл болып табылады
В) су-протондар доноры яғ ни негіз болып табылады
С) су-протондар акцепторы, яғ на-қ ышқ ыл болып табылады
D) су-протондар доноры яғ ни қ ышқ ыл болып табылады
Е) су-протондар акцепторы, яғ на негіз жә не қ ышқ ыл болып табылады
212$. AlCl3 гидролизінің II-сатысы бойынша қ ысқ артылғ ан иондар тең деуі:
A) (AlOH)2+ + H2O [Al(OH)2]+ + H+
B) Al3+ + H2O = (AlOH)2+ + H+
C) Al3+ + 2H2O = (Al(OH)2)+ + 2H+
D) Al3+ + 3H2O = Al(OH)3 + 3H+
E)[Al(OH)2]+ + H2O = Al(OH)3 + H+
213$. Тұ здардың гидролиздену дә режесіне ә сер ететін факторлар:
A) температура, концентрация
B) қ ысым кПа, температура
C) ыдыстың пішіні
D) ерітіндінің тү сі
E) элементтің мө лдір емес коэффициенті.
214$. 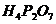 молекуласындағ ы фосфор атомының тотығ у дә режесі
молекуласындағ ы фосфор атомының тотығ у дә режесі
A) +5
B) +1
C) +2
D) +3
E) +6
215$. 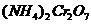 молекуласындағ ы азоттың тотығ у дә режесі:
молекуласындағ ы азоттың тотығ у дә режесі:
A) -3
B) -2
C) -1
D) +1
E) +2
216$. Ванадий оксидтеріндегі ванадийдің тотығ у дә режесі тө мендеу ретімен орналастыр:
A) V2O5, VO2, V2O3, VO
B) VO2, V2O3, V2O5, VO
C) V2O3, VO, V2O5, VO2
D) VO, V2O5, VO2, V2O3
E) VO2, V2O5, V2O3, VO
217 $. Хлор оксидтеріндегі хлордың тотығ у дә режесі ө су ретімен орналастыр:
A) Cl2O, ClO2, Cl2O6, Cl2O7
B) ClO2, Cl2O6, Cl2O7, Cl2O,
C) Cl2O6, Cl2O7, ClO2, Cl2O
D) Cl2O7, Cl2O, ClO2, Cl2O6
E) ClO2, Cl2O6, Cl2O, Cl2O7
218$. Н3РО3 молекуласындағ ы фосфор атомының валенттілігі:
A) III
B) II
C) I
D) IV
E) V
219$. Азот қ осылыстарының NF3, NH3, NH2OH, N2H4 формулаларының азоттың тотығ у дә режесіне сә йкестігі:
A) +3, -3, -1, -2
B) -2, +2, +4, +3
C) +5, +4, +1, -3
D) +4, -4, +2, -2
E) -7, -5, +5, -1
220$. Оттегі қ осылыстарының H2O, F2O2, O2, H2O2 формулаларының оттегінің тотығ у дә режесіне сә йкестігі:
A) -2, +1, 0, -1
B) -2, +2, +4, +3
C) +5, +4, +1, -3
D) +4, -4, +2, -2
E) -7, -5, +5, -1
221$. Мына реакцияда 3K2SO3 + K2Cr2O7 + 4H2SO4 = 3K2SO4 + Cr2(SO4)3 + 4H2O тотық тырғ ыштың эквиваленттік факторы:
A) 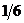
B) 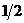
C) 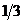
D) 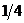
E) 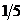
222$. Мына реакцияда 2H2S + SO2 = 3S + 2H2O тотық сыздандырғ ыштың эквиваленттік факторы:
A) 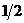
B) 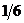
C) 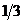
D) 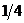
E) 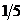
223$. Химиялық реакцияда стехиометриялық коэффициенттерді қ ойың дар:
K2S + KMnO4 + H2O ——› S + MnO2 + KOH:
A) 324328
B) 438232
C) 256491
D) 342676
E) 532168
224$. Гальваникалық элементтегі:
A) ТТР энергия электр энергиясына айналады
B) электр энергиясы химиялық энергияғ а айналады
C) электролиттің диссоциациясы жү реді
D) электролиттің ассоциациясы жү реді
E) термохимиялық реакциялар жү реді
225$. Электролиз процесінің негізінде жү реді:
A) тотығ у-тотық сыздану реакциясы
B) қ ышқ ылдардың жә не тұ здардың ыдырау реакциясы
C) қ ышқ ылдардың жә не негіздердің қ осылу реакциясы
D) ТТР электр энергиясына ауысуы
E) Атомның электрон беру реакциясы
226$. Катод – электродында жү ретін процесс:
A) электролит катиондарының тотық сыздануы;
D) электролит аниондарының тотығ уы;
C) электролит молекулаларының ионғ а ыдырауы
D) электролит иондарының молекулағ а ассоциациялануы;
E) элементтің тотығ у дә режесінің ө згеруі.
227$. Анод – электродында жү ретін процесс:
A) электролит анионының тотығ уы;
B) электролит катиондарының тотық сыздануы;
C) электролит молекулаларының ионғ а ыдырауы
D) электролит иондарының молекулағ а ассоциациялануы;
E) элементтің тотығ у дә режесінің ө згеруі.
228$. Инертті анодқ а жатады:
A) графит, платина
B) мырыш, мыс
C) хром, марганец
D) мырыш, хром
E) темір, мырыш
229$. Активті анодқ а жатады:
A) мыс
B) платина
C) неон
D) графит
E) пластмасса
230$. MgCI2 ерітіндісінің электролизі кезінде анодта жү ретін процесс:
A) хлор иондарының тотығ уы
B) магний иондарының тотығ уы
C) су молекуласының тотық сыздануы
D) сутегі иондарының тотық сыздануы
E) оттегі иондарының тотығ уы
231$. KNO3 ерітіндісінің электролизі кезінде катодта жү ретін процесс:
A) су молекуласының тотық сыздануы
B) нитрат–иондарының тотығ уы
C) калий иондарының тотық сыздануы
D) сутегі иондарының тотық сыздануы
E) азот иондарының тотық сыздануы.
232$. Никель хлориді ерітіндісінің электролизі кезінде активті анодта тотығ ады:
A) Ni
B) H+
C) CI-
D) H2O
E) O2
233$. Гальваникалық элементтің ЭҚ К неге тең:
A) ЭДС = jкатод - jанод
B) ЭДС =lg[H+] - lg[OH-]
C) 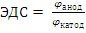
D) 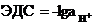
E) 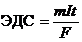
234$. КОН балқ ымасының электролизі кезінде катодта жә не анодта бө лінетін зат:
А) К, О2
В) О2, О2
С) Н2, О2
D) О2, Н2О
Е) К, Н2О
235$. КОН ерітіндісінің электролизі кезінде катодта жә не анодта бө лінетін зат:
А) Н2, О2
В) О2, О2
С) К, О2
D) О2, Н2О
Е) К, Н2О
236$. AlCl3 балқ ымасының электролизі кезінде катодта жә не анодта бө лінетін зат:
А) Al, Cl2
В) Al, О2
С) Al, Н2
D) Н2О, Cl2
Е) Al, Н2О
237$. AlCl3 ерітіндісінің электролизі кезінде катодта жә не анодта бө лінетін зат:
А) Н2, Cl2
В) Al, О2
С) Al, Н2
D) Н2О, Cl2
Е) Al, Н2О
238$. CuSO4 ерітіндісі электролизденгенде 1 сағ ат жә не ток кү ші 4А болғ анда катодта қ анша грамм мыс бө лінеді?
А) 4, 74 гр.
В) 6, 2 гр.
С) 32, 4 гр.
D) 8, 48 гр.
Е) 3, 24 гр.
239$. 5, 3935г кү місті AgNO3 ерітіндісінен ток кү ші 8А болғ анда бө ліп алу ү шін қ анша уақ ыт қ ажет?
А) 603 сек.
В) 60 сек.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|