
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
«Бейорганикалық химия» пәнінен 6 страница
A) 6
B)10
C)14
D) 2
E) 8
F) 32
G) 16
H) 13
29$$$. 3d, 5f, 2s энергетикалық дең гейшелерде максимал электрон сандары:
A) 10
B) 14
C) 2
D) 18
E) 24
F) 32
G) 16
H) 13
30$$$. 1s орбиталдың кү йі квант сандарының жиынтығ ымен анық талады:
A) n = 1
B) l = 0
C) m = 0
D) m = 2
E) l = 4
F) n = 2
G) n = 3
31$$$. 2p орбиталдың кү йі квант сандарының жиынтығ ымен анық талады:
A) n = 2
B) l = 1
B) m = +1, 0, -1
C) m = 0
D) m = -2, 0, +2
E) l = 4
F) n = 1
G) n = 3
32$$$. 3d орбиталдың кү йі квант сандарының жиынтығ ымен анық талады:
A) n=3
B) l=2
C) m=-2, -1, 0, +1, +2
D) n=3
E) l=3
F) m = +1, 0, -1
G) m = +3, +2, +1, -1, -2, -3
33$$$. Ү шінші периодта солдан оң ғ а қ арай натрийдан хлорғ а қ арай:
A) атомдардың иондану потенциалы артады
B) электрон қ осылғ ышығ ы артады
C) атомдардың электртерістілігі артады
D) атомдардың иондану потенциалы кемиді
E) электрон қ осылғ ышығ ы тө мендейді
F) атомдар радиустары артады
G) атомдар радиустары кемиді
H) атомдардың электртерістілігі тө мендейді
34$$$. Бериллий топшасы элементтерінде жоғ арыдан тө мен қ арай, берилийден барийге қ арай;
A) атомдардың иондану потенциалы кемиді
B) электрон қ осылғ ышығ ы тө мендейді
C) атомдар радиустары артады
D) увеличение потенциала ионизации
E) электрон қ осылғ ышығ ы артады
F)элементтер радиустары тө мендейді
G) атомдардың электртерістілігі артады
35$$$. Бериллий топшасы элементтерінде жоғ арыдан тө мен қ арай, берилийден барийге қ арай;
A) атомдардың иондану потенциалы кемиді
B) атомдардың электртерістілігі кемиді
C) элементтер радиустары артады
D) атомдардың иондану потенциалы артады
E) электрон қ осылғ ышығ ы артады
F)уменьшение радиусов элементов
G) элементтер радиустары артады
36$$$. Жә й заттар – типтік тотық сыздандырғ ыштар:
A) сутегі
B) кө міртегі
C) магний
D) оттегі
E) озон
F) бром
G) хлор
37$$$. Мына қ атарларда солдан оң ғ а қ арай иондар радиустары ө седі:
A) Al+3, Mg+2, Na+
B) Be+2, Mg+2, Ca+2
C) Cl-, S-2, P-3
D) Na+, Mg+2, Al+3
E) Ca+2, Mg+2, Be+2
F)P-3, S-2, Cl-
G) J-, Cl-, Br-
38$$$. Қ ыздырғ анда термиялыұ тұ рақ сыз жә не жең іл ыдырайды:
A) аммонийдің барлық тү рлері
B) азот қ ышқ ылының барлық тұ здары
C) оттекті қ ышқ ылдардың барлық тұ здары
D) фосфор қ ышқ ылының барлық тұ здары
E) барлық орта тұ здар
F) оттегі молекуласы
G) азот молекуласы
39$$$. sp3, sp2, sp типті гибридтену молекласының кең істіктік қ ұ рылымы:
A) тетраэдр
B) жазық ү шбұ рыш
C) сызық тық
D) жазық квадрат
E) ромб
F) гантель
G) шар
H) алтыбұ рыш
40$$$. АО- дың sp-гибридтенуі молекулаларда:
A) СО2
B) HCN
C) C2H2
D) C2H6
E) H2CO3
F) H2SO4
G) CuCl2
H) HI
41$$$. АО- дың sp-гибридтенуі молекулаларда:
A) BeF2
B) HgCl2
C) CO2
D) C2H4
E) COCl2
F) H2CO3
G) H2SO4
H) CO
42$$$. АО- дың sp2-гибридтенуі молекулаларда:
A) C2H4
B) COCl2
C) H2CO3
D) H2SO4
E) CuCl2
F) C2H6
G) CO
H) CO2
43$$$. АО- дың sp2-гибридтенуі молекулаларда:
A) C6H6
B) BF3
C) H2SiO3
D) СО2
E) HCN
F) C2H2
G) C2H6
44$$$. АО- дың sp3-гибридтенуі молекулаларда:
A) C2H6
B) NH3
C) CCl4
D) C2H4
E) COCl2
F) H2CO3
G) H2SO4
H) H2O
45$$$. АО- дың sp3-гибридтенуі молекулаларда:
A) SiF4
B) CH4
C) NH3
D) H2O
E) SO3
F) P2O5
G) K3[Fe(CN)6]
H) NaAlO2
46$$$. АО- sp, sp2, sp3 – гибридтенуі бар молекулалар:
A) C2H2
B) C2H4
C) CH4
D) FeO
E) NaCl
F) Н2О
G) CO
47$$$. CH4, PCl5 жә не SF6 молекулаларында кө міртектің, фосфор жә не кү кірттің гибридтену тү рі:
A) sp3
B) sp3d
C) sp3d2
D) spd
E) sp
F) sp3d3
G) sp2
H) sp3d4
48$$$. BeCl2 BF3 жә не SF6 молекулаларында бериллий, бор жә не кү кірттің гибридтену тү рі:
A) sp
B) sp2
C) sp3d2
D) sp33d
E) spd
F) spd4
G) sp2d
H) sp3
49$$$. sp-гибридтенуі мына электрон бұ лттарының қ абысуымен тү зіледі:
A) s – s
B) s - px
C) px - px
D) py - py
E) pz - pz
F) d – d
G) d – s
H) pz – d
50$$$. Сызық тық конфигурация мына молеклаларда:
A) СО2
B) BeF2
C) HgCl2
D) NH3
E) H2O
F) SO3
G) P2O5
H) Fe(CN)3
51$$$. Тригональді жазық конфигурация мына молеклаларда:
A) BF3
B) AlCl3
C) GaH3
D) СО2
E) BeF2
F) HgCl2
G) NH3
H) H2O
52$$$. Тетраэдрлік конфигурация мына молеклаларда:
A) SiCl4
B) CH4
C) GeH4
D) C2H4
E) COCl2
F) H2CO3
G) H2SO4
H) CuCl2
53$$$. Сызық тық, тетраэдрлік кең істіктік қ ұ рылым мына молекулаларда:
A) BeCl2
B) CO2
C) CH4
D) H2S
E) H2O
F) BF3
G) PCl5
H) HCl
54$$$. Кө міртек диоксиді молекуласының қ ұ рылысы, σ - жә не π – байланыстарының саны,
кө міртегі атомнының гиридтену тү рі:
A) сызық тық
B) 2σ жә не 2π
C) sp
D) бұ рыштық
E) 2σ жә не 0π
F) sp²
G) sp³
H) тетраэдрлік
55$$$. Коваленттік полюссіз байланыс мына молекулаларда:
A) H2
B) O2
C) СІ2
D) Na2O
E) Mg
F) HCl
G) H2O
H) НІ
56$$$. Полюссіз молекулалар:
A) CO2
B) CH4
C) СF4
D) Н2О
E) NH3
F) N2H4
G) NH2ОН
H) Н2О2
57$$$. Полюссіз молекулалар:
A) F2
B) PF5
C) SiF4
D) H2O
E) NH3
F) HCl
G) S4
58$$$. Коваленттік полюсті байланыс мына молекулаларда:
A) HCl
B) НІ
C) НҒ
D) H2
E) O2
F) СІ2
G) NаСІ
H) Mg
59$$$. Полюсті молекулалар:
A) Н2О
B) NH3
C) N2H4
D) CO2
E) CH4
F) СF4
G) N2
H) Н2
60$$$. Полюсті молекулалар:
A) NH3
B) NH2OH
C) Н2О2
D) CO2
E) CH4
F) СF4
G) С6Н6
H) СF6
61$$$. Полюсті молекулалар:
A) H2O
B) NH3
C) PCl3
D) CO2
E) Cl2
F) NaCl
G) Fe
62$$$. Мына қ осылыстарда ең жоғ арғ ы иондану дә режесі:
A) K-Cl
B) K-I
C) Na-Cl
D) S-H
E) Fe-Cl
F) Zn-Cl
G) Cu-Cl
H) Ag-Cl
63$$$. Мына бө лшектерде донорлы – акцепторлы механизм бойынша байланыс тү зілді:
A) NH 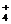
B) ВH 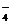
C) H2SiF6
D) GeH4
E) C2H4
F) COCl2
G) H2CO3
H) NH3
64$$$. Молекулалар арасында сутектік байланыс:
A) H2O
B) NH3
C) N2H4
D) HNO3
E) HNO2
F) NaOH
G) CO2
H) KF
65$$$. Молекулалар арасында сутектік байланыс:
A) Н2О2
B) NH3
C) N2H4
D) COCl2
E) H2CO3
F) Cr2O3
G) CrCl2
H) H2SeO3
66$$$. Молекулалар арасында сутектік байланыс:
A) HF
B) NH2ОН
C) Н2О
D) H2SeO3
E) CO2
F) CH4
G) С6Н6
H) СF6
67$$$. Ассоциаттарды тү зуге қ абілетті молекулалар:
A) Суда
B) Аммиак
C) Гидразин
D) Тұ з қ ышқ ылы
E) Кү кірт қ ышқ ылы
F) Натрий гидроксиді
G) Оттегі
H) Метан
68$$$. Донор бола алады:
A) Азот
B) Хлорид-анион
C) Оттегі
D) Бериллий
E) Сутегі
F) Кремний
G) Темір
H) Марганец
69$$$. Акцептор бола алады:
A) Темір
B) Кремний
C) Сутегі
D) Азот
E) Фторид-анион
F) Оттегі
G) Хлорид-анион
H) Карбонил
70$$$. Ковалентті байланыс қ асиеті:
A) бағ ытталуы
B) қ анығ уы
C) полярлығ ы
D) иондану дә режесі
E) диссоциация
F) конденсация
G) кристалдану
H) айдау
71$$$. Азот молекуласында σ - жә не π - байланыстарының саны, байланыс еселігі:
A) 3
B) 1σ
C) 2π
D) 2
E) 3π
F) 2σ
G) 1
72$$$. Оттегі молекуласында σ - жә не π - байланыстарының саны, байланыс еселігі:
A) 2
B) 1σ
C) 1π
D) 3
E) 2π
F) 2σ
G) 1
73$$$. Фтор молекуласында σ - жә не π - байланыстарының саны, байланыс еселігі:
A) 1
B) 1σ
C) 0π
D) 3
E) 1π
F) 2σ
G) 2
74$$$. Хлор молекуласында σ - жә не π - байланыстарының саны, байланыс еселігі:
A) 1
B) 1σ
C) 0π
D) 2
E) 2π
F) 2σ
G) 4
75$$$. ВБ теориясы бойынша кө міртегі (II) оксиді молекуласында:
A) С жә не О атомдарының қ ос байланысы 2р- электрондардың жұ птасуы есебінен тү зіледі
B) біреуі - донорлы-акцепторлы механизм бойынша С бос 2р-орбиталі есебінен, О электрондық жұ бынан
C) ү штік байланыс
D) қ ос байланыс
E) бір байланыс алмасу механизмі бойынша тү зіледі
F) бір байланыс донорлы-акцепторлы механизмі бойынша тү зіледі
G) 1σ - жә не 1π - байланыстары алмасу механизмі бойынша тү зіледі
76$$$. Кө міртегі (IV) оксиді молекуласына тә н:
A) 2π - байланыстар
B) 2σ - байланыстар
C) сызық тық молекула
D) 1σ -, 2π - байланыс
E) тетраэдр
F) sp3-гибридтену
G) sp2-гибридтену
77$$$. Орталық атомының sp –гибридтенуі молекулада:
A) CO2
B) COS
C) CS2
D) CH4
E) COCl2
F) CSCl2
G) H2S
78$$$. Орталық атомының sp2 –гибридтенуі молекулаларда:
A) COCl2
B) CSCl2
C) H2CO3
D) CCl4
E) Cl2
F) C2H2
G) CO2
79$$$. Орталық атомының sp3 –гибридтенуі молекулаларда:
A) CCl4
B) CH4
C) NH3
D) C6H6
E) CO2
F) COCl2
G) BeCl2
80$$$. σ - байланыс электрондық бұ лттардың қ аптасуы кезінде тү зіледі:
A) s - s
B) s - px
C) px - px
D) py - px
E) py - pz
F) pz - pz
G) dx – dx
81$$$. Донорлы-акцепторлы механизм бойынша тү зіледі:
A) 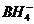
B) 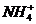
C) 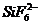
D) 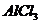
E) 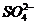
F) 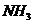
G) 
82$$$. Алмасу механизм бойынша тү зіледі:
A) 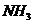
B) 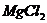
C) 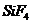
D) 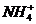
E) 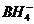
F) 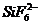
G) 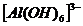
83$$$. σ -байланысына, π - и δ - байланысына, σ - и π - σ - байланысына қ атысады:
A) σ -байланысына s-орбиталдардың электрондары
B) σ - жә не π - байланысына р-орбиталдардың электрондары
C) σ -, π - жә не δ - байланысына d-орбиталдардың электрондары
D) σ - жә не π - байланысына s жә не p -орбиталдардың электрондары
E) σ -, π - жә не δ - байланысына s жә не p -, d-орбиталдардың электрондары
F) σ - байланысына s жә не p -орбиталдардың электрондары
байланысына s жә не p -орбиталдардың электрондары
G) σ -связывании – тек d-орбиталдардың электрондары
84$$$. CH4, NH3, H2O молекулаларының кең істіктік конфигурациясы
A) тетраэдрлік
B) тригональді-пирамидальді
C) бұ рыштық
D) жазық ү шбұ рыштық
E) сызық тық
F) плоскоквадратная
G) тригональді-бипирамидальді
85$$$. H2, СО2, Н2О молекулаларының кең істіктік конфигурациясы
A) гантел тә різді
B) сызық тық
C) бұ рыштық
D) жазық ү шбұ рыштық
E) тетраэдрлік
F) жазық квадратты
G) тригоналді
86$$$. Cl2, SO2, HCN молекулаларының кең істіктік конфигурациясы:
A) гантел тә різді
B) бұ рыштық
C) сызық тық
D) жазық ү шбұ рыштық
E) тетраэдрлік
F) жазық квадратты
G) тригоналді
87$$$. SiF4, PCl3, SiF6 молекулаларының кең істіктік конфигурациясы:
A) тетраэдрлік
B) тригоналді -пирамидалді
C) октаэдрлік
D) жазық ү шбұ рыштық
E) сызық тық
F) бұ рыштық
G) гантел тә різді
88$$$. 1800 бұ рыш молекулаларда:
A) CO2
B) BeCl2
C) HCN
D) H2CO3
E) SiF4
F) SO2
G) NH3
89$$$. Орталық атомның sp-, sp2-, sp3-гибридті орбиталдарының геометриялық пішіні:
A) сызық тық
B) жазық ү шбұ рыштық
C) тетраэдр
D) бұ рыштық
E) октаэдр
F) тригоналді пирамида
G) тригоналді бипирамида
90$$$. Орталық атомның sp-, sp2-, sp3d-гибридті орбиталдарының геометриялық пішіні:
A) сызық тық
B) жазық ү шбұ рыштық
C) тригоналді бипирамида
D) бұ рыштық
E) октаэдр
F) тетраэдр
G) тербелмелі
91$$$. Орталық атомның sp2-, sp3d-, sp3d2 -гибридті орбиталдарының геометриялық пішіні:
A) жазық ү шбұ рышты
B) тригоналді бипирамида
C) октаэдр
D) бұ рышты
E) тетраэдр
F) сызық тық
G) тербелмелі
92$$$. Ковалентті химиялық байланыс мынадай байланыс болып табылады:
A) қ аннық қ ан
B) бағ ытталғ ан
C) берік
D) қ аннық пағ ан
E) бағ ытталмағ ан
F) ә лсіз
G) индукциялық
93$$$. Иондық химиялық байланыс мынадай байланыс болып табылады:
A) бағ ытталмағ ан
B) қ аннық пағ ан
C) берік
D) бағ ытталғ ан
E) қ аннық қ ан
F) ә лсіз
G) индукциялық
94$$$. Мына молекулада валенттік бұ рыш 180о тең:
A) BeCl2
B) CO2
C) XeF2
D) H2O
E) H2S
F) SO2
G) AlCl3
95$$$. Негіздік оксидтер:
A) CaO
B) Na2O
C) K2O
D) P2O5
E) SO3
F) CuO
G) ZnO
H) SO2
96$$$. Кү шті қ ышқ ылдар:
A) H2SO4
B) HCl
C) HNO3
D) H3PO4
E) HNO2
F) H2S
G) H2CO3
H) H3AsO4
97$$$. Ә лсіз қ ышқ ылдар:
A) HNO2
B) H3PO4
C) H2CO3
D) HNO3
E) HClO4
F) HCl
G) HClO3
H) H2SO4
98$$$. Бір негізді қ ышқ ылдар:
A) HCl
B) HI
C) HBr
D) H2CO3
E) H2SO4
F) H3PO4
G) H2SeO4
H) H2CrO7
99$$$. Екі негізді қ ышқ ылдар:
A) H2S
B) H2SO4
C) H2CO3
D) H3PO4
E) HNO3
F) H3AsO4
G) HF
H) HCl
100$$$. Бейтараптану реакциясы:
A) HCl + NaOH = NaCl + H2O
B) 2HCl + Ca(OH)2 = CaCl2 + 2H2O
C) HNO3 + KOH = KNO3 + H2O
D) Fe(OH) 3 = Fe2 O3 + H2O
E) Zn + CuSO4 = ZnSO4 + Cu
F) NH3 + HCl = NH4Cl
G) S + O2 = SO2
H) CaCO3 = CaO + CO2
101$$$. Алмасу реакциясы:
A) AgNO3 + NaCl = AgCl ↓ + NaNO3
B) Na2SO4 + BaCl2= BaSO4↓ + 2NaCl
C) (NH4)2S + ZnCl2 = ZnS↓ + NH4Cl
D) Na + O2 = Na2 O
E) H2SO4 + NaOH = Na2SO4 + H2O
F) Cl2 + Na = NaCl
G) CaCO3 = CaO + CO2
H) S + O2 = SO2
102$$$. Қ осылу реакциясы:
A) NH3 + HCl = NH4Cl
B) S + O2 = SO2
C) Na + O2 = Na2 O
D) 2HCl + Ca(OH)2 = CaCl2 + 2H2O
E) HNO3 + KOH = KNO3 + H2O
F) AgNO3 + NaCl = AgCl + NaNO3
G) Na2SO4 + BaCl2= BaSO4 + 2NaCl
H) CaCO3 = CaO + CO2
103$$$. Ыдырау реакциясы:
A) CaCO3 = CaO + CO2
B) NH4Cl = NH3 + HCl
C) Cu(OH)2 = CuO + H2O
D) S + O2 = SO2
E) Na + O2 = Na2 O
F) HNO3 + KOH = KNO3 + H2O
G) AgNO3 + NaCl = AgCl + NaNO3
H) Zn + CuSO4 = ZnSO4 + Cu
104$$$. Амфотерлі гидроксидтер:
A) Al(OH)3
B) Cr(OH)3
C) Zn(OH)2
D) Fe(OH)2
E) NaOH
F) LiOH
G) Ca(OH)2
105$$$. Амфотерлі гидроксидтер:
A) Be(OH)2
B) Al(OH)3
C) Fe(OH)3
D) NH4OH
E) Mg(OH)2
F) Ba(OH)2
G) Sr(OH)2
H) LiOH
106$$$. Амфотерлі гидроксидтер:
A) Sn(OH)2
B) Zn(OH)2
C) Sb(OH)3
D) Ni(OH)2
E) NaOH
F) KOH
G) Fe(OH)2
107$$$. Қ ышқ ыл тү збейтін оксидтер:
A) NO
B) BaO
C) Ag2O
D) P2O3
E) SО2
F) CO2
G) N2O5
H) Cl2O
108$$$. Кальцийдің дигидрофосфатында фосфордың , кальцийдің, оттегінің массалық ү лесі:
A) 26
B) 27
C) 17
D) 92
E) 64
F) 02
G) 13
H) 86
109$$$. Азот (V) оксидінің 1\4 моль, 1\10 моль, 2 моль салмағ ы:
A) 27 г
B) 10, 8
C) 216г
D) 32г
E) 44г
F) 49г
G) 81г
H) 162г
110$$$. Ерітінділерден мырышты жең іл ығ ыстырады:
A) Кадмий
B) Кобальт
C) Мыс
D) Магний
E) Натрий
F) Калий
G) Алюминий
H) Барий
111$$$. Қ ышқ ылдармен де, сілтілермен де ә рекеттеседі:
A) Мырыш
B) Бериллий
C) Алюминий
D) Натрий
E) Магний
F) Кө міртегі
G) Оттегі
H) Платина
112$$$. Амфотерлі оксидтер:
A) Cr2O3
B) MnO2
C) ZnO
D) Mn2O3
E) CrO3
F) MnO
G) Mn2O7
H) Na2O
113$$$. Мына тұ здардың сулы ерітінділерінің ә рекеттесуінен химиялық реакция жү реді:
A) барий нитраты мен аммоний сульфаты
B) натрий карбонаты мен тұ з қ ышқ ылы
C) калий гидроксиді мен азот қ ышқ ылы
D) калий сульфаты мен рубидий дихроматы
E) барий гидроксиді мен и магний нитраты
F) калий перманганаты мен натрий сульфаты
G) азот қ ышқ ылы мен мыс сульфаты
H) темір нитраты мен тұ з қ ышқ ылы
114$$$. Тотық тырғ ыш емес қ ышқ ылдардан мына металдар сутегін ығ ыстырады:
A) Марганец, темір
B) Мырыш, магний
C) алюминий, галлий
D) Платина, алтын
E) кү міс, қ орғ асын
F) мыс, палладий
G) Молибден, вольфрам
H) Ванадий, тантал
115$$$. Сұ йылтылғ ан кү кірт қ ышқ ылымен ө ң дегенде ерітіндіге айналатын металл қ оспалары:
A) Магний, барий, мырыш
B) Бериллий, қ алайы, хром
C) Марганец, темір, алюминий
D) Скандий, теллур, қ орғ асын
E) Таллий, алюминий, галлий
F) Платина, алтын, кү міс
G) Германий, қ орғ асын, мырыш
H) Цирконий, гафний, натрий
116$$$. Тұ з ерітіндісінен басқ а металды ығ ыстыратын металл;
A) темір + мыс сульфаты (II)
B) мырыш + кү міс нитраты
C) мыс + кү міс нитраты (I)
D) кү міс + сынып нитраты
E) Никель + магний хлориді
F) Хром + алюминий сульфаты
G) Кобальт + кадмий нитраты
H) Кадмий + мырыш сульфаты
117$$$. Суда ерімейтін хлоридтер:
A) СuCl2
B) Hg2Cl2
C) PbCl2
D) NaCl
E) BaCl2
F) MnCl2
G) HgCl2
H) NH4Cl
118$$$. Зертханада оттегін мына реакция бойынша алады:
A) KClO3 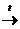
B) KMnO4 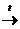
C) NaNO3 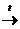
D) SeO2 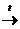
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|