
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Литература.. Вопросы для самоконтроля.. Химическая схема синтеза.
Литература.
1.Г.Дайсон, П.Мей. Химия синтетических лекарственных веществ. Мир. М. 1964., 182 с.
2. З. Гауптман, Ю.Грефе, Х.Ремане. Органическая химия. М.Химия,1979, 832 с.
Вопросы для самоконтроля.
1.Какие значения ПДК имеют исходные вещества для синтезаметиленового синего?
2.Расписать по стадиям и операциям синтез метиленового синего.
3.Haзвать особенности работы с нитритом натрия и объяснить необходимость выдерживания низких (0-4°С) температур.
4.Назвать восстановители, близкие по эффективности цинковой пыли.
5.Объяснить роль натрия тиосульфата.
2.1.1. Получение п-нитрозодиметиланилина.
Оборудование: фарфоровый стакан (250 мл), мешалка, капельная воронка, термометр, баня со льдом, воронка Бюхнера, колба Бунзена.
Реактивы: диметиланилин (м.м. – 150,18; Тпл=85°С), концентрированная соляная кислота, 20% раствор NaNO2.
В стакане, снабженном мешалкой, капельной воронкой и термометром, растворяют при перемешивании 13,3 г диметиланилина в 35млконцентрированной НСl. Раствор охлаждают до 0°Си прибавляют 8,3 г NaN02 в виде20% раствора с такой скоростью, чтобы температура реакционной смеси не превышала 3-4°С. Смесь перемешивают 1час, осадок п-нитрозодиметиланилина отфильтровывают, отжимают и высушивают.
2.1.2. Получение метиленового синего.
В стакане растворяют 12 г нитрозодиметиланилина в 450 мл воды, к этому раствору добавляют 67,5 мл концентрированной НС1 и маленькими порциями вводят цинковую пыль, продолжая энергичное перемешивание. После обесцвечивания раствора избыток соляной кислоты нейтрализуют, добавляя раствор соды дo началa помутнения раствора. Смесь фильтруют. Фильтр переносят в стакан и прибавляют pаствop 22,5 г (Nа2S2O3 • 5H2О) в 90мл воды и 120 г льда. При перемешивании из капельной воронки прибавляют 10%раствор бихромата калия до тех пор, пока проба, нанесенная пипеткой на фильтровальную бумагу не будет оставлять на ней вытек желтого цвета.
Затем смесь переносят в колбу, соединенную с обратным холодильником и прибавляют к ней раствор 9 г диметиланилина в смеси 7 г концентрированной соляной кислоты и 75 мл воды. После этого в течении 40 минут при энергичном перемешивании прибавляют из капельной воронки 180 мл 10% раствора К2Сr2О7 и 75 мл насыщенного раствора хлористого цинка. Эту смесь нагревают на водяной бане при 85-90°С до тех пор, пока окраска не станет синей.
Добавляют 75 г NaCl, 140 мл 22% серной ккислоты и, хорошо перемешав, дают раствору отстоятся. Выпавший темно-синий осадок отфильтровывают и высушивают.
2.2. ПОЛУЧЕНИЕ ОКСОЛИНА.
1,2,3,4-тетрогидро-1,2,3,4-тетрооксонафталинолиногидрат.
|
|
С10Н4О4·2Н2О
Молекулярная масса – 224,17.
Белыйили с кремовым оттенком кристаллический порошок без запаха, легко растворим в ацетоне и воде,мало растворим в эфире, нерастворим в хлороформе, хлорметилене. В щелочной среде быстро темнеет. Хранится в холоде в плотно закрытой склянке из темного стекла. Тпл = 129-133°С.
Оригинальный противовирусный препарат. Обладает вируцилидной активностью, эффективен при вирусных заболеваниях глаз, кожи, ринитах. Окaзываeт профилактическое действие при гриппе.
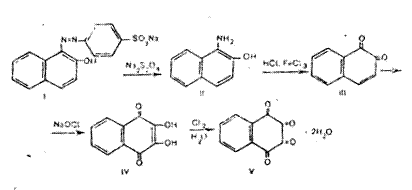
Исходным веществом в синтезе оксолина является натриевая соль 2-гидроксинафталин-1-азобензол-4-сульфокислоты (краситель кислотный оранжевый). Восстановление соли гиддросульфитом натрия в водной даёт 1-аминонафтол-2, который в виде гидрохлорида окисляют хлоридом железа (III) в водной среде до 1,2 нафтохинона. Окисление нафтохинона гипохлоритом натрия приводит к изонафтазарину, окисление которого хлором дает оксолин.
Химическая схема синтеза.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|
