
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Литературный обзор
Литературный обзор
Реакции нуклеофильного замещения в ароматическом кольце.
Существует несколько способов нуклеофильного замещения в ароматическом кольце:
1) Через соли диазония
2) Механизм отщепление-присоединение
3) Механизм присоединение-отщепление
Нуклеофильное замещение через ион диазония
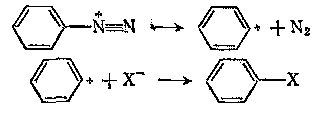
Замещение диазогруппы основано на чрезвычайно хорошей уходящей группе, атоме азота N2. При ее отщеплении образуется арильный катион. Этот катион не очень устойчив, так как свободная орбиталь лежит в плоскости кольца и не участвует в сопряжении, поэтому заряд не делокализован, однако он все-таки образуется, так как отщепляющаяся молекула азота является очень хорошей, устойчивой уходящей группой.[1]
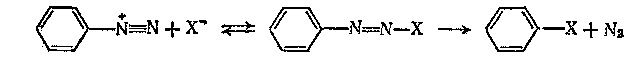
В других реакциях интермедиатом является аддукт нуклеофила и диазониевого иона. Замещение происходит, когда элиминируется азот.
И последним способом является замещение по радикальному типу с переносом электрона, этот механизм наиболее вероятно реализуется в реакциях катализируемых солями меди.[2]
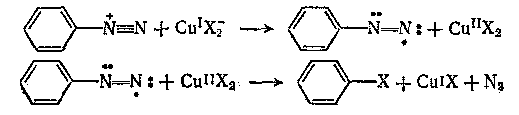
Приведенные механизмы реализуются соответственно в реакциях а) гидролиз арилдиазониевых солей в фенолы, б) реакции арилдиазониевых ионов с N-3 с образованием арилазидов, в) реакция Зандмейера катализируемая хлоридом или бромидом меди(I).
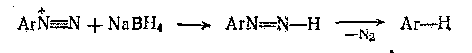
Часто в синтезах полезно применять реакцию замещения на водород. Обычно это используется после введения нитро или аминогруппы для ориентации заместителей. Замену диазогруппы лучше всего проводить реакцией с ортофосфорной кислотой или с боргидридом натрия.
Замещение диазогруппы на галоген является важным способом, так как образуется единственный изомер, в отличии от галогенирования. Фторирование происходит при реакции разложения тетрафторборатов диазония, при их термическом разложении образуется арилфторид.[2]
Нуклеофильное замещение по типу отщепление-присоединение.
Неактивированные арилгалогениды, в которых хотя бы одно из двух орто-положений по отношению к атому галогена не занято заместителем, с сильными нуклеофилами реагируют по механизму, включающему последовательные стадии отщепления и присоединения. Нуклеофил Nu- на первой стадии действует как основание отрывая протон в орто-положении к атому галогена ароматического субстрата. Отщепляется именно орто-протон, поскольку в арилгалогенидах орто-протон самый «кислый». Образовавшийся карбанион быстро выбрасывает анион Hal-, в результате чего образуется незаряженная очень не стабильная частица, которую можно представить в виде бензольного кольца с тройной связью. Этот неустойчивый интермедиат называют дегидробезолом или бензином. На этом заканчивается стадия отщепления.[4]
Отличительным свойством этого механизма является то, что входящий нуклеофил не обязательно присоединяется к тому атому углерода, к которому была присоединена уходящая группа.[2]
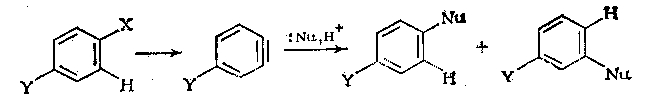
Впервые дегидробензол был обнаружен как интермедиат в реакции хлорбензола с амидом калия. В результате которой 14C метка в исходном веществе распределилась в анилине так, как этого следует ожидать при образовании дегидробензола. Этому механизму способствуют эффекты благоприятствующие уходу водорода из ароматического кольца в виде протона. Присоединение нуклеофилов протекают очень быстро.[2]
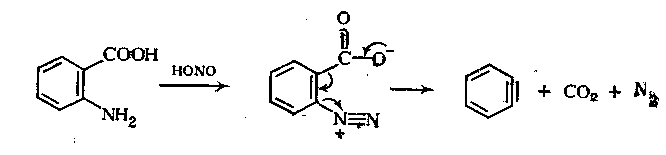
Кроме катализируемого основаниями, существует еще один способ генерирования дегидробензола. Некоторые из них применяются в синтезах. Одним из наиболее приемлемых способов является диазотирование α-амино бензойных кислот. После диазотирования происходит синхронное элиминирование азота и CO2.Образование дегидробензола таким образом возможно в присутствии соединений которые быстро с ним реагируют.[2]
Нуклеофильное замещение по типу присоединение-отщепление.
Присоединение нуклеофила к ароматическому кольцу с последующим отщеплением заместителя приводит к нуклеофильному замещению. Основным энергетическим требованием для протекания этого процесса является образование промежуточного продукта присоединения. Стадия присоединения облегчается электронакцепторными заместителями, поэтому нитроароматические субстраты являются лучшими для нуклеофильного ароматического замещения. Другие акцепторные заместители в меньшей степени повышают реакционную способность. В определенных условиях 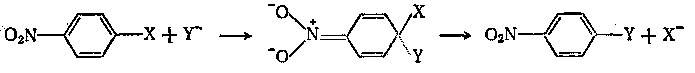
промежуточные аддукты достаточно устойчивы, их называют комплексами Мейзенгеймера.
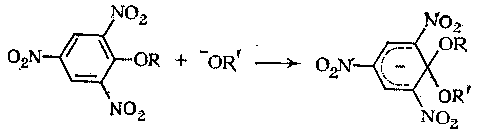
Аддукты, полученные из нитросоединений, сильно окрашены. Хорошими примерами подобных комплексов являются соединения полученные реакцией алкоксильных ионов с алкил-2,4,6-тринитрофениловыми эфирами:
Нуклеофильное замещение протекает через аналогичные интермедиаты, если ароматическое кольцо имеет потенциальную уходящую группу. Наиболее обычным случаем является замещение галогена, но по механизму присоединение-отщепление можно заместить также алкокси-, нитро-, и цианогруппы. Следует заметить, что способность уходящей группы к отщеплению в таких реакциях оказывается иной, чем при нуклеофильном замещении у насыщенного углерода. Например, фтор часто является лучшей уходящей группой в реакциях нуклеофильного ароматического замещения, чем другие галогены.[2]
Нуклеофильное замещение является основным методом введения заместителей в перфторированное ароматическое кольцо. Протекание этих реакций облегчено повышенной электронакцепторностью полифторированного ароматического кольца.[1]
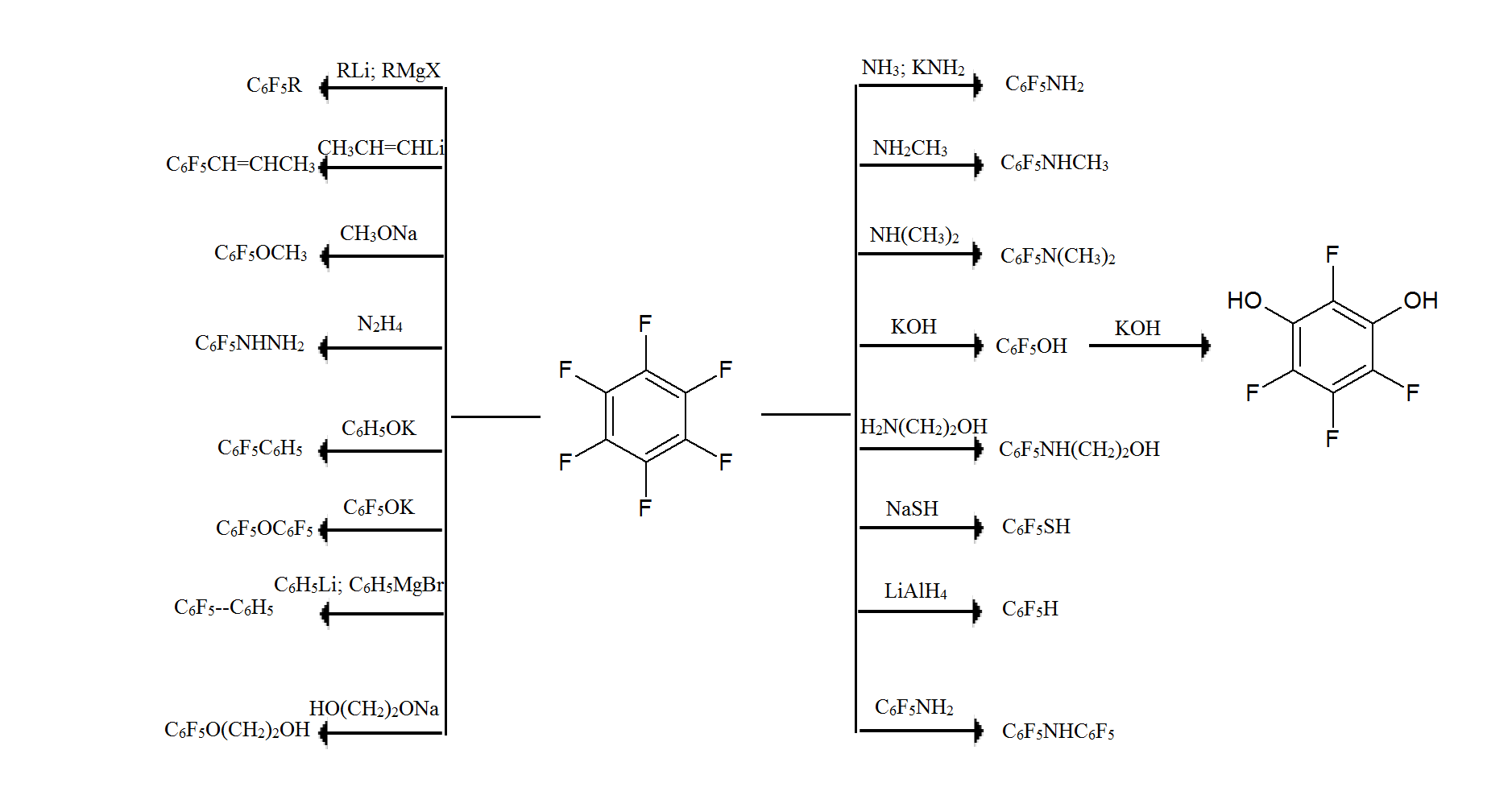
Замена одного атома в гексафторбензоле легко протекает при действии самых различных нуклеофильных агентов. Эти реакции привели к получению большого числа пентафторзамещенных производных бензола с различными функциональными группами.[1]
В общем случае место вступления второго заместителя в соединения типа C6F5X определяется конкуренцией влияния заместителя X и влиянием атомов фтора.
Если X является сильным электрондонорным заместителем, то его влияние может преобладать над влиянием атомов фтора. Так при действии гидроокиси калия на пентафторфенол образуется тетрафторрезорцин, а при действии аммиака на гексафторбензол или пентафторанилин преимущественно тетрафтор-m-фенилендиамин.

В случае других электронодонорных заместителей влияние атомов фтора преобладает и при действии на C6F5X образуются преимущественно пара-изомеры.
При реакции соединений типа C6F5X содержащих электроноакцепторные заместители (X= NO2, SO2CH3, COOCH3 и др.) с нуклеофильными агентами возможно отщепление как в орто-, так и в пара-положениях к заместителю.
В пентафторпроизводных бензола типа C6F5X содержащих электроноакцепторные заместители (X= CF3, C2F5, CN и др.) под действием нуклеофильных агентов отщепляется атом фтора находящийся в пара-положении к заместителю.
При замещение пентафторзамещенных производных бензола типа C6F5X следует также учитывать возможность взаимодействия входящей группы с уже имеющейся. Так например, если находящийся в ароматическом кольце заместитель способен образовывать водородные связи или комплексы донорно-акцепторного типа с атакующим нуклеофилом, то в этом случае большое влияние на направление реакции оказывает растворитель. Можно полагать, что замещение орто-атома фтора происходит через образование циклического переходного состояния. = NO2, COOR, COOH, COR.[5]
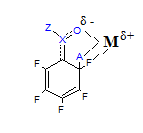

В том случае, когда реакция проводится в малополярных растворителях, преимущественно замещается атом фтора в орто-положении к заместителю. При проведении реакции в полярных растворителях, особенно в диполярных апротонных растворителях, препятствующих образованию циклических переходных состояний, преобладает замещение атома фтора в пара-положении. Это дает возможность управлять реакцией и получать орто- или пара-дизамещенные продукты в зависимости от необходимости.[5]
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|