
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Катионы (мэкв/л) 2 страница
Вне связи с белками железо очень токсично, так как запускает свободно-радикальные реакции с образованием активных форм кислорода.
Выведение
В сутки обычные потери железа составляют 1-2 мг и происходят несколькими путями:
· с желчью
· вместе со слущивающимся эпителием ЖКТ,
· десквамация кожи,
· у женщин детородного возраста – с месячными кровотечениями от 14 до 140 мг/месяц,
· выпадение волос, срезание ногтей.
Существует точная регуляция обмена железа
Основными факторами, влияющими на обмен железа, являются потребности гемопоэза, пищевой фактор и уровень запаса металла в тканях. Количество железа в организме поддерживается тремя основными путями:
1. Регуляция всасывания в кишечнике.
2. Поддержание рециркуляции железа эритроцитов.
3. Регуляция количества поступающего в клетку железа.
Функции гепсидина
Среди белков-регуляторов обмена железа к настоящему времени наиболее хорошо изучен гепсидин, олигопептид из 25 аминокислот. Гепсидин синтезируется в печени при достаточном количестве железа в гепатоците или под действием цитокинов. Действие гепсидина заключается в снижении активности белка ферропортина, отвечающего за выход ионов железа из клетки в кровь:
1. В энтероците действие гепсидина приводит к тому, что большая часть железа остается в клетке, запасается в ферритине и теряется при слущивании кишечного эпителия.
2. При действии гепсидина на макрофаг происходит задержка железа внутри макрофага.
Являясь белком острой фазы, гепсидин повышается при любых воспалительных процессах, протекающих в организме, и при бактериальных инфекциях. Повышение продукции происходит посредством провоспалительных цитокинов, наиболее эффективным из которых является интерлейкин-6. Образующийся избыточный гепсидин, уровень которого может повышаться в сотни раз (!), блокирует выход железа из макрофагов, вызывая тем самым гипоферремию. Недостаток железа в крови приводит к снижению эритропоэза – развивается "анемия воспаления" ("анемия хронических заболеваний").
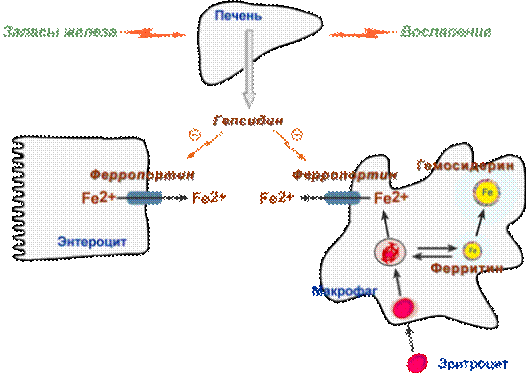
Действие гепсидина на обмен железа
Система IRE/IRP
Система IRE/IRP (англ. iron-responsive element / iron-responsive element-binding proteins, железочувствительный элемент / белок, связывающий железочувствительный элемент) обеспечивает регуляцию поступления железа в клетку
· синтеза рецепторов к трансферрину,
· синтеза ферритина.
Молекулы IRP способны связываться с участком IRE матричной РНК двух белков – рецептора трансферрина (TfR) и ферритина. При этом присоединение IRP к мРНК рецептора трансферрина защищает ее от разрушения РНКазами, а присоединение его к мРНК ферритина не позволяет ей участвовать в процессе трансляции и синтезе новых молекул ферритина.
При снижении концентрации железа в клетке белок IRP активируется и, как следствие, мРНК рецепторов трансферрина существует дольше, образуется больше рецепторов и повышается поток железа в клетки. Одновременно снижается синтез ферритина.
Когда концентрация железа в клетке возрастает, оно присоединяется к IRP и снижает его сродство к матричным РНК. Конечным результатом является исчезновение рецепторов к трансферрину с мембраны и увеличение синтеза молекул ферритина, депонирующего железо.
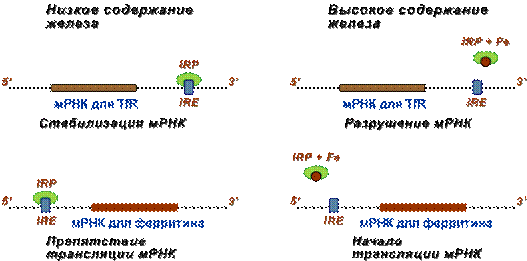
Регуляция синтеза рецепторов к трансферину и ферритина
Дефицит железа есть у трети населения
Нарушение обмена железа
Избыток +
Существует аутосомно-рецессивное заболевание гемохроматоз, связанное с нарушением гепсидиновой регуляции и избыточностью всасывания железа в кишечнике. Для него характерны цирроз печени, поражение сердца и поджелудочной железы, паращитовидных желез.
Приобретенныйизбыток железа возникает при гемолитических анемиях, нарушении использования железа в метаболизме, при избыточной парентеральной терапии железодефицитных состояний. Накапливающийся ферритинпреобразуется в гемосидерин, в результате резко снижается использование железа. Такое состояние называется гемосидероз.
Потребление препаратов железа per os не приводит к интоксикации, так как возможности транспорта металла из кишечника ограничены саморегуляцией энтероцитов и свойствами транспортных систем. Избыток железа задерживается в эпителии кишечника и выводится со слущивающимися клетками.
Дефицит
При недостаточности железа в организме (железодефицит) мобилизация резервов происходит в следующем порядке:
· сначала используется железо из депо (ферритин),
· затем в клетках (кроме эритроидных) снижается количество гемопротеинов до жизнеспособного минимума,
· далее истощаются запасы сывороточного железа (трансферрин),
· в последнюю очередь страдает синтез гемоглобина.
Таким образом, железодефицитная анемия является проявлением крайнегодефицита железа и нормальная концентрация гемоглобина крови не должна быть критериемобеспеченности организма железом!
По данным ВОЗ железодефицитное состояние имеется у трети населения планеты. В России это значение достигает 20%.
Причины дефицита железа
Причинами нехватки железа являются
· недостаток его в пище (несбалансированное вегетарианство),
· заболевания ЖКТ со снижением всасывания (гипоацидные гастриты и энтериты),
· потери железа с кровью при менструальных, кишечных или иных кровотечениях,
· у новорожденных и грудных детей недостаток железа связан в первую очередь с недополучением его при внутриутробном развитии, и также в связи с ускоренным ростом в первый год жизни (физиологическая анемия).
У женщин детородного возраста основные потери железа вызывают менструальные кровотечения. Известно, что около 20% женщин теряет 20 мл крови, 70% – 40-60 мл крови, 5% – 100 мл, 5% – 200 мл крови за цикл. Учитывая, что в 1 мл крови находится около 0,7 мг железа, потери железа составляют от 14 мг до 140 мг.
Во время беременности мать отдает ребенку 300-500 мг железа, особенно активно это происходит на 28-32 неделях, когда ребенку требуется по 22 мг в неделю. При лактации потери железа у матери составляют 11-12 мг/сут.
У мужчин и пожилых женщин основной причиной железодефицитных состояний являются кровопотери через ЖКТ. К сожалению, методы определения скрытой крови в кале низкочувствительны и позволяют обнаружить крови только при ее количестве свыше 15 мл (10,5 мг железа) в суточной порции кала.
Симптомы
Недостаточный синтез цитохромов, железосодержащих белков и нарушение доставки кислорода к тканям (при снижении содержания гемоглобина) вызывает ряд специфических и неспецифических симптомов:
· ухудшение вниманияи памяти у детей и взрослых,
· иногда детская гиперактивность,
· уплощение, волнистость и ломкость ногтей, появление исчерченности, белых пятен и полосок на ногтях,
· выпадающий и секущийся волос,
· поражение эпителия, проявляющееся в сухости и трещинах кожи рук и ног,
· неинфекционный ларингофаринготрахеит(гиперемия, покраснение и охриплость), что дезориентирует врача,
· мышечная слабость:
– общая утомляемость,
– недостаточное сокращение сфинктеров мочевого пузыря, при этом характерным признаком является выделение нескольких капель мочи при резком кашле, смехе, чихании,
– недостаточное сокращение сфинктеров пищевода, что позволяет забрасываться соляной кислоте в пищевод и вызывать изжогу.
· атрофический гастрит– может быть как причиной, так и следствием железодефицита, половина
больных гастритом имеет недостаток железа,
· обострение ишемической болезни сердца и других сердечно-сосудистых заболеваний, так как усиливает гипоэнергетическое состояние клеток (снижение содержания цитохромов в миокардиоцитах),
· извращение обонятельных предпочтений – нравится запах краски, бензина, выхлопных газов, резины, мочи,
· извращение вкусовыхпредпочтений – больные едят мел, штукатурку, уголь, песок, мясной фарш, лед.
Обмен гема и гемоглобина
Гемоглобин - основной белок крови
Гемоглобин входит в состав группы белков гемопротеины, которые сами являются подвидом хромопротеинов и подразделяются на неферментативные белки (гемоглобин, миоглобин) и ферменты (цитохромы, каталаза, пероксидаза). Небелковой частью их является гем – структура, включающая в себя порфириновое кольцо (состоящее из 4 пиррольных колец) и иона Fe2+. Железо связывается с порфириновым кольцом двумя координационными и двумя ковалентными связями.
Строение гемоглобина
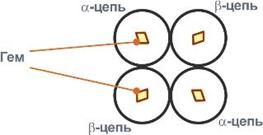
Строение гемоглобина А
Гемоглобин представляет собой белок, включающий 4 гемсодержащие белковые субъединицы. Между собой протомеры соединяются гидрофобными, ионными, водородными связями по принципу комплементарности. При этом они взаимодействуют не произвольно, а определенным участком - контактной поверхностью. Этот процесс высокоспецифичен, контакт происходит одновременно в десятках точек по принципу комплементарности. Взаимодействие осуществляют разноименно заряженные группы, гидрофобные участки, неровности на поверхности белка.
Белковые субъединицы в нормальном гемоглобине могут быть представлены различными типами полипептидных цепей: α, β, γ, δ, ε, ξ (соответственно, греч. - альфа, бета, гамма, дельта, эпсилон, кси). В состав молекулы гемоглобина входят по двецепи двухразных типов.
Гем соединяется с белковой субъединицей, во-первых, через остаток гистидина координационной связью железа, во-вторых, через гидрофобные связи пиррольных колец и гидрофобных аминокислот. Гем располагается как бы "в кармане" своей цепи и формируется гемсодержащий протомер.
Нормальные формы гемоглобина
Существует несколько нормальных вариантов гемоглобина:
· HbР – примитивный гемоглобин, содержит 2ξ- и 2ε-цепи, встречается в эмбрионе между 7-12 неделями жизни,
·
· HbF – фетальный гемоглобин, содержит 2α- и 2γ-цепи, появляется через 12 недель внутриутробного развития и является основным после 3 месяцев,
· HbA – гемоглобин взрослых, доля составляет 98%, содержит 2α- и 2β-цепи, у плода появляется через 3 месяца жизни и к рождению составляет 80% всего гемоглобина,
· HbA2 – гемоглобин взрослых, доля составляет 2%, содержит 2α- и 2δ-цепи,
· HbO2 – оксигемоглобин, образуется при связывании кислорода в легких, в легочных венах его 94-98% от всего количества гемоглобина,
· HbCO2 – карбогемоглобин, образуется при связывании углекислого газа в тканях, в венозной крови составляет 15-20% от всего количества гемоглобина.
Патологические формы гемоглобина
HbS – гемоглобин серповидно-клеточной анемии.
MetHb – метгемоглобин, форма гемоглобина, включающая трехвалентный ион железа вместо двухвалентного. Такая форма обычно образуется спонтанно, в этом случае ферментативных мощностей клетки хватает на его восстановление. При использовании сульфаниламидов, употреблении нитрита натрия и нитратов пищевых продуктов, при недостаточности аскорбиновой кислоты ускоряется переход Fe2+ в Fe3+. Образующийся metHb не способен связывать кислород и возникает гипоксия тканей. Для восстановления ионов железа в клинике используют аскорбиновую кислоту и метиленовую синь.
Hb-CO – карбоксигемоглобин, образуется при наличии СО (угарный газ) во вдыхаемом воздухе. Он постоянно присутствует в крови в малых концентрациях, но его доля может колебаться от условий и образа жизни.
Угарный газ является активным ингибитором гем-содержащих ферментов, в частности, цитохромоксидазы, 4-го комплекса дыхательной цепи.
HbA1С – гликозилированный гемоглобин. Концентрация его нарастает при хронической гипергликемии и является хорошим скрининговым показателем уровня глюкозы крови за длительный период времени.
У гемоглобина есть молекулярные болезни
Серповидно-клеточная анемия
HbS – гемоглобин серповидно-клеточной анемии. При й: α, β, γ, δ, ε, ξ этом нарушении в ДНК в результате точковой мутации триплет ЦТТ заменен на триплет ЦАТ, что влечет за собой включение в 6-м положении β-цепи вместо глутаматааминокислоты валина. Изменение свойств β-цепи влечет изменение свойств всей молекулы и формирование на поверхности гемоглобина "липкого" участка. При дезоксигенации гемоглобина участок "раскрывается" и связывает одну молекулу гемоглобина S с другими подобными. Результатом является полимеризация гемоглобиновых молекул и образование крупных белковых тяжей, вызывающих деформацию эритроцита и при прохождении капилляров гемолиз.
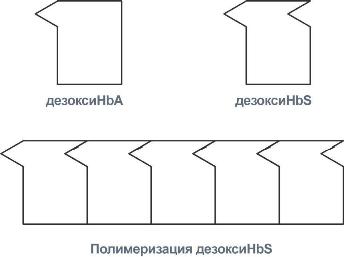
Схема отличия гемоглобина S от гемоглобина А и его полимеризация
Нарушение синтеза гемоглобина
Порфирии
Порфирии – это группа гетерогенных наследственных заболеваний, возникающих в результате нарушения синтеза гема и повышения содержания порфиринов и их предшественников в организме. Выделяют наследственные и приобретенные формы порфирии.
Приобретенныеформы порфирий носят токсический характер и вызываются действием гексахлорбензола, солей свинца и других тяжелых металлов (ингибирование порфобилиногенсинтазы, феррохелатазы и др.), лекарственными препаратами (антигрибковый антибиотик гризеофульфин).
При наследственныхформах дефект фермента имеется во всех клетках организма, но проявляется только в одном типе клеток. Можно выделить две большие группы порфирий:
1. Печеночные – группа заболеваний с аутосомно-доминантными нарушениями ферментов различных этапов синтеза протопорфирина IX. Наиболее ярким заболеванием этой группы является перемежающаяся острая порфирия, при которой у гетерозигот активность уропорфириноген-I-синтазы снижена на 50%.
Заболевание проявляется после достижения половой зрелости из-за повышенной потребности гепатоцитов в цитохроме Р450 для обезвреживания половых стероидов, обострение состояния также часто бывает после приема лекарственных препаратов, метаболизм которых требует участия цитохрома Р450. Потребление и снижение концентрации гема, необходимого для синтеза цитохрома Р450, активирует аминолевулинатсинтазу . В результате больные экскретируют с мочой большие количества порфобилиногена и аминолевулиновой кислоты. На свету порфириноген окисляется в окрашенные порфобилин и порфирин, и это является причиной потемнения мочи при ее стоянии на свету при доступе воздуха. Симптомами являются острые боли в животе, запоры, сердечно-сосудистые нарушения, нервно-психические расстройства.
2. Эритропоэтические – аутосомно-рецессивные нарушения некоторых ферментов синтеза протопорфирина IX в эритроидных клетках. При этом смещается баланс реакций образования уропорфириногенов в сторону синтеза уропорфириногена I. Симптомы заболевания схожи с предыдущим, но дополнительно наблюдается светочувствительность кожи, обусловленная наличием уропорфириногенов, кроме этого отмечаются трещины на коже и гемолитические явления.
Талассемии
Для талассемий характерно снижение синтеза α-цепей гемоглобина (α-талассемия) или β-цепей (β-талассемия). Это приводит к нарушению эритропоэза, гемолизу и тяжелым анемиям.
Миоглобин тоже способен связывать кислород
Миоглобин является одиночнойполипептидной цепью, состоит из 153 аминокислот с молекулярной массой 17 кДа и по структуре сходен с β-цепью гемоглобина. Белок локализован в мышечной ткани. Миоглобин обладает более высоким сродством к кислороду по сравнению с гемоглобином. Это свойство обуславливает функцию миоглобина – депонирование кислорода в мышечной клетке и использование его только при значительном уменьшении парциального давления О2 в мышце (до 1-2 мм рт.ст).
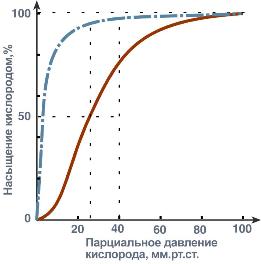
Кривые насыщения кислородом показывают отличия миоглобина и гемоглобина:
· одно и то же 50%-е насыщение достигается при совершенно разных концентрациях кислорода – около 26 мм рт.ст. для гемоглобина и 5 мм рт.ст. для миоглобина,
· при физиологическом парциальном давлении кислорода от 26 до 40 мм рт.ст. гемоглобин насыщен на 50-80%, тогда как миоглобин – почти на 100%.
Таким образом, миоглобин остается оксигенированным до того момента, пока количество кислорода в клетке не снизится до предельныхвеличин. Только после этого начинается отдача кислорода для реакций метаболизма.
Эффективность транспорта кислорода регулируется
Изменение рН среды
Влияние рН на сродство гемоглобина к кислороду носит название эффекта Бора. При закислении среды сродство снижается, при защелачивании – повышается.
При повышенииконцентрации протонов (закисление среды) в тканях возрастает освобождение кислорода из оксигемоглобина. Влегких после удаления угольной кислоты (в виде СО2) из крови и одновременном увеличении концентрации кислорода высвобождаются ионы Н+ из гемоглобина.
Реакция взаимодействия кислорода с гемоглобином упрощенно имеет вид:

Изменение сродства гемоглобина к кислороду в тканях и в легких при изменении концентрации ионов H+ и О2 обусловлено конформационными перестройками глобиновой части молекулы. В тканях ионы водорода присоединяются к остаткам гистидина, образуя восстановленный гемоглобин (H-Hb) с низким сродством к кислороду. В легких поступающий кислород "вытесняет" ион водорода из связи с остатком гистидина гемоглобиновой молекулы.
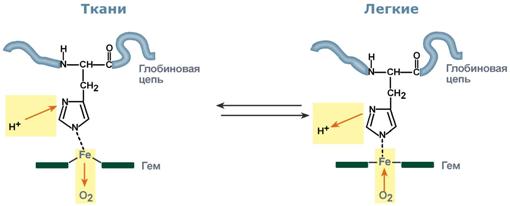
Механизм эффекта Бора
Кооперативное взаимодействие
Взаимовлияние протомеров олигомерного белка друг на друга называется кооперативное взаимодействие.
В легких такое взаимодействие субъединиц гемоглобина повышает его сродство к кислороду и ускоряет присоединение кислорода в 300 раз. В тканяхидет обратный процесс, сродство снижается и ускорение отдачи кислорода также 300-кратное.
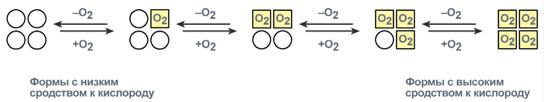
Схема кооперативного взаимодействия субъединиц гемоглобина
Объясняется такой феномен тем, что в легких при присоединении первой молекулы кислорода к железу (за счет 6-й координационной связи) атом железа втягивается в плоскость гема, кислород остается вне плоскости. Это вызывает перемещение участка белковой цепи и изменение конформации первого протомера. Такой измененный протомер влияет на другие субъединицы и облегчает связывание кислорода со второй субъединицей. Это меняет конформацию второй субъединицы, облегчая присоединение последующих молекул кислорода и изменение других протомеров.
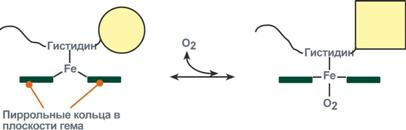
Изменение формы субъединиц гемоглобина при присоединении кислорода
Роль 2,3-дифосфоглицерата
2,3-Дифосфоглицерат образуется в эритроцитах из 1,3-дифосфоглицерата, промежуточного метаболита гликолиза, в реакциях, получивших название шунт Раппопорта.
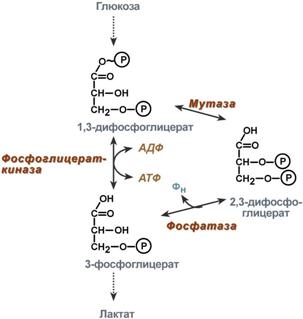
Реакции шунта Раппопорта
2,3-Дифосфоглицерат располагается в центральной полости тетрамера дезоксигемоглобина и связывается с β-цепями, образуя поперечный солевой мостик между атомами кислорода 2,3-дифосфоглицератаи аминогруппами концевого валина обеих β-цепей, также аминогруппами радикалов лизинаи гистидина.
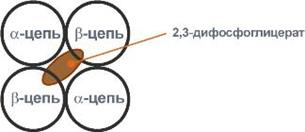
Расположение 2,3-дифосфоглицерата в гемоглобине
Функция 2,3-дифосфоглицерата заключается в снижении сродства гемоглобина к кислороду. Это имеет особенное значение при подъеме на высоту, при нехватке кислорода во вдыхаемом воздухе. В этих условиях связывание кислорода с гемоглобином в легких не нарушается, так как концентрация его относительно высока. Однако в тканях за счет 2,3-дифосфоглицерата отдача кислорода возрастает в 2 раза.
Газообмен происходит по градиенту концентраций
Обмен кислорода и углекислого газа в тканях
В тканях диффундирующий в кровь из клеток СО2 большей частью (около 90%) по градиенту концентрации попадает в эритроциты. Движущей силой этого процесса является быстрая, постоянно идущая реакция превращения его в угольную кислоту при участии фермента карбоангидразы. Угольная кислота диссоциирует и подкисляет содержимое эритроцита, что улучшает отдачу оксигемоглобином кислорода (Эффект Бора).
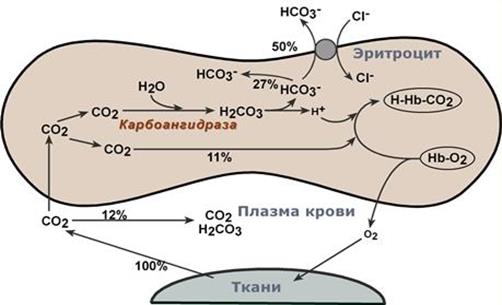
Реакции газообмена в капиллярах тканей
Одновременно с концевыми NH2-группами β-цепей гемоглобина связывается 10-12% карбонат-иона с образованием карбаминогемоглобина(H-HbCO2).
Остальные бикарбонаты выходят в плазму крови в обмен на ионы хлора (гипохлоремический сдвиг).
Обмен кислорода и углекислого газа в легких
В легочных капиллярах имеется относительно низкая концентрация углекислого газа в альвеолярном воздухе:
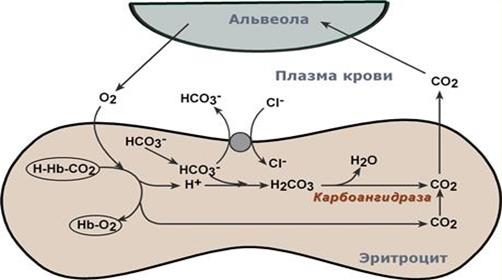
Реакции газообмена в легочных капиллярах
· происходит высокоэффективная диффузия СО2 из плазмы через альвеолярные мембраны и его удаление с выдыхаемым воздухом,
· уменьшение концентрации СО2 в плазме стимулирует его образование в карбоангидразной реакции внутри эритроцита и снижает здесь концентрацию иона HCO3–,
· одновременно высокая концентрация кислорода вытесняет СО2 из комплекса с гемоглобином с образованием оксигемоглобина – более сильной кислоты, чем угольная,
· диссоциирующие от оксигемоглобина ионы Н+ нейтрализуют поступающий извне ион HCO3– с образованием угольной кислоты. После карбоангидразной реакции образуется СО2, который выводится наружу.
Гем необходим для многих ферментов
Гем является небелковой частью многих гемопротеинов:
· гемоглобин (до 85% общего количества гема организма), локализованный в эритроцитах и клетках костного мозга,
· миоглобин скелетных мышц и миокарда (17%),
· цитохромы дыхательной цепи,
· ферменты цитохромоксидаза, цитохром P450, гомогентизатоксидаза, пероксидаза, миелопероксидаза, каталаза, тиреопероксидаза и т.д. – менее 1%.
Строение и синтез гема
Синтез гема в основном идет в предшественниках эритроцитов, клетках печени, почек, слизистой кишечника, и в остальных тканях. Первая реакция синтеза с участием δ-аминолевулинат-синтазы (греч. δ - "дельта") происходит в митохондриях. Следующая реакция при участии аминолевулинатдегидратазы (порфобилиноген-синтазы) протекает в цитозоле. Здесь из двух молекул δ‑аминолевулиновой кислоты образуется циклический порфобилиноген (монопиррол).
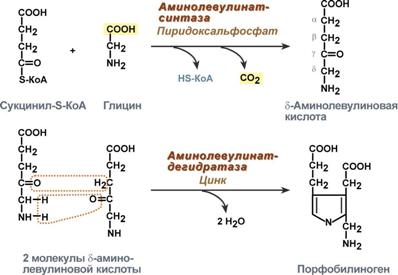
Синтез порфобилиногена
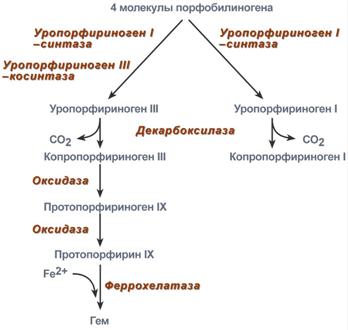
После синтеза порфобилиногена четыре его молекулы конденсируются с образованием уропорфириногена(тетрапиррол). Их различают два вида - уропорфириноген типа I и уропорфириноген типа III. В синтезе обоих видов порфиринов принимает участие уропорфириноген I-синтаза, в образования уропорфириногена III дополнительно принимает участие фермент уропорфириноген III-косинтаза.
Судьба обоих типов уропорфириногена двояка: они могут окисляться до уропорфирина (на рисунке не показано) или декарбоксилироваться до копропорфириногенасоответствующего типа. Копропорфириноген III превращается либо в копропорфирин III (не показано), либо идет на синтез протопорфирина IX.
 й: α, β, γ, δ, ε, ξ
й: α, β, γ, δ, ε, ξ
Синтез гема из порфобилиногена
Копропорфириноген III окисляется в протопорфириноген IX и далее в протопорфирин IX. Последний после связывания с железом образует гем, реакцию катализирует феррохелатаза (гемсинтаза).
Названия пигментов (уропорфирины и копропорфирины) были даны веществам по источникуих первоначального выделения, при этом восстановленные бесцветные формы называют порфириногенами. Для порфиринов характерно наличие изомериивследствие различного расположения радикалов.
Регуляция синтеза гема
1. Скорость синтеза глобиновых цепей зависит от наличия гема, он ускоряет биосинтез "своих" белков.
2. Основным регуляторным ферментом синтеза гема является аминолевулинатсинтаза.
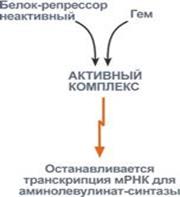
· гемпосле взаимодействия с молекулой белка-репрессора формирует активный репрессорный комплекс, связывается с ДНК и подавляет транскрипцию, мРНК для фермента не образуется и синтез фермента прекращается. Также имеется отрицательный аллостерический эффект гема на фермент.
| 
|
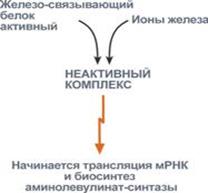
| Подавление гемом синтеза аминолевулинатсинтазы | Стимуляция синтеза аминолевулинатсинтазы ионами железа |
· с другой стороны, достаточное количество ионов железа оказывает положительный эффект при синтезе молекулы аминолевулинатсинтазы. В клетке имеется особый железосвязывающий белок, который в отсутствии ионов железа обладает сродством к мРНК фермента и блокирует ее трансляцию в рибосоме, т.е. синтез белковой цепи. Ионы железа связываются с этим железосвязывающим белком, образуя с ним неактивный комплекс, что инициирует синтез фермента.
3. Положительным модулятором аминолевулинатсинтазы служит гипоксиятканей, которая в эритропоэтических тканях индуцирует синтез фермента.
4. В печени повышение активности аминолевулинатсинтазы вызывают соединения, усиливающие работу микросомальной системы окисления (жирорастворимые токсины, стероиды) – при этом возрастает потребление гема для образования цитохрома Р450, что снижает внутриклеточную концентрацию свободного гема. В результате происходит дерепрессия синтеза фермента.
Распад гема - многостадийный процесс
За сутки у человека распадается около 9 г гемопротеинов, в основном это гемоглобин эритроцитов. Эритроциты живут 90-120 дней, после чего лизируются в кровеносномрусле или в селезенке.
При разрушении эритроцитов в кровяном русле высвобождаемый гемоглобин образует комплекс с белком-переносчиком гаптоглобином (фракция α2-глобулинов крови) и переносится в клетки ретикуло-эндотелиальной системы (РЭС) селезенки (главным образом), печени и костного мозга.
Синтез билирубина
В клетках РЭС гем в составе гемоглобина окисляется молекулярным кислородом. В реакциях последовательно происходит разрыв метинового мостика между 1-м и 2-м пиррольными кольцами гема с их восстановлением, отщеплением железа и белковой части и образованием оранжевого пигмента билирубина.
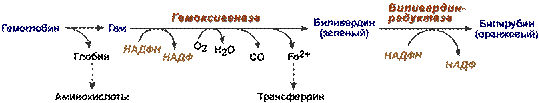
Реакции распада гемоглобина и образования билирубина
Билирубин – токсичное, жирорастворимое вещество, способное нарушать окислительное фосфорилирование в клетках. Особенно чувствительны к нему клетки нервной ткани.
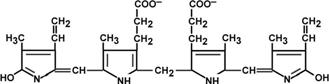
Строение билирубина
Выведение билирубина
Из клеток ретикуло-эндотелиальной системы билирубин попадает в кровь. Здесь он находится в комплексе с альбумином плазмы, в гораздо меньшем количестве – в комплексах с металлами, аминокислотами, пептидами и другими малыми молекулами. Образование таких комплексов не позволяет выделяться билирубину с мочой. Билирубин в комплексе с альбумином называется свободный (неконъюгированный) или непрямой билирубин.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|