
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Организмніңбуферлікжүйелері.
Организмнің қ алыптыжұ мысжасауыү шіноның ішкіортасының тұ рақ тылығ ының маң ызызор. Ғ ылымитілменайтқ андаоны - гомеостаздепатайды. Ағ заның физиологиялық функцияларының бекемдігін, тұ рақ тылығ ынкө рсететін, оның ішкіқ ұ рылысының қ ұ рамыменқ асиеттерінің салыстырмалыдинамикалық тұ рақ тылығ ы гомеостаз депаталады.
Гомеостаздың негізгікө рсеткіштерінің бірі - сутегі ( Н+) жә негидроксил (ОН-) иондарының қ атынасыменанық талатынхимиялық ортаның реакциясыболыптабылады. Олқ алыптыжағ дайдақ андаә лсізсілтілік ( рН= 7. 4) ортаболады, алоның сә лғ анақ ышқ ылдық жақ қ аығ ысуыбарлық жү йенің қ айтымсызө згерісінеұ шыратуымү мкін. Сондадаболса, ұ лпаларданү немізаталмасупроцесінің нә тижесіндетү зілетінө німдер, ә сіресеСО2қ анғ атү сіпотырады. Шетелғ алымдары: З. Андерсонжә неП. Аструптың зерттеулерібойынша 3 секундішіндеорганизмдеө мірсү ругесә йкескелметінқ ышқ ылмө лшерікө бейіпкетуімү мкін. Соғ анқ арамастанқ анның рНө згермейді.
Ө йткеніорганизмдебиологиялық сұ йық тық тардың ортасын, яғ ниқ ышқ ылдылығ ынтұ рақ тыұ стаптұ ратынпроцестержү реді. Олардың тұ рақ тылығ ыбуферлікжү йелердің ә серетумеханизміментікелейбайланысты.
Бикарбонаттық буферлікжү йеқ анплазмасының негізгіжү йесіболыпесептеледі. Бұ лжү йеә лсізкө мірқ ышқ ылынан (К=3, 3 10-7) жә ненатрийбикарбонатынантұ рады. Олардың молекулаларық анның плазмасынындаболады. Н2СО3ә лсізқ ышқ ыл, сондық таннашардиссоциациаланады, яғ нибоскү йіндеортаның қ ышқ ылдылығ ынанық тайтынН+ионынө зіненбө ліпжібермейді.
 Н2СО3 Н2СО3 - протонның доноры
Н2СО3 Н2СО3 - протонның доноры
NaHCO3 HCO3- - протонның акцепторы
Қ ышқ ыл заттар кө п мө лшерде қ анғ а бө лінгенде, сутегі иондары гидрокарбонат ионымен ә рекеттесіп, Na+ жә не Н+ иондары алмасып, ә лсіз кө мір қ ышқ ылын тү зеді:
Н+ + НСО3- = Н2СО3
Кө мір қ ышқ ылының артық мө лшері карбоангидраза (КА) ферментінің ә серінен ыдырайды:
 Н2СО3КА СО2 + Н2О ( t= 37oC)
Н2СО3КА СО2 + Н2О ( t= 37oC)
CO2 гипервентилляция нә тижесінде ө кпе арқ ылы сыртқ а шығ ады.
Егер, қ андағ ы ОН- -иондардың концентрациясы жоғ арыласа, олар ә лсіз кө мір қ ышқ ылымен ә рекеттеседі:
ОН- + Н2СО3 = НСО3- + Н2О
Оксигемоглобин - гемоглобин жү йесі қ анның буферлік сыйымдылығ ының 75%-ін қ ұ райды, ол гемоглобин ионы (Нb-) мен гемоглобиннің (ННb) арасындағ ы тепе-тең дікпен сипатталады.
HHb -донор Hb -акцептор
Hb- + H+ = HHb
HHb + OH- = Hb- + H2O
Сол сиякты бұ л жү йе оксигемоглобин -ионы (НbО2-) мен оксигемоглобиннің (ННbО2) арасындағ ы байланыс мына тең деумен кө рсетіледі:
ННbО2 -протонның доноры
HbО2- -протонның акцепторы
HbО2- + Н+ = ННbО2
ННbО2 + ОН- = HbО2- + H2O
Екі тепе-тең діктің арасындағ ы байланыс мыны тең деумен кө рсетіледі:
HHb + О2 = ННbО2
Фосфаттық буферлік жү йе клеткаішілік жә не тканьдік негізгі жү йе болып есептеледі. Бү йректе жү ретін физиологиялық процестерде маң ызды роль атқ арады. Бұ л жү йе 2 тұ здан тұ рады:
 NaH2РО4 (Н2РО4- -протонның доноры)
NaH2РО4 (Н2РО4- -протонның доноры)
Na2HРО4 (НРО42- -протонның акцепторы)
Н2РО4- = Н+ + НРО42-
рН = 7, 4 болғ анда, 

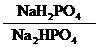 =
= 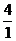
Тканьдік метаболизмнің қ ышқ ыл туындалары гидрофосфатпен нейтралданады: НРО42- + Н+ = Н2РО4-
Сілтілік туындылар дигидрофосфатпен ә рекеттеседі:
ОН- + Н2РО4- = НРО42- + Н2О
Тү зілген ө німдер бү йректе жиналып, несеппен сыртқ а шығ ады.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|