
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
5. Факторы и разы.
Пример:
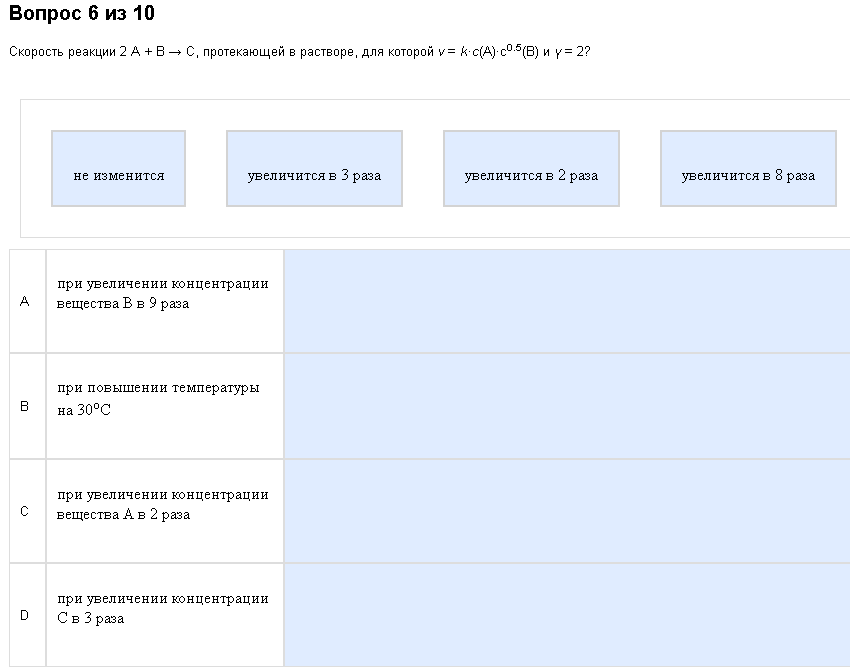
Олдскулы свело – старый скрин, вопрос не изменился…
Как с этим бороться:
Разберем факторы по отдельности.
1) Концентрации. Там есть формула, см. условия внимательно. В этой формуле есть с(А) и с(В) — концентрации веществ А и В. У них могут быть разные степени, в примере у В — 0, 5, а у А не стоит, значит 1. НЕ НАДО тащить коэффициенты в формулу. Про реакцию не сказано и никогда не будет, что она простая. Мысленно подставляем изменение в разах в формулу, если предлагают увеличить В в 9 раз, то подставляем 90, 5=3, то есть скорость увеличится в 3 раза. Если концентрацию А изменить в 2 раза, то 21=2 раза, скорость увеличится в 2 раза. Если концентрацию предлагают уменьшать, то и скорость должна уменьшаться. От концентрации С скорость на зависит, ведь С не входит в формулу.
2) Давление. В примере нет, но бывает. Если давление изменить в N раз, то все концентрации меняются в N раз, но только при условии, что все вещества газы, но только при условии, что все вещества газы. Дальнейшие оценки как в концентрациях. Обратите внимание, в примере реакция в растворе. Например, если бы реакция протекала в газе, и при этом давление увеличивалось бы в 3 раза, то с(А) и с(В) увеличились бы в 3 раза, а делее, вставив в формулу эти разы 31·30, 5=5, 2 раза, ну примерно. Важное замечание: реакции бывают идущими в растворе и в газовой фазе. Для реакций, идущих в растворе изменение давление не приводит к изменению скорости. Это как в примере. Не проебитесь с этим.
3) Температура. Для оценки температуры использовать γ, которая в условии тоже есть, и формулу Вант-Гоффа, не могу не похвалить ещё раз Вант Гоффа, великий человек, и тут он помог.
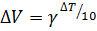
Вставить температуру и эту стремную закорючку из условия, осторожно посчитать на калькуляторе, или в уме, благо несложно. В примере это будет:
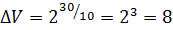 раз.
раз.
Обратите внимание, что между температурой и скоростью прямая зависимость, при увеличении температуры скорость увеличивается, при уменьшении уменьшается.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|