
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Тема 4. Кинетика.
Введение: Кинетика отделена от равновесия, что может быть лучше. Кинетика – раздел химии, изучающий скорости реакций.
1) Формула, как рассчитать скорость реакции:
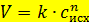
Тут V — скорость реакции, (моль/л*время), k — константа скорости (размерность может быть разной), cисх — концентрация исходного вещества (моль/л), n — называется порядок по веществу, короче, степень. Концентраций может быть несколько, тогда они перемножены, каждая в своей степнени. Например, для реакции А+В=С уравнение будет иметь вид
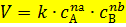
Где
V – скорость реакции
K – константа скорости
CА и cВ — концентрации исходных веществ А и В (моль/л)
nА и nB — называется порядок по веществу А и В
2) Формула, как связать константу скорости и период полураспада (реакции первого порядка).
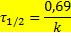
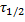 — период полураспада (время), k — константа скорости. Приводится из ностальгии. Года с 2016 эта формула нахуй никому не упала, но мы всё помним и скучаем по тем временам.
— период полураспада (время), k — константа скорости. Приводится из ностальгии. Года с 2016 эта формула нахуй никому не упала, но мы всё помним и скучаем по тем временам.
3) Уравнение Вант-Гоффа:
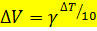
Формула не совсем как в учебнике, но для удобства решения задач она слегка преобразована. Δ Т — изменение температуры, γ — температурный коэффициент Вант-Гоффа, 10=10, а Δ V — величина, показывающая, во сколько раз изменится скорость реакции, если изменить температуру.
Типичные вопросы:
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|