
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
m(FeSO4)=(0,6092 ± 0,0032) г/100 мл
m(FeSO4)=(0,6092 ± 0,0032) г/100 мл
Лабораторная работа №6
«Йодометрическое титрование»
1) Приготовление 500 мл 0,05М раствора тиосульфата натрия Na2S2O3 (вторичный стандарт).
Методика:
Растворы тиосульфата обычно готовят из кристаллического Na2S2O3 ∙5H2O. Для приготовления растворов Na2S2O3 следует применять дистиллированную воду, не содержащую примесей ионов тяжёлых металлов, кислорода воздуха и углекислого газа. fэкв.( Na2S2O3)=1/1.
Дистиллированную воду для растворения тиосульфата предварительно кипятят 1 час, охлаждают в колбе, закрытой пробкой с U-образной трубкой, наполненной твёрдым КОН. Навеску Na2S2O3 ∙5Н2О растворяют в свежепрокипячённой и охлаждённой дистиллированной воде. Раствор хранят в тёмном месте, в хорошо закрытой посуде.
Масса Na2S2O3:
gNa2S2O3= Vр-ра Na2S2O3 ∙ С(1/1 Na2S2O3) ∙ M(1/1 Na2S2O3)=6,2 г
=248 г/моль экв.
2) Приготовление 100 мл 0,05М раствора K2Cr2O7 (первичный стандарт).
Методика – см. приготовление раствора (NH4)2SO4 ∙ H2O.
|
m2=14,8966 г
Характеристики K2Cr2O7:
TK2Cr2O7 = m K2Cr2O7/Vр-ра=0,002709 г/мл;
С(1/6 K2Cr2O7)=1000 TK2Cr2O7/М(1/6 K2Cr2O7)=0,0552857 н.
=49 г/моль экв.
3) Стандартизация тиосульфата.
Методика:
В коническую колбу для титрования переносят пипеткой раствор K2Cr2O7, добавляют 10 мл 2 н. раствора H2SO4 и 1 г кристаллического KI (или соответствующий объём его концентрированного раствора). Колбы закрывают стеклянными пробками, дают постоять 5-10 минут в темноте до завершения реакции (раствор цвета суспензированного коровьего навоза J). Выделившийся I2 титруют тиосульфатом до слабо-жёлтой окраски; затем титруемый раствор разбавляют ≈в 2 раза, добавляют каплю индикатора крахмала и заканчивают титрование, когда синяя окраска раствора перейдёт в светло-зелёную (ионы Cr3+).
Титрование протекает по реакциям:
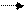 K2Cr2O7+6KIизб+7H2SO4 3I2+Cr2(SO4)3+4K2SO4+7H2O
K2Cr2O7+6KIизб+7H2SO4 3I2+Cr2(SO4)3+4K2SO4+7H2O
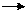 2Na2S2O3+I2 Na2S4O6+2NaI
2Na2S2O3+I2 Na2S4O6+2NaI
Результаты титрования:
| VK2Cr2O7, мл | V Na2S2O3, мл |
| 10,75 | |
| 10,8 | |
| 10,6 | |
| 10,65 | |
| 10,65 |
V Na2S2O3=10,69 мл
Стандартные характеристики тиосульфата:
нормальная концентрация:
по титру K2Cr2O7–
С(1/1Na2S2O3)=[TK2Cr2O7∙ V K2Cr2O7∙ 1000]/[M(1/6 K2Cr2O7 ∙ V Na2S2O3]=0,05172 н.
по концентрации K2Cr2O7–
С(1/1Na2S2O3)=[C(1/6 K2Cr2O7) ∙ V K2Cr2O7]/VNa2S2O3=0,05172 н.
титр:
по титру K2Cr2O7–
TNa2S2O3=[T K2Cr2O7∙ V K2Cr2O7∙ M(1/1Na2S2O3)]/[VNa2S2O3∙ M(1/6 K2Cr2O7)]=0,001283 г/мл
по концентрации K2Cr2O7–
TNa2S2O3=[С(1/5 Na2S2O3) ∙ V K2Cr2O7 ∙ M(1/1 Na2S2O3))]/[VNa2S2O3∙1000]=0,001283 г/мл
 |
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|