
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Приготовление раствора тетрабората натрия
Приготовление раствора тетрабората натрия
Навескутетрабората натрия (Na2B4O7 x 10 H2O) рассчитывают по формуле:
Р Na2B4O7 x 10 H2O, г = V Na2B4O7 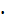 N Na2B4O7
N Na2B4O7 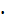 мЭ Na2B4O7 x 10 H2O.
мЭ Na2B4O7 x 10 H2O.
Значение мЭ Na2B4O7 x 10 H2O находят из уравнения реакции, в которой может участвовать тетраборат натрия:
Na2B4O7 + 2 HCl + 5 H2O = 2 NaCl + 4H3 BO3.
1г – м Na2B4O7 взаимодействует с 2 г – ионами водорода. Отсюда:
Э Na2B4O7 x 10 H2O = 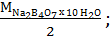 мЭ Na2B4O7 x 10 H2O =
мЭ Na2B4O7 x 10 H2O = 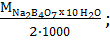
М Na2B4O7 x 10 H2O 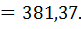
Для приготовления 250,00 г 0,1000 н раствора необходимая навеска численно равна
 Р Na2B4O7 x 10 H2O,г = 250 0,1 381,37/ 2
Р Na2B4O7 x 10 H2O,г = 250 0,1 381,37/ 2 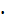 1000 = 4,7671 г.
1000 = 4,7671 г.
Эту навеску взвешивают на аналитических весах с точностью 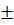 0,0001 г и количественно переносят в мерную колбу. Раствор в колбе доводят до метки
0,0001 г и количественно переносят в мерную колбу. Раствор в колбе доводят до метки
Лабораторная работа
Приготовление 0,1н раствора соляной кислоты
Соляную кислоту с концентрацией, приблизительно равной 0,1 н, готовят из концентрированной кислоты. Для определения концентрации этой кислоты, выраженной в г-экв /л, 100 мл кислоты наливают в цилиндр и измеряют плотность раствора аэрометром. По справочным таблицам находят соответствующую измеренной плотности нормальность. Объем кислоты, необходимый для приготовления разбавленного раствора, рассчитывают , используя следствие из закона эквивалентов:
V конц. = Vразб 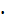 Nразб / Nконц.
Nразб / Nконц.
Например, необходимо приготовить 500 мл 0,1 н раствора соляной кислоты. Плотность концентрированной кислоты d = 1,17 г/см3. Кислоте с такой плотностью соответствует концентрация (н) = 10,97. Таким образом, необходимый объем кислоты равен:
V конц. = 500 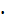 0,1 / 10,97
0,1 / 10,97 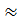 4,5 мл.
4,5 мл.
Готовят раствор следующим образом: в колбу наливают 250 мл воды, приливают 4,5 мл кислоты и остаток воды (250 мл). Закрывают колбу пробкой, тщательно перемешивают.
Лабораторная работа 4.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|