- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Качественный контроль димедрола 1 страница
| Rp: Dimedroli 0, 003, Furacilini 0, 04, Mentholi 0, 02, Zinci oxydi 1, 0, Vaselini 20, 0 Lanolini 5, 0 M. D. S. Мазь в нос Сложная мягкая лекарственная форма для наружного применения, комбинированная мазь, содержащая вещества списка Б. Расчеты: mобщ = 26, 063 % порошков для мази суспензии 1, 04 — 26, 063 х = 1, 04 • 100 = 3, 99% < 5% х — 100, 0 26, 063 Теоретическое обоснование: Готовим по массе в ступке, каждый тип мази отдельно. Ментол растворим в вазелине, и образует мазь-раствор. Масса мази меньше 30, 0 поэтому основу не расплавляем, а подогреваем ступку. Целесообразно начинать приготовление мази именно с мази-раствора. Для мази суспензии рассчитываем % порошков, он меньше 5%, поэтому оксид цинка и фурацилин растираем с родственной к основе жидкостью. Оксид цинка и фурацилин не растворимы ни в воде ни в вазелине, поэтому образуют мазь суспензию. Димедрол алкалоидоподобное вещество он вводится в растворенном виде и образуется мазь-эмульсия. Полученный раствор эмульгируют ланолином водным т. к. не указана консистенция ланолина. Все мази смешать ипереложить в баночку. Этикетки «Мазь в нос», «Наружное», «Хранить в прохладном защищенном от света месте» ППКкрецепту № 13. 06. 2012 t Mentholi 0, 02 Vaselini 1, 0 Agua purificatae q. s. Dimedroli 0, 003 Lanolini hydrici 2, 0 Zinci oxydi 1, 0 Furacilini 0, 04 Olei Vaselini q. s. Vaselini 19, 0 Lanolinihydrici 3, 0 mобщ = 26, 063 Приготовил: Проверил: Отпустил: |
Качественный контроль димедрола а) р-ция образования оксониевой. соли – к 0, 1г порошка + 1-2кап H2SO4(к)= жёлт. окр постепенно приобретающее оранж. окр (оксон. соль). а) Реакция образования оксониевой соли. К 0, 1 порошка + 1-2кап концентрированной серной к-ты. Появляется желтое окрашивание, постепенно приобретающее оранжевый оттенок (оксониевая соль). При добавлении 1-2 кап Н2О окр. исчезает.
б) на Сl- (дим)*HCl + AgNO3 = AgCl + (дим)*HNO3 выпадает бел. творожистый. осадок(р-рим в аммиаке, не р-рим в HNO3) Cl- + AgNO3 = AgCl + NO3- | ||
Билет №2. Rp: Sol. Atropinisulfatis 0, 25% 100ml
Steril!
D. S. Для в/в введения по 0, 2 мл
Сложная жидкая лекарственная форма для инъекций, истинный раствор с сильнодействующим в-вом списка А.
Расчеты:
Vобщ = 100 мл
Атропина сульфат – состоит из слабого основания и сильной к-ты, поэтому стабилизируем 0, 1М р-ром HCl
Кол-во стабилизатора: 10 мл – 1000мл р-ра х = 10 • 100 = 1 мл 1мл = 20 кап
х мл - 100 мл р-ра 1000
Теоретическое обоснование:
Готовят массо-объемным способом в асептических условиях, в мерной колбе, методом доведения до объема, т. к. раствор для инъекций.
. Раствор фильтруют через вату и складчатый фильтр, проверяют на чистоту, маркируют и закрывают под обкатку. Стерилизуют паровым методом при t = 120ОС 8 минут, т. к. объем р-ра 100 мл. После стерилизации раствор повторно проверяют на чистоту и оформляют к отпуску. Этикетки «Для инъекций», «Стерильно», «Хранить в прохладном защищенном от света месте», «Обращаться с осторожностью». Больному выдается сигнатура. На обратной стороне сигнатуры кол-во и название стабилизатора
ППК к рецепту № 13. 06. 2012 А
Aguaproinjektionibusq. s.
Atropini sulfatis 0, 25
Sol. Acidi hydrohloridi 0, 1M 1ml
Agua pro injektionibus ad 100ml
Vобщ = 100 ml
Приготовил: Проверил: № анализа 2/3 Подпись провизора-аналитика: Дата:
Формула атропина сульфата
| ВАК 0, 25% р-ра атропина сульфата П: работа с требованием: правильность выписывания; наличие указаний о способе применения Дата, № требования, название или № отделения, ППК № ан-за, подпись пров-аналит: дозы не превышены, атропина сульфат – подчеркнуть красн. карандаш. (т. к. сп А), ППК О: б/цв, прозр. жид-ть, б/видим. мех. вкл(провер-ся до и после стер-ции) КПО: в плот. укупор. таре. под металлическим колпачком Осн. этик: «Для инъекций», «Стерильно», На этикетке указаны состав л. с. на латинском языке и способ применения Sol. Atropini sulfatis 0, 25% — 100ml, в/в по 0, 2 мл, наименование и адрес аптеки, № анализа (до и после стерилизации), дата, срок годности 30 суток, фамилии приготовившего, проверившего и отпустившего лекарственную форму. Предупр. этик: «Обращ. с остор. », «Хр. в п. з от с. м. », «Беречь от детей». О, Ф: ОБЯЗАТЕЛЬНО!!! Пров-ся до и после стер-ции, не < 5флак данной серии стер-ции Vo=100мл, доп. откл = ± 3% [ 97÷ 103 мл] таб. 5 ПХК ОБЯЗАТЕЛЕН!!! до стерилизации проверяют рН, ПХК атропина изотонирующего вещ-ва и стабилизатора; после стер. рН и ПХК атропина Кач: 1) на основание атропина (р-ция Витали-Морена) – 5 кап. р-ра преп-та + неск. кап. HNO3(к ) ивыпаривают = жёлт. осадок + 3 кап. спирт. р-ра KOH и ацетона = фиолет. окр (исчезает при стоянии)
2) к р-ру + р-р аммиака = бел. ос (основание атропина) 3) На H2SO4 к р-ру + ВаСl2 = бел. крист. ос (не р-рим в к-тах и щел) SO42- + BaCl2 = BaSO4 + 2Cl- 4)на Na –к р-ру + укс. к-та+цинк-уранил-ацетат= жёлт. крист. ос Na+ + Zn(UO2)3(CH3COO)8 + CH3COOH + 9H2O = Na(Zn(UO2)3(CH3COO)9)*9H2O + H+ 5)на Сl – к р-ру + HNO3 + AgNO3 = бел. тв. ос (р-рим в аммиаке, не р-рим в HNO3) Cl- + AgNO3 = AgCl + NO3- Колич: 1)М-д нейтрализации в спирто-хлороформенной среде – инд –ф/фт – к р-ру + СН3Сl и титруют NaOH = до роз. окр. водн. слоя (атропин)*H2SO4 + 2NaOH = Na2SO4 + 2(атропин) + 2H2O Расчеты: 1) Анализ атропина М = 694, 8 f=1/2 Cf=0, 05 T = 694, 8*1/2*0, 05 = 0, 01737 1000 Слепую методику для атропина надо изменить и увеличить количество раствора для анализа до 5 мл, т. к. получается очень маленький ориентировочный объем и соответственно увеличиваются и все остальные реактивы, не меняется только титр. Сначала титруется HCl. На титрование 0, 05мл 0, 1M кислоты (столько содержится в 5мл р-ра) надо 0, 05мл 0, 1MNaOH, а затем начинает титроваться атропин, поэтому формула будет:
m(атр)=(V1 – 0, 05)*K1*T*100 = (0, 82 – 0, 05) • 1 • 0, 01737 • 100 = 0, 267 5 5 Voр = m 100мл р-ра – 0, 25 атропина T 5мл р-ра - Х атропина X = 5 • 0, 25 = 0, 0125 100 Voр = 0, 0125 = 0, 72мл V1 = 0, 82ml 0, 01737 доп. откл =8% [0, 23 ÷ 0, 27]
2) Анализ NaCl Аргентометрия с поверхностно-действующим индикатором. Метод Фаянса к 1мл р-ра + 3кап бром-фенол-синий + укс к-та(р ) = пока фиолетовое окр. не перейдёт в зел-жёлт( 3кап) и титруют AgNO3 = до фиол. ос
NaCl + AgNO3 → AgCl↓ + NaNO3 V2 = 3, 2мл m(NaCl) = (V2 – 0, 05)*K2*T*10 = (3, 2 – 0, 05) • 1 • 0, 002922 • 100 = 0, 920 1 1 Voр = mT= 0, 002922 100 млр-ра – 0, 875 гNaCl T 1 мл р-ра – Х, X = 0, 00875
Voр = 0, 00875 = 2, 99 ml 0, 002922 доп. откл ±6% [0, 8225 ÷ 0, 9275] (таб. 7) | ||
Билет №1. Rp: Promedoli 0, 003, Analgini 0, 2, Saccari 0, 25
M. f. pulvis, D. t. d №10, S. по 1 порошку 3 раза в день
Сложный дозированный порошок для внутреннего применения, с веществами списка А и Б
 Проверка доз: Р — 0, 05 Prodosi 0, 003 Проверка доз: Р — 0, 05 Prodosi 0, 003
 Промедол ВProdie 0, 009
С — 0, 2 Дозы не превышены
Норма отпуска 0, 25 не превышена Промедол ВProdie 0, 009
С — 0, 2 Дозы не превышены
Норма отпуска 0, 25 не превышена
 АнальгинР — 1, 0 АнальгинР — 1, 0
 В Pro dosi 0, 2
С — 3, 0 Pro die 0, 6
Дозы не превышены
Количество Промедола 0, 003 • 10 = 0, 03
т. к кол-во промедола < 0, 05 то берем тритурацию промедола 1: 10
Количество тритурации 0, 03 • 10 = 0, 3
Количество Анальгина 0, 2 • 10 = 2, 0
Количество Сахара 0, 25 • 10 = 2, 5
Количество сахара с учетом тритурации 2, 5 – 0, 3 = 2, 2mобщ = 0, 3 + 2, 0 + 2, 2 = 4, 5
Теоретическое обоснование
Готовят по массе в ступке, в первую очередь в ступку помещают и растирают сахар, т. к. это кристаллическое в-во общего списка и выписано в большем количестве, далее в-ва добавляют по равилу приготовления порошков от меньшего кол-ва к большему (тритурация промедола и анальгин). Промедол находится на ПКУ – его тритурацию отвешивает провизор – технолог, оформляется обратная сторона рецепта «Triturationispromedoli 1: 10 0, 3 Отпустил, Принял, Дата» После проверки на однородность массу развешивают на 10 вощеных капсул. Этикетки: «Порошок», «Внутреннее», «Обращаться с осторожностью». Пакет опечатывают. Больному выдают сигнатуру.
ППК к рецепту № 13. 06. 2012 А
Saccari 2, 2
Triturationis Promedoli 1: 10 0, 3
Analgini 2, 0
mобщ = 4, 5 m1 = 0, 45
Приготовил: Проверил: Отпустил: В Pro dosi 0, 2
С — 3, 0 Pro die 0, 6
Дозы не превышены
Количество Промедола 0, 003 • 10 = 0, 03
т. к кол-во промедола < 0, 05 то берем тритурацию промедола 1: 10
Количество тритурации 0, 03 • 10 = 0, 3
Количество Анальгина 0, 2 • 10 = 2, 0
Количество Сахара 0, 25 • 10 = 2, 5
Количество сахара с учетом тритурации 2, 5 – 0, 3 = 2, 2mобщ = 0, 3 + 2, 0 + 2, 2 = 4, 5
Теоретическое обоснование
Готовят по массе в ступке, в первую очередь в ступку помещают и растирают сахар, т. к. это кристаллическое в-во общего списка и выписано в большем количестве, далее в-ва добавляют по равилу приготовления порошков от меньшего кол-ва к большему (тритурация промедола и анальгин). Промедол находится на ПКУ – его тритурацию отвешивает провизор – технолог, оформляется обратная сторона рецепта «Triturationispromedoli 1: 10 0, 3 Отпустил, Принял, Дата» После проверки на однородность массу развешивают на 10 вощеных капсул. Этикетки: «Порошок», «Внутреннее», «Обращаться с осторожностью». Пакет опечатывают. Больному выдают сигнатуру.
ППК к рецепту № 13. 06. 2012 А
Saccari 2, 2
Triturationis Promedoli 1: 10 0, 3
Analgini 2, 0
mобщ = 4, 5 m1 = 0, 45
Приготовил: Проверил: Отпустил:
|
Качественный химический контроль анальгина
1. Реакция кислотного гидролиза и доказательство входящего в состав молекулы формальдегидносульфитного производного. 0, 05 препарата нагревают с 0, 5мл разведеннойHCl. Сначала ощущается запах диоксида серы (SO2), а затем формальдегида
2. Реакция на восстановительную способность анальгина. 0, 05 препарата смачивают каплей воды + 2мл спирта + 5 кап HCl. После растворения препарата + 2мл 0, 1моль/л р-ра йодата калия. Раствор окрашивается в малиновый цвет, затем выделяется бурый осадок йода 5SO2 + 2KJO3 → 4SO3 + J2 + K2SO4 3. На Na Крупинку препарата внести в бесцветное пламя, пламя окрашивается в желтый цвет 4. Реакция внутриаптечного контроля с FeCl3 0, 05 препарата растворяют в 0, 5 мл воды + по 3кап HCl и FeCl3 = синее окрашивание, при стоянии переходящее в красное , затем р-р обесцвечивается | ||
БИЛЕТ №18. Rp: Sol. Papaverini hydrochloridi 2% 50ml
Steril!
D. S. По 1 мл 2 раза в день
Сложная жидкая лекарственная форма для инъекций, истинный раствор с сильнодействующим в-вом списка Б.
Папаверина1, 0
Воды для инъекций до 50мл
Теоретическое обоснование:
Готовят массо-объемным способом в асептических условиях, методом доведения до объема. Р-р не стабилизируют, т. к. папаверин не разлагается при стерилизации. Стерилизуют при 120ОС – 8минут. В мерной колбе в небольшом количестве воды растворяют папаверин, затем доводят до объема 50мл, фильтруют во флакон для отпуска через вату и складчатый фильтр, проверяют на чистоту, маркируют и закрывают под обкатку. После стерилизации раствор повторно проверяют на чистоту и оформляют к отпуску. Этикетки «Для инъекций», «Стерильно», «Хранить в прохладном защищенном от света месте».
ППКкрецепту № 12. 03. 2012
Agua pro injektionibus q. s.
Papaverini hydrochloridi 1, 0
Agua pro injektionibus ad 50ml
Vобщ = 50 ml
Приготовил: Проверил: № анализа 2/3 Подпись провизора-аналитика: Дата:
Формула папаверина гидрохлорида

|
ВАК папаверина гидрохлорида 2% 50 мл П: работа с требованием: правильность выписывания; наличие указаний о способе применения Дата, № требования, название или № отделения, ППК № ан-за, подпись пров-аналит: дозы не превышены, ВРД – 0, 2; ВСД – 0, 6 О: б/цв, прозр. жид-ть, б/видим. мех. вкл(провер-ся до и после стер-ции). Рез-ты к-ля – в «Журнал регистрации рез-тов органолепт., физ и хим к-ля» КПО: : в плот. укупор. таре. под металлическим колпачком Осн. этик: «Для инъекций», «Стерильно», На этикетке указаны состав л. с. на латинском языке и способ применения Sol. Papaverini hydrochloridi 2% - 50ml, в/в по 1 мл, наименование и адрес аптеки, № анализа (до и после стерилизации), дата, срок годности 30 суток, фамилии приготовившего, проверившего и отпустившего лекарственную форму. Предупр. этик: «Хр. в п. з от с. м. ».. О, Ф: ОБЯЗАТЕЛЬНО!!! Пров-ся до и после стер-ции, не < 5флак данной серии стер-ции Vo=50мл, доп. откл = ± 4% [ 48÷ 52 мл] таб. 5 ПХК ОБЯЗАТЕЛЕН!!! до стерилизации проверяют рН, ПХК папаверина; после стер. рН и ПХК папаверина Кач: 1) на основание папаверина а) к 1мл р-ра + HNO3(к) 1-2кап = жёлт. окр – при t* на вод. бане – оранж. окр б) к 1 мл р-ра + 1-2кап Н2SO4(к) при t* сине-фиолет. окр в) к 1 мл р-ра + реактив Марки 2-3кап при t*слабо нагревают на вод. бане = фиолет. окр 2) на HCl – к 1 мл р-ра + 1-2кап HNO3 + AgNO3 = бел. твор. осадок нерастворимый в азотной к-те Cl- + AgNO3 → AgCl↓ + NO3- Колич: 1)М-д нейтрализации – 1 + 3-5кап ф/фт и титруют 0, 1моль/л р-ром NaOH= до роз. окр (папаверин)*HCl+NaOH=(папаверин)+NaCl+H2O 1мл 0, 1моль/лNaOH соответствует 0, 03759г папаверина г/х Р: V = 0, 55мл m(папаверина) = V • K • T • 50 = 0, 55 • 1 • 0, 03759 • 50 = 1, 03 1 1 T=0, 3759 Voр = m 100 мл р-ра – 2, 0 папаверина T 1 мл р-ра - Х папаверина Х= 0, 02
Vор = 0, 02 = 0, 53мл 0, 03759 доп. откл = ±6% (таб 7) 1, 0 – 100% Х – 6% Х=0, 06 [0, 94 ÷ 1, 06]
2)Аргентометрия с адсорбционным индикатором. М-д Фаянса – 0, 22г пор р-рить в 2мл Н2О + 3кап бромфенол-синий + по каплям укс. к-ту(р) =до зел-жёлт. окр. Титруют 0, 1моль/л AgNO3 = до фиол. окр (папаверин)*HCl + AgNO3 = (папаверин)*HNO3 + AgCl↓
3)Меркуриметрия– 0, 22г пор р-рить в 2мл Н2О + 2-3кап 1% спирт. р-ра Дифенилкарбазона + 2-3кап HNO3титруют 0, 1 моль/л р-ром Hg(NO3)2 = сине-фиол. окр 2(папаверин)*HCl+Hg(NO3)2=2(папаверин)*HNO3 + HgCl2 | ||
Билет №3. Rp: Coffeini-natrii benzoatis 1, 0, Natrii bromidi 2, 0, Sirupi simpleci 5ml, Agua purificatae ad 200ml
M. D. S. по 1 столовой ложке 3 раза в день
Сложная жидкая лекарственная форма для внутреннего применения, с веществом списка Б, истинный раствор
Расчеты: Vобщ = 200мл
Количество приемов: 200: 15 = 13 приемов
 Проверка доз: Р — 0, 5 prodosi 1, 0: 13 = 0, 08 Проверка доз: Р — 0, 5 prodosi 1, 0: 13 = 0, 08
 Кофеин бензоат натрия Вprodie 0, 24
C — 1, 5 Дозы не превышены
% порошков: 2. 0 — 200мл х = 2, 0 • 100 = 1% < 3%
х — 100мл 200
количество натрия бромида: 2, 0 *5=10 мл
Количество натрия бензоата: 1, 0 • 5 = 5мл
Количество воды: 200 – 10- 5 = 180мл
Теоретическое обоснование:
Проверяют дозы. Готовят массо-объемным способом в фдо. Вода с учетом растворов-концентратов. Добавляют во флакон для отпуска 5мл концентрата кофеина бензоата натрия и в последнюю очередь 5мл сахарного сиропа.
Оформляют к отпуску. Этикетки: «Внутреннее», «Микстура», «Хранить в прохладном защищенном от света месте».
ППК к рецепту № 13. 06. 2012 Детское
Aguapurificatae 180ml
Р-р Natriibromidi1: 5 – 10 мл
Sol. Coffeini-natriibenzoatis 1: 5 — 5ml
Sirupisimpleci 5ml
Vобщ = 200ml
Приготовил: Проверил: Отпустил: Кофеин бензоат натрия Вprodie 0, 24
C — 1, 5 Дозы не превышены
% порошков: 2. 0 — 200мл х = 2, 0 • 100 = 1% < 3%
х — 100мл 200
количество натрия бромида: 2, 0 *5=10 мл
Количество натрия бензоата: 1, 0 • 5 = 5мл
Количество воды: 200 – 10- 5 = 180мл
Теоретическое обоснование:
Проверяют дозы. Готовят массо-объемным способом в фдо. Вода с учетом растворов-концентратов. Добавляют во флакон для отпуска 5мл концентрата кофеина бензоата натрия и в последнюю очередь 5мл сахарного сиропа.
Оформляют к отпуску. Этикетки: «Внутреннее», «Микстура», «Хранить в прохладном защищенном от света месте».
ППК к рецепту № 13. 06. 2012 Детское
Aguapurificatae 180ml
Р-р Natriibromidi1: 5 – 10 мл
Sol. Coffeini-natriibenzoatis 1: 5 — 5ml
Sirupisimpleci 5ml
Vобщ = 200ml
Приготовил: Проверил: Отпустил:
|
ВАК концентрированного раствора кофеин-бензоата натрия 20% Работа с рецептом не проводится П: Проверить записи в книге учета лабораторных и фасовочных работ Вода очищенная – 1740 мл Кофеин-бензоат натрия – 400, 0 КУО = 0, 65 Vобщ = 2000мл № анализа, подпись провизора-аналитика Оформление рез-тов анализа: заполнить «Журнал регистрации рез-тов органолептич. хим. к-ля внутриаптечной заготовки, лек. форм, изготовл. по индивид. рец-м»; поставить № анализа и подпись провизора-аналитика в книге учета лаб. и фасовочн. работ. О: бесцветная прозрачная ж-ть, без мех. включений Ф: контроль не проводится КПО: Больным не отпускается. Состоит в правильном оформлении концентрата. Этикетка «SolutioCoffeini-natriibenzoatis 20%»; дата приготовления, № серии, срок годности 20 дней при to не выше 25о или 15 дней при t - 3-5oC. Приготовил: проверил; № анализа ПХК: ОБЯЗАТЕЛЬНО полный Кач: а) р-ция образ-я полийодида кофеина – к 0, 5мл р-ра + 2кап 0, 1моль/л йода + 2кап НСl = бур. ос; б) на бензоат Na - + 1кап FeCl3 = жёлт-роз. ос
Колич: 1) Метод рефрактометрии С% = n – n(H2O) Fn(H2O) =1, 3330 F(коф-бенз 20%) = 0, 00192
С% = 1, 3710 – 1, 3330 = 19, 79% 0, 00192
Доп. откл. ± 2% [19, 6 ÷ 20, 4]
Формула кофеина-бензоата натрия
| ||
Качественный химический контроль димедрола и анальгина
Качественный химический контроль анальгина
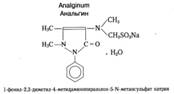 1. Реакция кислотного гидролиза и доказательство входящего в состав молекулы формальдегидносульфитного производного.
0, 05 препарата нагревают с 0, 5мл разведеннойHCl. Сначала ощущается запах диоксида серы (SO2), а затем формальдегида
1. Реакция кислотного гидролиза и доказательство входящего в состав молекулы формальдегидносульфитного производного.
0, 05 препарата нагревают с 0, 5мл разведеннойHCl. Сначала ощущается запах диоксида серы (SO2), а затем формальдегида
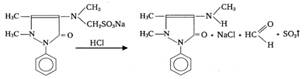 2. Реакция на восстановительную способность анальгина.
0, 05 препарата смачивают каплей воды + 2мл спирта + 5 кап HCl. После растворения препарата + 2мл 0, 1моль/л р-ра йодата калия. Раствор окрашивается в малиновый цвет, затем выделяется бурый осадок йода
5SO2 + 2KJO3 → 4SO3 + J2 + K2SO4
3. На Na Крупинку препарата внести в бесцветное пламя, пламя окрашивается в желтый цвет
4. Реакция внутриаптечного контроля с FeCl3
0, 05 препарата растворяют в 0, 5 мл воды + по 3кап HCl и FeCl3 = синее окрашивание, при стоянии переходящее в красное, затем р-р обесцвечивается
Качественный химический контроль димедрола
1. На основание димедрола
а) Реакция образования оксониевой соли. К 0, 1 порошка + 1-2кап концентрированной серной к-ты. Появляется желтое окрашивание, постепенно приобретающее оранжевый оттенок (оксониевая соль)
2. Реакция на восстановительную способность анальгина.
0, 05 препарата смачивают каплей воды + 2мл спирта + 5 кап HCl. После растворения препарата + 2мл 0, 1моль/л р-ра йодата калия. Раствор окрашивается в малиновый цвет, затем выделяется бурый осадок йода
5SO2 + 2KJO3 → 4SO3 + J2 + K2SO4
3. На Na Крупинку препарата внести в бесцветное пламя, пламя окрашивается в желтый цвет
4. Реакция внутриаптечного контроля с FeCl3
0, 05 препарата растворяют в 0, 5 мл воды + по 3кап HCl и FeCl3 = синее окрашивание, при стоянии переходящее в красное, затем р-р обесцвечивается
Качественный химический контроль димедрола
1. На основание димедрола
а) Реакция образования оксониевой соли. К 0, 1 порошка + 1-2кап концентрированной серной к-ты. Появляется желтое окрашивание, постепенно приобретающее оранжевый оттенок (оксониевая соль)
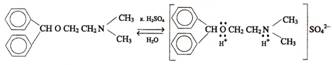 Качественный контроль сахара
К 0, 02 порошка + 1-2мл HCl и несколько кристаллов резорцина и кипятят 1 минуту – раствор окрасится в красный цвет
Качественный контроль сахара
К 0, 02 порошка + 1-2мл HCl и несколько кристаллов резорцина и кипятят 1 минуту – раствор окрасится в красный цвет
|
Билет №30. Rp: Dimedroli 0, 015; Analgini 0, 2; Sacchari 0, 3 M. f. pulvis, D. t. d №10, S. по 1 порошку 2 раза в день Сложный дозированный порошок для внутреннего применения, с веществами списка Б
С — 0, 25 Дозы не превышены
С — 3, 0 Prodie 0, 4 Дозы не превышены
Количество Димедрола 0, 015 • 10 = 0, 15 Количество Анальгина 0, 2 • 10 = 2, 0 Количество Сахара 0, 3 • 10 = 3, 0 mобщ = 0, 15 + 2, 0 + 3, 0 = 5, 15
Теоретическое обоснование Готовят по массе в ступке, в первую очередь в ступку помещают и растирают сахар, т. к. это кристаллическое в-во общего списка и выписано в большем количестве. Во вторую очередь добавляют Димедрол. Соотношение 1: 20 не превышено. В последнюю очередь добавляется анальгин. После проверки на однородность массу развешивают на 10 вощеных капсул. Этикетки: «Внутреннее»,
ППК к рецепту № 13. 06. 2012 Saccari 3, 0 Dimedroli 0, 15 Analgini 2, 0 mобщ = 5, 15 m1 = 0, 515
Приготовил: Проверил: Отпустил: | ||
Rp: Atropini sulfatis 0, 00025; Papaverini hydrochloridi 0, 02; Saccari 0, 8
M. f. pulvisD. t. d № 6 S. по 1 порошку 3 раза в день
Сложный дозированный порошок для внутреннего применения, с веществами списка А и Б
 Проверка доз: Р — 0, 001 Prodosi 0, 00025 Проверка доз: Р — 0, 001 Prodosi 0, 00025
 Атропин ВProdie 0, 00075
С — 0, 003 Дозы не превышены Атропин ВProdie 0, 00075
С — 0, 003 Дозы не превышены
 ПапаверинР — 0, 2 ПапаверинР — 0, 2
 В Prodosi 0, 02
С — 0, 6 Prodie 0, 06
Дозы не превышены
Количество Атропина 0, 00025 • 6 = 0, 0015 количество атропина меньше 0, 05 поэтому используем тритурацию 1: 100
Количество тритурации 0, 0015 • 100 = 0, 15
Количество Папаверина 0, 02 • 6 = 0, 12
Количество Сахара 0, 8 • 6 = 4, 8
Количество сахара с учетом тритурации 4, 8 – 0, 15 = 4, 65 mобщ = 4, 65 + 0, 12 + 0, 15 = 4, 92
Теоретическое обоснование
Готовят по массе в ступке, в первую очередь в ступку помещают и растирают сахар, т. к. это кристаллическое в-во общего списка и выписано в большем количестве. Количество сахара рассчитывается с учетом тритурации Во вторую очередь добавляют Папаверин, т. к его меньшее количество Соотношение 1: 20 превышено, поэтому часть растертого сахара отсыпают на капсулу и добавляют в конце приготовления порошка. В последнюю очередь добавляется тритурация атропина 1: 100. Оформляется обратная сторона рецепта. После проверки на однородность массу развешивают на 6 вощеных капсул. Этикетки: «Внутреннее», «Обращаться с осторожностью». Больному выдают сигнатуру.
ППК к рецепту № 13. 06. 2012 А
Saccari 4, 65
Papaverinihydrochloridi 0, 12
Triturationis Atropini sulfatis 1: 100 0, 15
mобщ = 4, 92 m1 = 0, 82
Приготовил:
Проверил:
Отпустил: В Prodosi 0, 02
С — 0, 6 Prodie 0, 06
Дозы не превышены
Количество Атропина 0, 00025 • 6 = 0, 0015 количество атропина меньше 0, 05 поэтому используем тритурацию 1: 100
Количество тритурации 0, 0015 • 100 = 0, 15
Количество Папаверина 0, 02 • 6 = 0, 12
Количество Сахара 0, 8 • 6 = 4, 8
Количество сахара с учетом тритурации 4, 8 – 0, 15 = 4, 65 mобщ = 4, 65 + 0, 12 + 0, 15 = 4, 92
Теоретическое обоснование
Готовят по массе в ступке, в первую очередь в ступку помещают и растирают сахар, т. к. это кристаллическое в-во общего списка и выписано в большем количестве. Количество сахара рассчитывается с учетом тритурации Во вторую очередь добавляют Папаверин, т. к его меньшее количество Соотношение 1: 20 превышено, поэтому часть растертого сахара отсыпают на капсулу и добавляют в конце приготовления порошка. В последнюю очередь добавляется тритурация атропина 1: 100. Оформляется обратная сторона рецепта. После проверки на однородность массу развешивают на 6 вощеных капсул. Этикетки: «Внутреннее», «Обращаться с осторожностью». Больному выдают сигнатуру.
ППК к рецепту № 13. 06. 2012 А
Saccari 4, 65
Papaverinihydrochloridi 0, 12
Triturationis Atropini sulfatis 1: 100 0, 15
mобщ = 4, 92 m1 = 0, 82
Приготовил:
Проверил:
Отпустил:
|
Качественный контроль атропина 1) на основание атропина (р-ция Витали-Морена) – 5 кап. р-ра преп-та + неск. кап. HNO3(к ) ивыпаривают = жёлт. осадок + 3 кап. спирт. р-ра KOH и ацетона = фиолет. окр (исчезает при стоянии)
2) к р-ру + р-р аммиака = бел. ос (основание атропина) 3) На H2SO4 к р-ру + ВаСl2 = бел. крист. ос (не р-рим в к-тах и щел) SO42- + BaCl2 = BaSO4 + 2Cl- 4)на Na –к р-ру + укс. к-та+цинк-уранил-ацетат= жёлт. крист. ос Na+ + Zn(UO2)3(CH3COO)8 + CH3COOH + 9H2O = Na(Zn(UO2)3(CH3COO)9)*9H2O + H+ 5)на Сl – к р-ру + HNO3 + AgNO3 = бел. тв. ос (р-рим в аммиаке, не р-рим в HNO3) Cl- + AgNO3 = AgCl + NO3-
Качественный контроль папаверина 1) на основание папаверина а) к 0, 02 порошка + HNO3(к) 1-2кап = жёлт. окр – при t* на вод. бане – оранж. окр б) к 0, 02 порошка + 1-2кап Н2SO4(к) при t* сине-фиолет. окр в) к 0, 02 порошка + реактив Марки 2-3кап при t*слабо нагревают на вод. бане = фиолет. окр 2) на HCl – к 0, 02 порошка + 1-2кап HNO3 + AgNO3 = бел. твор. осадок нерастворимый в азотной к-те Cl- + AgNO3 → AgCl↓ + NO3-
Качественный контроль сахара К 0, 02 порошка + 1-2мл HCl и несколько кристаллов резорцина и кипятят 1 минуту – раствор окрасится в красный цвет | ||
| Rp: Sol. Natrii hydrocarbonatis 5% - 100ml Steril! D. S. Для в/в введения Сложная жидкая лекарственная форма для инъекций, истинный раствор. Натрия гидрокарбоната5, 0 Вода для инъекцийдо 100 мл Теоретическое обоснование Готовят массо-объемным способом в асептических условиях, методом доведения до объема. В качестве растворителя используют воду для инъекций. Р-р не стабилизируют, т. к. натрия гидрокарбонат не разлагается при стерилизации. Стерилизуют паровым методом при 120ОС – 8минут. В мерной колбе в небольшом количестве воды растворяют натрия гидрокарбонат, затем доводят до объема 100мл, фильтруют во флакон для отпуска через вату и складчатый фильтр, проверяют на чистоту, маркируют и закрывают под обкатку. После стерилизации раствор повторно проверяют на чистоту и оформляют к отпуску. Флакон для отпуска заполняют раствором на 2/3, т. к при стерилизации выделяется CO2, После стерилизации оставить флакон на 2 часа чтобы выделившийся газ вновь перешел в раствор. Этикетки «Для инъекций», «Стерильно», «Хранить в прохладном защищенном от света месте». ППКкрецепту № 13. 06. 2012 Agua pro injektionibus q. s. Natrii hydrocarbonatis 5, 0 Agua pro injektionibus ad 100ml Vобщ = 100 ml Приготовил: Проверил: № анализа 2/3 Подпись провизора-аналитика: Дата: | ВАК натрия гидрокарбоната 5% - 100мл П: : работа с требованием: правильность выписывания; наличие указаний о способе применения Дата, № требования, название или № отделения, № ан-за 2/3, подпись пров-аналит Проверка ППК – пригот., провер., Режим стерилизации при120*С – 8мин. Оформление рез-тов в «Журнале регистраций результатов орг-лепт, физ и хим к-ля» О: б/цв, прозр. р-р, б/зап и мех. вкл(провер. до и после стер-ции мех. вкл) КПО: отпуск-ся во флак., где р-р занимает 2/3 V, т. к. при стер-ции выдел-ся СО2 и м. разорвать флакон; флакон закрыт под обкатку, чтобы СО2 не улетучивался. Осн этик: «Внутреннее. Для инъекций. Стерильно». Предупр. этик: «Хр. в пр. з. от. св. м». Если треб-е ЛПУ, то – на этик. указ-ся название и адрес аптеки, № б-цы, название отделения, состав на латин. яз., способ употреб., дата изгот-я, годен 30дн., подписи приготовил, проверил, отпустил, № ан-за. О, Ф: ОБЯЗАТЕЛЕН!!! Проверка Vo и герметич-ти укупорки. Vo=100ml. (таб 5) доп. откл. ±3% [97-103мл] ПХК ОБЯЗАТЕЛЕН!!! Кач: 1)Na: р-р подкисляют укс. к-той + реактив цинк-уранил ацетат = св. - жёлт. крист. ос
Na+ + Zn(UO2)3(CH3COO)8 + CH3COOH + 9H2O = Na(Zn(UO2)3(CH3COO)9)*9H2O + H+
2) НСО3: к 4-5кап р-ра + 2-3кап развед. НСl = пуз. углек. газа NaHCO3 + HCl = NaCl + H2O + CO2
Колич: М-д нейтрализации – 2мл р-ра помещ. в колбу на 50мл, доводят Н2О до метки, перемешать. К 5мл разведения + 1кап метил-оранж и титруют 0, 1 моль/л НСl = до роз. окр NaHCO3 + HCl = NaCl + H2O + CO2 Р: Т=0, 0084 г/моль 100мл – 5, 0г 2мл – Х Х=0, 1г 0, 1г – 50мл Х - 5мл Х=0, 01г Voр= m = 0, 01 =1, 2ml T 0, 0084 V= 1, 142 ÷ 1, 238 m=V*K*T*V(колбы)*100 = V*K*T*50*100 = 1, 15 *1*0, 0084*50*100 = 4, 83 Q*V(min) 2*5 2*5
Доп. откл ±4% (таб 7) 5, 0г – 100% Х – 4% Х=0, 2 [4, 8-5, 2г] | ||
|
БИЛЕТ №9. Rp: Inf. Radix Althaeae ex 2, 0 — 100ml; Natrii hydrocarbonatis 2, 0; Elixiris pectoralis 2ml M. D. S. по 1 столовой ложке 3 раза в день Сложная жидкая лекарственная форма для внутреннего применения, конденсационная суспензия за счет грудного эликсира, водная вытяжка из сырья содержащего слизи. Расчеты: Vобщ = 102 мл Кол-во экстракта-концентрата алтея сухого 1: 1 —2, 0 Количество концентрата натрия гидрокарбоната: 2, 0 • 20 = 40мл % порошков: 2, 0 — 105мл х = 2, 0 • 100 = 1, 9% < 3% КУО не х — 100мл 105 учитываем Количество воды: 105 42 = 63мл Теоретическое обоснование: Готовят массо-объемным способом в подставке, количество воды берут без учета КУО, т. к. % порошков < 3% и за вычетом концентрированного раствора. Сухого экстракта-концентрата берут столько же сколько и РЛС. В первую очередь в подставке растворяют экстракт-концентрат, раствор фильтруют во флакон для отпуска. Добавляют концентрат натрия гидрокарбоната. Отдельно в подставке смешивают 5мл полученного раствора с грудным эликсиром, эту смесь добавляют частями во флакон для отпуска. Оформляют к отпуску. Этикетки: «Внутреннее», «Микстура», «Хранить в прохладном защищенном от света месте», «Перед употреблением взбалтывать» На обратной стороне рецепта указываем: Ext. RadixAlthaeaesicci 1: 1 — 3, 0 ППК к рецепту № 13. 06. 2012 Aguapurificatae 110ml Ext. Radix Althaeae sicci 1: 1 — 3, 0 Sol Natrii hydrocarbonatis 1: 5 — 10ml Elixirispectoralis 5ml Vобщ = 102ml
|
ВАК концентрата натрия гидрокарбоната 5% 2л Работа с рецептом не проводится П: Проверить записи в книге учета лабораторных и фасовочных работ Вода очищенная – 1970 мл Натрия гидрокарбонат – 100, 0 КУО = 0, 3 Vобщ = 2000мл № анализа, подпись провизора-аналитика Оформление рез-тов анализа: заполнить «Журнал регистрации рез-тов органолептич. хим. к-ля внутриаптечной заготовки, лек. форм, изготовл. по индивид. рец-м»; поставить № анализа и подпись провизора-аналитика в книге учета лаб. и фасовочн. работ. О: бесцветная прозрачная ж-ть, без мех. включений Ф: контроль не проводится КПО: Больным не отпускается. Состоит в правильном оформлении концентрата. Этикетка «Solutionatriihydrocarbonatis 5%»; дата приготовления, № серии, срок годности 4 дня при to не выше 25о или 10 дней при t - 3-5oC. Приготовил: проверил; № анализа ПХК: ОБЯЗАТЕЛЬНО полный Качественный1) на Na+Чать р-ра на графитовой палочке вносят в бесцветное пламя. Пламя окраш. в желтый цвет 2) на HCO3- к 4-5 кап р-ра +2-3 кап разб HCl = пузырьки углекислого газа NaHCO3 + HCl = NaCl + H2O + CO2↑ КоличественныйМетод нейтрализациик 1 мл р-ра + 1кап метилоранжа и титруют 0, 1моль/л р-ром HCl до розового окрашивания NaHCO3 + HCl = NaCl + H2O + CO2↑ Т = 0, 0084 V= 5, 9 ml % гидрокарб = V• K • T • 100 = 5, 9 • 1 • 0, 0084 • 100 = 4, 956 % Доп. откл. ±2% [4, 9 ÷ 5, 1%] 1 1 Vор = m = 0, 05 = 5, 95мл T 0, 0084 | ||
|
БИЛЕТ № 7. Rp: Sol. Dibazoli 0, 5% - 100ml Steril! D. S. Для в/в введения Сложная жидкая лекарственная форма для инъекций, с веществом списка Б, истинный раствор. Расчеты: Vобщ = 100 мл Дибазол – состоит из слабого основания и сильной к-ты, поэтому стабилизируем 0, 1М р-ром HCl Кол-во стабилизатора: 10 мл – 1000мл р-ра Х = 10 • 100 = 1 мл Х мл - 100 мл р-ра 1000
Теоретическое обоснование: Готовят массо-объемным способом в асептических условиях, в мерной колбе, методом доведения до объема, т. к. раствор для инъекций. Раствор фильтруют через вату и складчатый фильтр, проверяют на чистоту, маркируют и закрывают под обкатку. Стерилизуют паровым методом при t = 120ОС 8 минут, т. к. объем р-ра 100 мл. После стерилизации раствор повторно проверяют на чистоту и оформляют к отпуску. Этикетки «Для инъекций», «Стерильно», «Хранить в прохладном защищенном от света месте». ППКкрецепту № 13. 06. 2012 Agua pro injektionibus q. s. Dibazoli 0, 5 Sol. Acidi hydrohloridi 0, 1M 1ml Agua pro injektionibus ad 100ml Vобщ = 100 ml Приготовил: Проверил: № анализа 2/3 Подпись провизора-аналитика: Дата:
Формула Дибазола
| Химический контроль дибазола П: : проверка правильности выписывания рецепта (107-у), проверка ппк (переписать из тлф). № ан-за, подпись пров-аналит: дозы не превышены. Режим стер-ции 120оС – 8мин. Проверка записей в «Журнале регистрации рез-тов контроля отдельных стадий изготовления р-ров для инъекций и инфузий». Органолептический контроль: б/цветная, прозрачная ж-ть, б/зап и видимых мех. включений (провер-ся до и после стер-ции) КПО: в плот. укупор. таре. под металлическим колпачком Осн. этик: «Для инъекций», «Стерильно», На этикетке указаны состав л. с. на латинском языке и способ применения «Sol. Dibazoli 1% - 100ml, для в/в введения», наименование и адрес аптеки, номер рецепта, фио больного, № анализа (до и после стерилизации), дата, срок годности 30 суток, фамилии приготовившего, проверившего и отпустившего лекарственную форму. Предупр. этик: «Хр. в п. з от с. м. ». Физический к.: ОБЯЗАТЕЛЕН для каж. серии ЛФ, требующих стер-ции в кол-ве не < 5флак. Проводится после расфасовки до стер-ции. До стер-ции Vо=100мл доп. откл = ±3% (т. 5) [97-103] 100мл – 100% Х – 3% Х=3мл Проверяется кач-во укупорки. ПХК ОБЯЗАТЕЛЕН до и после стерилизации!!! До стер-ции проверяют рН и ПХК дибазола и стаблизатора 0, 1моль/лHCl; после стер-ции – рН и ПХК дибазола (отбирается 1 флакон р-ра от каждой серии) и отсутствие механических включений Кач: 1) на основание дибазола – р-ция образования полийодида дибазола в кислой среде – к 0, 5 мл преп-та + 3кап. разведеной НСl и 3 кап. 0, 1М р-ра йода =взбалтывают= красновато-серебристый ос. (диб)*HJ*J2 2) наНСl а) к 5мл р-ра + 1кап метил-оранж = роз. окр б) на Сl– к 0, 5мл р-ра + 0, 5мл р-ра аммиака = осадок отфильтровать + 1мл HNO3(р) + 3кап AgNO3= белый творожистый осадок Cl- + AgNO3 → AgCl + NO3- Колич: М-д нейтрализации в спирто-хлороформенной среде – к 5мл р-ра+3мл хлороформа – титруют 0, 1моль/л р-ром NaOH при взбалтывании до роз. окр водн. слоя Инд – ф/фт 3кап. (при этом титруется сумма компонентов: дибазол + стаб-р НСl) (диб)*HCl + NaOH → (диб) + NaCl + H2O Расчеты: Расчёт кол-ва 0, 1моль/л НСl в 5мл исслед. р-ра в 100мл р-ра – 1мл НСl; в 5мл р-ра – Х, Х = 0, 05мл НСl На титрование 0, 05мл 0, 1М НСl расходуется 0, 05 мл 0, 1М р-ра NaOH, Следовательно на титрование дибазола пойдет (V – 0, 05) мл р-ра NaOH V = 1, 03 m = (V – 0, 05)*K*T*100 = (1, 03 – 0, 05) • 1 • 0, 02447 • 100 = 0, 48 5 5 1, 0 – 100мл Х - 5мл, Х = 0, 05 Vор. общ = 2, 04 + 0, 05=2, 09
Voр = m= 0, 05 = 1, 02 (+0, 05 ашхлор) = 1, 07 мл T 0, 01172
доп. откл ±8% (т. 7) 1, 0 – 100% Х – 8%, Х=? [0, 46-0, 54] | ||
|
К билету № 6 Методы количественного определения Новокаина (необязательно) 1) Колич. опред-е стабилизатора в ЛФ – М-д нейтрализации на инд. метил-красн. – 10мл р-ра титруют 0, 02моль/л р-ром едкого натра = желт. окр. (инд – 1кап метил-красн – V1) HCl+NaOH=NaCl+H2O 1мл 0, 02 моль/л р-ра едк. натра соответ. 0, 0007292г НСl 0, 3646 – сод-е газа хлористого водорода в 100мл 0, 1 моль/л р-ра НСl, в граммах Доп. откл=+4% (2, 88-3, 12) Vмл(НСl)=V1*0, 0007292*1000*100 10*0, 3646 2)Колич. опред-е новокаина Колич. опред-е суммы стабилизатора и новокаина - а) М-д нейтрализации на инд. ф/фт (рН=8, 2-10, 0) – к 5мл р-ра + 5мл спирто-хлороформенной смеси, нейтрализованной ф/фт и титруют 0, 1моль/л р-ром едк. натра (NaOH ) = до роз. окр водн. слоя(V2) HCl+NaOH=NaCl+H2O 1мл 0, 1моль/л р-ра NaOH соотв. 0, 02728г новокаина V1*K1 m(нов)=(V2*K2 – 2*5 )*T*1000 5 Где: 1/2 – выравнивание объёмов навесок; 1/5 – выравн-е концентраций титрованных р-ров
Rp: Sol. Protargoli 1% 10ml M. D. S. Капли в нос Сложная жидкая лекарственная форма для наружного применения, коллоидный раствор. Расчеты: Vобщ = 10 мл % порошков < 3% Теоретическое обоснование: Готовят массо-объемным способом. Не указан растворитель, поэтому берут воду очищенную, % порошков < 3% поэтому воду рассчитывают без учета КУО. Мерным цилиндром отмеривают 10 мл воды и переливают ее в выпарительную чашку. На спец. весах для красящих веществ отвешивают протаргол. Рассыпают его по поверхности воды тонким слоем и оставляют для набухания и растворения. Раствор нельзя перемешивать, т. к. из-за большого содержания белка могут образовываться комочки. После полного растворения вещества раствор перемешивают стеклянной полочкой и фильтруют через рыхлый тампон ваты во флакон для отпуска. Этикетки «Капли в нос», «Наружное», «Хранить в прохладном защищенном от света месте» ППК к рецепту № 13. 06. 2012 Agua purificatae 10, 0 Protargoli 0, 1 Vобщ = 10ml
Приготовил: Проверил: Отпустил:
|
К билету № 6 (продолжение) Методы количественного определения Новокаина (необязательно) б) Аргентометрия по Мору – к 5мл р-ра + 1кап хромата К и титруют 0, 1 моль/л AgNO3 = кирпич-крас. окр(V2) T=0, 02728г/мл (новок)*HCl + AgNO3 = (новок)*HNO3 + AgCl HCl + AgNO3 = AgCl + HNO3 2AgNO3 + K2CrO4 = Ag2CrO4 + 2KNO3 в) Аргентометрия по Фаянсу – к 5мл р-ра + 3кап бромфенол-синего + по каплям укс. к-ту (р)= до зел-жёл. окр(-3кап). Титруют 0, 1моль/л AgNO3 = до фиол. окр (V2) (новок)*HCl + AgNO3 = (новок)*HNO3 + AgCl HCl + AgNO3 = AgCl + HNO3 г) Меркуриметрия – к 5мл р-ра + 1-2кап HNO3(р )+ 3кап 1% ДФК и титруют 0, 1моль/л р-ром Hg(NO3)2 = до исчезновения фиол. окр (V2) (новок)*HCl+Hg(NO3)2=2(новок)*HNO3+HgCl2 2HCl+Hg(NO3)2=HgCl2+2HNO3 Колич. опред-е новокаина м-дом нитритометрии (стабилизатор определению не мешает) К 5мл р-ра + 1мл НСl(р); 0, 2г калия бромида (катализатор р-ции диазотир-я); 2 кап тропеолина ОО и 1кап метилен-синий. Титруют 0, 1моль/л р-ром NaNO2 = до перехода крас-фиол. окр в голубое. Титрование ведут вначале по 0, 2-0, 3мл в мин, а в конце титрования (за 0, 1-0, 2 мл до точки эквивалентности) по 1-2кап в мин (V2) Т=0, 02728г/мл m(нов)=V2*K2*T*1000 5 Химический контроль Протаргола П: работа с Rp - проверка правильности выпис-я Rp – ф 107у, штамп ЛПУ, печать и подпись врача, печать для Rp, указания о способе прим-я, проверка совместим-ти ингредиентов; ППК:, Дата, № Rp, приг., провер., №ан-за, подп. пров-анал. О: жид-ть тём-корич. цв, б/мех. вкл КПО: в соотв. с физ-хим св-ми отпускают в герметич. укуп. флаконе оранж. стекла; осн. этик: «Наружное», доп: «Хр. в прох. з. от св. месте»; на этикетке: состав ЛС: Раствор протаргола 1% - 10 мл, на этикетке указаны № и местонахождение аптеки, № Rp, фамилия и возраст больного, назначение врача, дата изготовления, срок годности, цена, подписи: приготовил, проверил, отпустил. № и фамилия больного на этикетке соответствуют № и фамилии на рецепте. О, Ф: Vo=10ml, доп. откл ±8% [9, 2 ÷ 10, 8мл]. Проверка герметич-ти укупорки
Хим к-ль – ВЫБОРОЧНО Кач: 1)р-ция на белок – к 0, 5мл р-ра + 3-5кап НСl(р)– t* до кипения, фильтруют + 5кап NaOH + 1кап CuSO4 = фиол. окр – р-ция на полипептидные связи, имеющ-ся в белках (биуретова р-ция)
│ │ │ пептидная связь (в белке таких связей много) OH 2) к неск. кап. р-ра + 2кап НСl(р)при t* = желтеет, появляется муть Колич: М-д роданометрии – 1мл р-ра в колбу д. титрования + по кап НNO3(р) при t* - до осветления + 0, 5мл железо-аммониевых квасцов – титруют 0, 02 моль/л роданида аммония = до жёлтовато-розового окр Под дей-ем НNO3 разруш-ся белк. часть молекулы и Ag переходит в ионогенное состояние (обр-ся АgNO3) AgNO3 + NH4CNS → AgCNS + NH4NO3 FeNH4(SO4)2 + 3NH4CNS → Fe(CNS)3 + 2(NH4)2SO4 Р: 1мл 0, 02 моль/л р-ра NH4CNS соотв-ет 0, 0270г протаргола. Протаргол в среднем сод-т 8% Ag, поэтому вводится Тусл; М = 107, 9
Т= f • Cf • M = 1 • 0, 02 • 107, 9 = 0, 002158 Tусл = T • 100 = 0, 002158 • 100 = 0, 0270 1000 1000 8 8 V = 0, 35ml m = V • K • Tусл • 10 = 0, 35 • 1 • 0, 0270 • 10 = 0, 0945 доп. откл ±15% [0, 085 ÷ 0, 115] 1 1
Vор = m(навески) 1г – 100мл Vор = 0, 01 = 0, 37мл Тусл Х – 1мл 0, 0270 Х=0, 01г | ||
|
БИЛЕТ № 14. Rp: Sol. Novokaini 1% - 50ml натрия хлорида к. с. Steril! D. S. Для в/м введения Сложная жидкая лекарственная форма для инъекций, с веществом списка Б, истинный раствор
Стабилизатор на 1% новокаин 9мл - 1000 мл р-ра Х = 9 • 50 = 0, 45мл 20 кап – 1 мл Х мл – 50 мл р-ра 1000 х кап – 0, 45 = 9 капель Е=0, 18 0, 18 – 1 и х – 0, 5 = 0, 09 нахлор 0, 9-100 и х – 50 = 0, 45. 0, 45 – 0, 09 = 0, 36 нахлор. Теоретическое обоснование Готовят массо-объемным способом в асептических условиях, в мерной колбе, методом доведения до объема, т. к. раствор для инъекций. При стерилизации новокаин частично теряет свои анальгезирующие свойства, поэтому добавляем стабилизатор – 0, 1 моль/л р-р HCl – 9 мл на 1 литр Раствор фильтруют через вату и складчатый фильтр, проверяют на чистоту, маркируют и закрывают под обкатку. Стерилизуют паровым методом при t = 120ОС 8 минут, т. к. объем р-ра 50 мл. После стерилизации раствор повторно проверяют на чистоту и оформляют к отпуску. Этикетки «Для инъекций», «Стерильно», «Хранить в прохладном защищенном от света месте». ППК к рецепту № 13. 06. 2012
Вз: Aq. proinjectionibusq. s. Nоvocaini 0, 5 Натрия хлорида 0, 36 Sol. Ac. hydrochlorici 0, 1моль/л – 0, 45 ml ( gttsIX) Aq. pro injectionibus ad 50ml Vo= 50ml Приготовил: Проверил: № анализа 2/3 Подпись провизора-аналитика: Дата:
Формула новокаина
|
ВАК р-ра новокаина 1% - 50 мл
П: работа с требованием – проверка правильности выпис-я доз в соотв-ии с возрастом б-ного(дозы не превышены), наличие указаний о способе применения. ППК – дата, № треб-я, хир. отд. б-цы №3 пригот., провер., № ан 2/3, подп. пров-анал, расфасовал Режим стерилизации 120*С – 8мин; запись в «Журн. рег. рез. к-ля отд. стадий изгот. р-ров для инъекций и инфузий» О: б/цв, прозр. жид-ть б/видим. мех. вкл(отсут-ие мех вкл. опред-ся до и после стер-ции) КПО: флаконы закрыты под обкатку; осн. этик: «Для инъекций». Предупр: «Стерильно. Хр. в пр. з. от св. м. Беречь от детей» На этикетке: состав ЛС на лат. яз, способ прим-я – Sol. Novocaini 1% - 50ml. Внутримышечно. Наимен-е и адрес аптеки, № б-цы, отделение, № ан-за 2/3, годность – 30дн, ФИО приготовившего, проверившего, отпустившего ЛС, дата. Список Б: ВРД и ВСД=0, 1г в/м О, Ф: ОБЯЗАТЕЛЕН!!! ДО СТЕРИЛИЗАЦИИ!!! Vo = 50ml доп. откл ±4% [48 ÷ 52 мл] проверка кач-ва укупорки ПХК ОБЯЗАТЕЛЕН!!! ДО И ПОСЛЕ СТЕР-ЦИИ. До стер-ции – рН=3, 8-4, 5, ПХК новокаина и стабилизатора (0, 1моль/л НСl). После – рН и ПХК новокаина. Кач: 1)на НСl (стабилизатор) – к 1мл р-ра + 1кап метил-красн = красн. окр 2) на основание новокаина (на аминогруппу) – а) р-ция диазотирования и сочетания с β -нафтолом – к 0, 5мл р-ра + 0, 5мл HCl(р ) + 0, 5мл NaNO2 = вылить в пробирку с 0, 5мл в-нафтола = оранж. окр.
б) лигниновая проба – 2кап р-ра на бумаж. капс. + 1-2кап HCl(р) =оранж. пятно
в) лёгкая окисляемость за счёт аминогруппы – к 0, 5мл + 1кап Н2SO4 + 1кап 0, 01моль/л KMnO4 = обесцвеч-е р-ра 3)на Сl – к 2-3кап + 1-2кап AgNO3 = бел. твор. ос (р-рим в р-ре аммиака) Cl- + AgNO3 = AgCl + NO3- Колич: Новокаин и стабилизатор (НСl) оказывают влияние на количественный анализ друг друга, т. к. оба обладают кислыми свойствами и способны титроваться щелочью NaOH. В анализе используют различия в степени основности этих двух кислот. Свободная HCl можнт быть оттитрована на индикатор метиловый красный, интервал перехода окраски которого сдвинут в кислую сторону. Новокаин в этих условиях титроваться не будет 3)Cтупенчатое титрование стабилизатора и новокаина м-дом нейтрализации на разные индикаторы. Расчеты сделаны на 50мл р-ра а) Количественное определение стабилизатора (HCl) 10мл р-ра титруют 0, 02моль/л р-ром едк. натрадо жёлт. окр. Инд – 1кап метилен-красный(V1) HCl + NaOH = NaCl + H2O
T=0, 0007292 г/мл V1 = 0, 43мл Vмл(HCl)= V1 • 0, 0007292 • 50 • 100 = 0, 44 • 0, 0007292 • 50 • 100 = 0, 43 мл 10 • 0, 3646 10 • 0, 3646 доп. откл ±8% [0, 414 ÷ 0, 486] Vор = 0, 09 • 0, 3646 = 0, 45ml 0, 0007292 • 100 б) Количественное определение новокаина К оттитрованному выше р-ру + 5мл спирто-хлороформенной смеси (+ ф/фт – 5кап 0, 1моль/л (V2)) и титруют 0, 1моль/л р-ром едк. натра (NaOH ) = роз. окр.
Т=0, 02728 г/мл (новок)*HCl + NaOH = (новок) + NaCl+ H2O
V2 = 3, 9мл m(нов) = V2 • K2 • T • 50 = 3, 9 • 1 • 0, 02728 • 50 = 0, 53 г Vор = 0, 1 = 3, 67 мл 10 10 0, 02728 доп. откл +8% [0, 46 ÷ 0, 54] | ||
|
БИЛЕТ №4. Rp: Inf. Rhizomata сum radices Valerianae 180ml; Natrii bromidi 4, 0; TincturaeLeonuri 5ml M. D. S. по 1 столовой ложке 3 раза в день Сложная жидкая лекарственная форма для внутреннего применения, с веществом списка Б, конденсационная суспензия за счет настойки пустырника, водная вытяжка из сырья содержащего эфирные масла. Расчеты: Vобщ = 185мл
Кол-во сырья валерианы: 1: 30 → 180: 30 = 6, 0 Кол-во экстракта-концентрата валерианы 1: 2 — 6, 0 • 2 = 12мл % порошков: 4, 0 — 185мл х = 4, 0 • 100 = 2, 16% < 3% КУО не х — 100мл 185 учитываем Количество воды: 185 – 5 -5 - 12 = 163мл
Теоретическое обоснование: Готовят массо-объемным способом в подставке, количество воды берут без учета КУО, т. к. % порошков < 3% и за вычетом экстракта-концентрата и концентрированного раствора. Не указана концентрация вытяжки – из данного сырья готовят вытяжку 1: 30, жидкого экстракта берут в 2 раза больше чем РЛС. В первую очередь в подставке растворяют NaBr, раствор фильтруют во флакон для отпуска. Добавляют концентрат кофеина-бензоата натрия и экстракт-концентрат валерианы. В последнюю очередь добавляется настойка пустырника, т. к. она содержит этиловый спирт. Оформляют к отпуску. Этикетки: «Внутреннее», «Микстура», «Хранить в прохладном защищенном от света месте», «Перед употреблением взбалтывать» На обратной стороне рецепта указываем: Ext. Valerianae fluidum 1: 2 — 12ml ППКкрецепту №13 13. 06. 2012 Agua purificatae 163ml Р-рNatrii bromidi 1: 5 20мл Ext. Valerianae fluidum 1: 2 — 12ml Tincturae Leonuri 5ml Vобщ = 185ml
Приготовил: Проверил: Отпустил:
|
ВАК концентрата NaBr (1: 5) 20% 1000 мл
Работа с рецептом не проводится П: Проверить записи в книге учета лабораторных и фасовочных работ Вода очищенная – 1970 мл Натрия гидрокарбонат – 100, 0 КУО = 0, 3 Vобщ = 2000мл № анализа, подпись провизора-аналитика Оформление рез-тов анализа: заполнить «Журнал регистрации рез-тов органолептич. хим. к-ля внутриаптечной заготовки, лек. форм, изготовл. по индивид. рец-м»; поставить № анализа и подпись провизора-аналитика в книге учета лаб. и фасовочн. работ. Хранить в защищенном от света месте. О: бесцветная прозрачная ж-ть, без мех. включений Ф: контроль не проводится КПО: Больным не отпускается. Состоит в правильном оформлении концентрата. Этикетка «Solutionatriibromidi 20%»; дата приготовления, № серии, срок годности 20 дней при to не выше 25оC. Приготовил: проверил; № анализа ПХК: ОБЯЗАТЕЛЬНО полный Кач: 1)Na+ – к 0, 5мл р-ра + 2кап укс. к-ты + 2кап Zn-уранил ацетата = жёлт. крист. ос NaBr + Zn(UO2)3(CH3COO)8 + CH3COOH + 9H2O = Na(Zn(UO2)3(CH3COO)9)·9H2O↓ + HBr 2) Br- а) к 1-2 кап р-ра на часовом стекле + 1-2 кап р-ра AgNO3 = желтоватый осадок, трудно растворимый в р-ре аммиака NaBr + AgNO3 → AgBr↓ + NaNO3 бл. -желт. б) - к 0, 5мл р-ра + 0, 5мл хлороформа + 0, 5мл HCl + неск. кап. р-ра хлорной извести, взбалтывают. Хлороформный слой окраш в желто-оранжевый цвет CaOCl2 + 2HCl → CaCl2 + H2O + Cl2↑ 2NaBr + Cl2 → Br2 + 2NaCl Колич: Если будет концентрат, то Метод рефрактометрии С% = n – n(H2O) F n(H2O) =1, 3330 F(NaBr 20%) = 0, 0013
С% = 1, 3587 – 1, 3330 = 19, 76% 0, 0013
Доп. откл. ± 2% [19, 6 ÷ 20, 4] | ||
|
Rp: Acidi salicylici 0, 05; Resorcini 0, 1; Mentholi 0, 1; Vaselini; Lanolini aa 10, 0 M. D. S. Смазывать кожу Сложная мягкая лекарственная форма для наружного применения, комбинированная мазь Расчеты: mобщ = 0, 05 + 0, 1 + 0, 1 + 10, 0 + 10, 0 = 20, 25 % порошков для мази суспензии 0, 15 — 20, 25 х = 0, 15 • 100 = 0, 74% < 5% х — 100, 0 20, 25
Теоретическое обоснование: Готовим по массе в ступке, каждый тип мази отдельно. Ментол растворим в вазелине, и образует мазь-раствор. Масса мази меньше 30, 0 поэтому основу не расплавляем, а подогреваем ступку. Целесообразно начинать приготовление мази именно с мази-раствора. Для мази суспензии рассчитываем % порошков, он меньше 5%, поэтому салициловую кислоту и резорцин растираем с родственной к основе жидкостью – вазелиновым маслом. Салициловую кислоту нельзя растирать в сухом виде, ее растирают с родственной к основе жидкостью. В первую очередь в ступке растирают резорцин, затем добавляют салициловую кислоту и вазелиновое масло, все растирают и добавляют вазелин. В конце все мази смешать и добавить безводный ланолин, т. к. растворенный резорцин может привести к некрозу тканей и поэтому нельзя допустить растворения резорцина. Этикетки «Мазь», «Наружное», «Хранить в прохладном защищенном от света месте» ППК к рецепту № 13. 06. 2012 t Mentholi 0, 1 Vaselini 1, 0 Resorcini 0, 1 Olei Vaselini q. s. Acidi salicylici 0, 05 Vaselini 9, 0 Lanolini anhydrici 10, 0 mобщ = 20, 25
Приготовил: Проверил: Отпустил: |
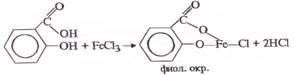
Химический контроль салициловой кислоты Качественный контроль: 1) Реакция с FeCl3 К 0, 1г мази + 2мл H2O и кипятят 1 минуту на водяной бане до расплавления основы. После охлаждения к водному извлечению + 1-2 кап FeCl3 Появляется фиолетовое окрашивание
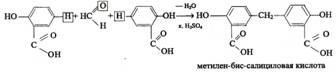
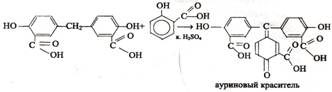
2) Реакция образования ауринового красителя. В фарфоровую чашку помещают салициловую кислоту + конц. H2SO4 и 1-2 кап. р-ра формальдегида. Появляется красное окрашивание
Количественный: Метод нейтрализации в спиртовой среде. 0, 5г мази отвешиваем на пергаментной бумаге и помещаем в стаканчик д/титрования + по 4-5мл спирта и хлороформа, нейтрализованных по ф/ф, и нагревают на вод. бане при темп. 50-55*С 10мин. Охлажд. и + 2-3кап. ф/ф и титруем 0, 1моль/л р-ром NaOH до розового окрашивания водного слоя.
T = 0, 01381г mг = V • K • T • 20, 25 0, 5 | ||
|
Rp: Platyphyllini hydrotartratis 0, 002; Papaverini hydrochloridi 0, 03; Saccari 0, 2 M. f. pulvisD. t. d № 6 S. по 1 порошку 2 раза в день Сложный дозированный порошок для внутреннего применения, с веществами списка А и Б
С — 0, 03 Дозы не превышены
С — 0, 6 Prodie 0, 06 Дозы не превышены Количество Платифилина 0, 002 • 6 = 0, 012 количество Платифилина меньше 0, 05 поэтому используем тритурацию 1: 10 Количество тритурации 0, 012 • 10 = 0, 12 Количество Папаверина 0, 03 • 6 = 0, 18 Количество Сахара 0, 2 • 6 = 1, 2 Количество сахара с учетом тритурации 1, 2 – 0, 12 = 1, 08 mобщ = 1, 08 + 0, 12 + 0, 18 = 1, 38
Теоретическое обоснование Готовят по массе в ступке, в первую очередь в ступку помещают и растирают сахар, т. к. это кристаллическое в-во общего списка и выписано в большем количестве. Количество сахара рассчитывается с учетом тритурации Во вторую очередь добавляют тритурацию Платифилина, т. к его меньшее количество Соотношение 1: 20 не превышено. В последнюю очередь добавляется Папаверин. Оформляют обратную сторону рецепта. После проверки на однородность массу развешивают на 6 вощеных капсул. Этикетки: «Внутреннее», «Обращаться с осторожностью» Больному выдают сигнатуру ППК к рецепту № 13. 06. 2012 А Saccari 1, 08 Triturationis Platyphyllini hydrotartratis 1: 10 0, 12 Papaverini hydrochloridi 0, 18 mобщ = 1, 38 m1 = 0, 23
Приготовил: Проверил: Отпустил: |
Качественный химический контроль папаверина гидрохлорида Все реакции подлинности папаверина основаны на легкой окисляемости за счет 4-х метоксигрупп 1) На основание папаверина а)С концентрированной серной кислотой к 0, 02г порошка + HNO3(к) 1-2кап = жёлт. окр – при нагревании на вод. бане – оранж. окр б) С концентрированной H2SO4 к 0, 02г порошка + 1-2кап Н2SO4(к) нагревают = сине-фиолет. окр в) С реактивом Марки к 0, 02г порошка + реактив Марки 2-3кап и слабо нагревают на вод. бане = фиолет. окр 2) На НСl а) на HCl – к 1 мл р-ра + 1-2кап HNO3 + AgNO3 = бел. твор. осадок нерастворимый в азотной к-те Cl- + AgNO3 → AgCl↓ + NO3-
Формула папаверина гидрохлорида
| ||
|
БИЛЕТ № 20. Rp: Sol. Acidi ascorbinici5% - 50ml Steril! D. S. Для в/в введения Сложная жидкая лекарственная форма для инъекций, с легкоокисляющимся веществом, истинный раствор
Стабилизаторы на 5% аскорбиновую к-ту Натрия тиосульфит 2мл - 1000 мл р-ра Х = 2 • 50 = 0, 1 мл Х мл – 50 мл р-ра 1000 Натрия гидрокарбонат 23, 85 – 1000 мл р-ра Х = 23, 85 • 50 = 1, 19 Х - 50 мл р-ра 1000 Теоретическое обоснование Готовят массо-объемным способом в асептических условиях, в мерной колбе, методом доведения до объема, т. к. раствор для инъекций. В качестве растворителя используют воду для инъекций т. к. аскорбиновая кислота легкоокисляющееся в-во то для стабилизации раствора используют антиоксидант-восстановитель – натрия сульфит безводный. Для уменьшения болезненности инъекций добавляется натрий гидрокарбонат. Раствор фильтруют через вату и складчатый фильтр, проверяют на чистоту, маркируют и закрывают под обкатку. Стерилизуют паровым методом при t = 120ОС 8 минут, т. к. объем р-ра 50 мл. После стерилизации раствор повторно проверяют на чистоту и к отпуску. Этикетки «Для инъекций», «Стерильно», «Хранить в прохладном защищенном от света месте». ППК к рецепту № 13. 06. 2012
Вз: Aq. proinjectionibusq. s. Acidiascorbinici 2, 5 Natriihydrocarbonatis 1, 19 Natrii sulfitis 0, 1 Aq. proinjectionibusad 50ml Vo= 50ml Приготовил: Проверил: № анализа 2/3 Подпись провизора-аналитика: Дата:
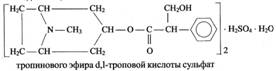
| ВАК р-ра аскорбиновой кислоты 5% - 50 мл П: работа с требованием – проверка правильности выпис-я доз в соотв-ии с возрастом б-ного(дозы не превышены), наличие указаний о способе применения. ППК – дата, № треб-я, хир. отд. б-цы №3 пригот., провер., № ан 2/3, подп. пров-анал, расфасовал Режим стерилизации 120ОС – 8мин; запись в «Журн. рег. рез. к-ля отд. стадий изгот. р-ров для инъекций и инфузий» О: б/цв, прозр. жид-ть б/видим. мех. вкл(отсут-ие мех вкл. опред-ся до и после стер-ции) КПО: флаконы закрыты под обкатку; осн. этик: «Для инъекций». Предупр: «Стерильно. Хр. в пр. з. от св. м. Беречь от детей» На этикетке: состав ЛС на лат. яз, способ прим-я – Sol. Acidiascorbinici 5% - 50ml. Внутивенно. Наимен-е и адрес аптеки, № б-цы, отделение, № ан-за 2/3, годность – 30дн, ФИО приготовившего, проверившего, отпустившего ЛС, дата. О, Ф: ОБЯЗАТЕЛЕН!!! ДО СТЕРИЛИЗАЦИИ!!! Vo=50ml доп. откл ±4% [48 ÷ 52мл] проверка кач-ва укупорки ПХК ОБЯЗАТЕЛЕН!!! ДО И ПОСЛЕ СТЕР-ЦИИ. До стер-ции – рН, ПХК аскорбиновой к-ты и стабилизаторов. После – рН и ПХК аскорбиновой к-ты. Хим. к-ль: ПХК подлежит каждая серия ОБЯЗАТЕЛЬНО Кач: Р-ции подлинности на аскорбиновую к-ту основаны на ее сильно выраженных восстановительных св-вах. При этом енольная форма окисляется и переходит в кетонную
1. Р-ция с р-ром серебра кр-ру прибавляют 2 кап. р-ра AgNO3образуется черный осадок
2. Р-ция с реактивом Фелинга р-р нагревают с реактивом Фелинга. Выделяется кирпично-красный осадок │ │ С-ОН 2С=О ║ + 2Cu(OH)2 → │ + Cu2O↓ + 3H2O С-ОН 3С=О кирпично │ │ красный осадок 3. Р-ция с хлоридом окисного железа и ферроцианидом калия к р-ру + 1-2 кап р-ра FeCl3. Происходит восстановление железа(III) до (II) │ │ С-ОН 2С=О ║ + 2FeCl3 → │ + FeCl2 + 3HCl С-ОН 3С=О обесцвечивание │ │ раствора После прибавления к р-ру 1 кап. феррицианида калия появляется синее окрашивание 3FeCl2 + 2K3[Fe(CN)6] → 6KCl + Fe3[Fe(CN)6]2↓ синее окрашивание Количественное определение аскорбиновой к-ты 1. М-д йодометрии(прямое титрование ) – 1мл р-ра титруют 0, 1 моль/л йода = жёлт окр (окрашивание придает неоттитрованный йод)
│ │ М аск. к-ты = 176, 13 f = ½ С-ОН 2С=О Т = 0, 1 • ½ • 176, 13 = 0, 0088 Vор = 0, 05 = 5, 68 мл ║ + J2 → │ + 2HJ 1000 0, 0088 С-ОН 3С=О V = 2, 8мл │ │ m = V • K • T • 50 = 2, 8 • 1 • 0, 0088 • 50 = 2, 552 1 1 Доп. откл ± 4% [2, 4 ÷ 2, 6] 2)М-д нейтрализации – к 1 мл р-ра +3-4 кап фенолфталеина титруют р-ром NaOHдо розового окрашивания │ │ С-ОН С-ОH ║ + NaOH → ║ + H2O С-ОН С-ОNa │ │ М аск. к = 176, 13 f = 1 Т = 176, 13 • 1 • 0, 1 = 0, 01761 mаск. к = V • K • T • 50 1000 1 V1 = 2, 75 мл mаск. к = 2, 75 • 1• 0, 01761 • 50 = 2, 42 г Доп откл ± 4% [2, 4 ÷ 2, 6] 1 | ||
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|
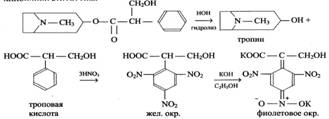
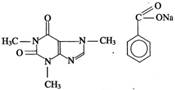
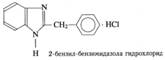
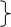 ¾ C¾ N¾
¾ C¾ N¾ 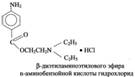
 Проверка доз : Р — 0, 01 Prodosi 0, 002
Проверка доз : Р — 0, 01 Prodosi 0, 002 Платифилин ВProdie 0, 004
Платифилин ВProdie 0, 004 Папаверин Р — 0, 2
Папаверин Р — 0, 2 ВProdosi 0, 03
ВProdosi 0, 03