
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
№ 9 Зертханалық сабақ
№ 9 Зертханалық сабақ
Электролиз.
Жұ мыстың мақ саты: Электролиз процесінің жү руін кө ру жә не оның ә р тү рлі жағ дайының схемасын қ ұ ру. Электрохимиялық коррозия жылдамдығ ына ә р тү рлі факторлар ә серін кө ру.
№1 Тә жрибе. Тұ рақ ты тоқ кө зінің теріс полюсін анық тау. Зертханада электролизер ретінде U тә різдес шыны ыдыстан тұ рақ ты екі электрод салынғ ан прибор қ олданылады.
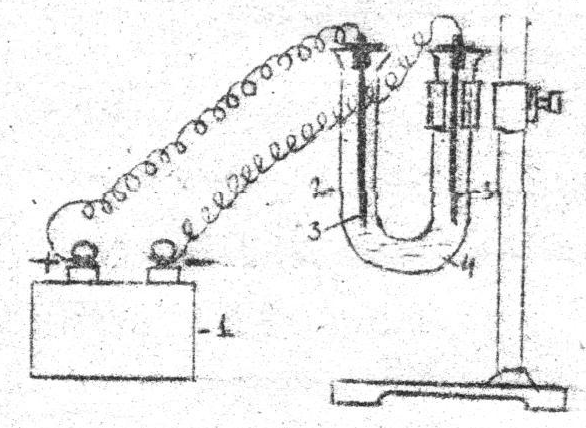 1-тұ рақ ты тоқ кө зі; 2- U тә різдес шыны ыдыс; 3- электродтар; 4- электролит ерітіндісі.
1-тұ рақ ты тоқ кө зі; 2- U тә різдес шыны ыдыс; 3- электродтар; 4- электролит ерітіндісі.
U- тә різдес шыны ыдысқ а натрий сульфатының ерітіндісін қ ұ йып, 1-2 тамшы фенолфталеин тамызың дар. Мыс электродтары тоқ кө зімен қ осың дар. 30-40 секундтан кейін теріс полюс қ осылғ анэлектродтың жанында ерітінді қ ызыл тү ске боялады. Электрлиз схемасын жазың дар.
№ 6 сурет. Электролизер.
№2 Тә жрибе. Калий иодиді ерітіндісінің электролизі.
Электролизерге калий иодиді ерітіндісін қ ұ йың дар, графит электродтарын батырың дар да оларды тұ рақ ты тоқ кө зіне қ осың дар. 3 минуттай электролиз жү ргізің дер, катодта газ тә різдес сутегі бө лінеді, ал анодта бос иод бө лінеді. Электролиз схемасын жазың дар. Тә жірбие біткен соң электродтар мен электролизерді жақ сылап кранның астына жуың ыздар.
№3 Тә жрибе. Мыс (ІІ) сульфатының ерітіндісінің электролизі.
Электролизерге мыс сульфаты ерітіндісін қ ұ йың дар, оғ ан графит электродтарын батырың дар, тұ рақ ты тоқ кө зімен қ осың дар. 3-5 минут электролиз жү ргізің іздер. Анодта оттегінің бө лінгенін байқ аң дар. Тә жірибе біткен соң катодта мыс бө лінгенін байқ аң дар. Енді тоқ кө зінің полюсін ауыстырың дар. Нені байқ айсың дар? Электролиздің схемасын жазып, байқ ағ ан қ ұ былыстарың ды тү сіндірің дер.
№4 Тә жрибе. Хлор-ионының коррозияны жылдамдатуы.
Екі пробиркағ а 6 мл мыс сульфатын, 2 мл кү кірт қ ышқ ылын қ ұ йың дар. Бір пробиркағ а 5 мл натрий хлоридін қ ұ йың дар. Екі пробиркағ а да алюминий сымын батырың дар. Қ ай пробиркада газ интенсивті бө лінеді?
Анодтық, катодтық жә не жалпы процестердің тең деулерін жазың дар. Реакция жылдамдығ ына хлор-ионының ә серін тү сіндірің дер.
№5 Тә жрибе. Оттегінің концентарциясына байланысты коррозия.
Болат пластинканы наждак қ ағ азымен тазалаң дар. Кранның астына қ ойып жуың дар. Фильтр қ ағ азымен сү ртіп кептірің дер. Содан кейін таза пластинканың бетіне мынандай ерітінділер: натрий хлориді, калий гексацианоферрат (ІІІ) жә не фенолфталеин қ оспасынан тұ ратын ерітіндіні тамызың дар. 3-5 минут уақ ыттан соң тамшының ортасында кө к тү сті, ал шетінде қ ызыл тү сті ерітінділер пайда болады. Тамшының арасында гальваникалық элемент тү зіледі. Тамшының ортасында оттегі аз болғ андық тан анодтық, шетінде оттегі кө п болғ андық тан катодтық зона пайда болады. Тамшының ортасында темір екі валентті ионғ а тотығ ады, сондық тан турнбулевая синь (кө к тү сті) пайда болады.
Тамшының шетінде судың ә серімен оттегі тотық сызданып, гидроксид-ион тү зеді, сондық тан фенолфталеин қ ызылғ а боялады.
Катодтық жә не анодтық процесстердің тең деуін жазың дар: Ғ е2+ жә не ОН- иондарын анық тау реакцияларының жә не темірдің тат басу (ржавчина) реакциясының тең деуін жазың дар.
№6 Тә жрибе. Металдарды коррозиядан протектор ә дісімен қ орғ ау.
Пробиркағ а сү йытылғ ан сірке қ ышқ ылын қ ұ йың дар. Оғ ан бірнеше тамшы калий иодиді ерітіндісін тамызың дар, бір-бірімен контактқ а келтіріп мырыш жә не қ орғ асын пластинкаларын батырың дар.
І- ионы Pb2+ ионына индикатор болып саналады. PbІ2 сары тү сті тұ нба. Салыстыру ү шін басқ а пробиркағ а осы ерітінділерді қ ұ йып, тек қ орғ асынды салың дар. Қ ай пробиркада қ орғ асын иодиді тез тү зіледі? Pb – Zn гальваникалық элементтің схемасын жазың дар. Қ ай металл протектор болып саналады?
№7 Тә жрибе. Коррозия жылдамдығ ына ингибитор ә сері.
Екі пробиркағ а 5-6 мл кү кірт қ ышқ ылын қ ұ йың дар. Ә р пробиркағ а жұ қ а темір пластинкасын салың дар. Бір пробиркағ а уротропин не басқ а ингибитор қ осың дар. Ингибитордың коррозия жылдамдығ ына ә серін қ орытындылаң дар.
Ө зін ө зі бақ ылауғ а жә не зертханалық жұ мысты қ орғ ауғ а арналғ ан сұ рақ тар:
- Электролиз деген не?
- Анод жә не катодта жү ретін процестерді тү сіндірің дер.
- Металды рафинадтау деген не? Ол қ алай жү реді?
- Электролиз заң дары?
- Металдар коррозиясы деген не?
- Коррозияның қ андай тү рлерін білесің дер?
- Электрохимиялық коррозияның химиялық коррозиядан айырмашылығ ы неде?
- Коррозиялық микрогальвани элементтері неге пайда болады?
- Қ андай факторлар коррозия жылдамдығ ына ә сер етеді?
- Металдарды коррозиядан қ орғ ау ә дістері. Қ ысқ аша ә р ә дісті сипатта.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|