
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
№ 1 Определение движений в суставах конечностей. Значение этого исследования для диагностики повреждений и заболеваний опорно-двигательной системы. 8 страница
| № 84 Клиническая и рентгенологическая диагностика остеоартроза крупных суставов. Клинико-рентгенологически выделяют 3 стадии остеоартрозов: I стадияхарактеризуется быстрой утомляемостью конечности, «скованностью» мышц. Только некоторые больные отмечают умеренное ограничение движений в суставе из-за скованности. Боли в суставе, как правило, отсутствуют. Только при некоторых артрозо-артритах, которые начинаются с патологического процесса в синовиальной оболочке, заболевание может начинаться с болевого и воспалительного синдрома. Рентгенологически в этой стадии развития болезни выявляется сужение суставной щели за счет хондролиза и возможен легкий, не всегда выявляющийся, субхондральный склероз. Нередко клиническая симптоматика этой стадии заболевания настолько незначительна, что больные даже не обращают на них особого внимания. Поэтому в некоторых литературных источниках можно встретить утверждение, что начало артроза чаще всего бессимптомное. Выше изложенное в основном характерно для диспластических артрозов. Посттравматические артрозы нередко начинаются со II стадии, так как при невправленных внутрисуставных переломах имеется первичное нарушение целости суставного гиалинового хряща. При наличии смещения внутрисуставных отломков с диастазом между ними более 2мм., регенерация гиалинового хряща невозможна. Имеющийся посттравматический дефект замещается костной мозолью, покрытой рубцовой соединительной тканью, а это уже и есть морфологические элементы II стадии развития артроза, который проявляет себя болевым синдромом, особенно при нагрузке на поврежденную конечность. II стадия характеризуется нарастанием ограничения движений, которые могут сопровождаться крепитацией. Обычно боли возникают в начале ходьбы – «стартовые боли». Они появляются из-за того, что во время первого шага основная нагрузка приходится на самый патологически измененный участок нагружаемой части суставной поверхности. Затем нагрузка при движениях более или менее распределяется равномерно на всю суставную поверхность, и боли могут полностью исчезнуть или заметно уменьшится до такой степени, что не мешают больному преодолевать даже значительные расстояния. Однако, с течением времени, особенно после продолжительной нагрузки, к концу рабочего дня боли усиливаются, но после отдыха могут вовсе исчезнуть. Появляется деформация сустава, гипотрофия мышц, контрактура, хромота. Рентгенологически выявляется значительное сужение суставной щели в 2-3 раза в сравнении с нормой, выражен субхондральный склероз, выявляются остеофиты в местах наименьшей нагрузки. К конечному этапу этой стадии развития болезни болевой синдром может иметь волнообразное проявление: периоды усиления болевого синдрома сменяются различными по продолжительности периодами значительного снижения интенсивности болей или полным их исчезновением. Как правило, такое проявление боли связано с вовлечением в процесс синовиальной оболочки, т. е. с развитием хронического рецидивирующего синовита, который является неотъемлемой частью клинических проявлений III стадии развития болезни. III стадия характеризуется почти полной потерей подвижности в суставе, сохраняются только пассивные качательные движения, выражена сгибательная контрактура. Боли сохраняются в покое, не проходят после отдыха. Возможна нестабильность сустава. При локализации процесса в суставах нижних конечностей к этому времени больные самостоятельно ходить не могут и прибегают к помощи трости или костылей. Рентгенологически – суставная щель почти полностью отсутствует. Суставная поверхность деформирована, выражены краевые разрастания. Основным рентгенологическим признаком этой стадии развития болезни и предыдущей является появление множественных кист в субхондральных зонах суставных поверхностей. | № 85 Консервативное лечение остеоартрозов крупных суставов. Больным с деформирующим артрозом необходимо соблюдать определенный двигательный режим, направленный на разгрузку больного сустава. Им следует избегать продолжительной ходьбы, длительного стояния на ногах или пребывания в одной позе, не следует носить тяжести. При выраженном болевом синдроме во время ходьбы необходимо пользоваться тростью или ходить с помощью костылей. Для разгрузки больного сустава, даже в домашних условиях, следует применять манжетное вытяжение с грузом по оси ноги 2-3кг. При резких болях, не проходящих от вышеперечисленных мероприятий, можно применять фиксацию сустава гипсовой повязкой на 2-4 недели, но при этом еще больше ограничиваются движения, а контрактуры усугубляются. Цель консервативного лечения артрозов – восстановление кровообращения в тканях больного сустава. Терапия должна быть комплексной и включать не только медикаментозное лечение, но и физиотерапевтическое, санаторно-курортное. Ниже описанное консервативное лечение должно быть комплексным и соответствовать стадии развития болезни. Средства микроциркулярного воздействия применяются для восстановления системы микроциркуляции. С этой целью применяют различные средства, фармакогенез которых неодинаков: ангиотрофин, андекалин, депокалликреин, дильминал, инкрепан. Они назначаются в первой стадии заболевания у больных без явлений синовитиа в течении 3-х недель. При развитии воспаления в тканях сустава лучше использовать средства, инактивирующие кининовую систему - контрикал, залол, трасилол и др. К средствам микроциркуляторного воздействия относятся АТФ, никотиновая кислота, никошпан, троксевазин, продектин, трентал, доксиум, фосфоден, эсфлазин. Для улучшения усвоения кислорода тканями сустава применяют витамины группы В. Нормализует метаболические процессы в тканях солкосерил, особенно при тяжелых поражениях. Косвенно улучшают микроциркуляцию гепарин и антикоагулянты непрямого действия. Обезболивающая и противовоспалительная терапия. Наиболее распространенным препаратом этой группы является аспирин. Он обладает противовоспалительным, обезболивающим эффектом, улучшает микроциркуляцию. С этой же целью применяют анальгин, бутадион. Фепразон является наиболее перспективным препаратом этой группы, т. к. почти не оказывает воздействия на желудочно-кишечный тракт и может назначаться даже при язвенной болезни желудка. В ряду с ним стоит кетанов. Весьма эффективны нестероидные противовоспалительные препараты: индометацин, напроксен, вольтарен, диклофенак. Базизные антиартрозные препараты способны улучшать обмен дистрофически измененных суставных хрящей. К ним относят: румалон, мукартрин, артепарон, хлорохин и др. Последний способен усиливать регенерацию хрящевой ткани после травм и дистрофических процессов. Главное влияние базисных препаратов заключается в том, что они связывают ферменты, ответственные за повреждение хряща при артрозе. Десенсибилизирующие препараты назначаются во всех стадиях артроза. Внутрисоставное введение лекарственных препаратов получило широкое распространение. Чаще всего вводят гармональные препараты (гидрокортизон, дексаметазон, дипроспан и др. ), которые уменьшают выход лизосомальных ферментов и альтерацию тканей, оказывая противовоспалительное, десенсибилизирующее действие, но могут усугублять дегенерацию хряща. Поэтому их предпочитают вводить при тяжелых формах развития болезни. Воздействие на симпатическую нервную систему достигается блокадами нервных стволов, узлов и сплетений, которые направлены на устранение болей и снятие мышечного спазма с последующим увеличением амплитуды движений в суставах. Физиотерапевтические методы лечения направлены на стимулирование обменных и трофичесих процессов, восстановление микроциркуляции, активизации процессов восстановления и уменьшение дистрофических процессов. При назначении ФТЛ учитывается стадия заболевания. В начальных стадиях артроза без явлений синовита назначают для стимуляции обменных процессов индуктотермию, ДМВ, СМВ, СМТ, ультразвуковую терапию, радоновые, хлоридно-натриевые, скипидарные ванны, грязелечение. При этом следует учитывать, что у больных с обострением синовита тепловые процедуры могут усиливать болевой синдром. В этих случаях назначают фонофорез или электрофорез анальгина, апифора, гидрокортизона, салицилата натрия, папаверина. Для стимуляции обменных процессов в хряще назначают электрофорез цинка, лития, серы. Аналгезирующим эффектом обладают УФ-облучение, синусоидальные, диадинамические токи, ультразвук. Местно применяют компрессы с медицинской желчью, камфорным спиртом, повязки с вазелином, троксевазином. ЛФК и массаж стимулируют кровообращение, тканевой обмен и способствуют улучшению функции сустава. При обострении синовита ЛФК и массаж не показаны. Санаторно-курортное лечение начинают проводить у больных I-II ст. без синовита в период ремиссии. Используют грязевые курорты, с хлоридно-натриевыми, радоновыми водами (Бобруйск, Летцы, Светлогорск, Берестье, Радон и др. ) | № 86 Показания и варианты оперативного лечения при остеоартрозах крупных суставов. Оперативное лечение рекомендуется при III ст. заболевания. Основная цель оперативного лечения - ликвидация болевого синдрома и восстановление опороспособности конечности. Очень желательно восстановление или сохранение движений в суставе. При вторичных артрозах оперативное лечение нередко является первым мероприятием уже в начальной стадии процесса с целью ликвидации биомеханических причин заболевания (инконгруентность, децентрация, нестабильность) и прерывания его в начальных стадиях. Характер оперативных вмешательств зависит от этиологии артроза, его стадии и локализации. При первичных деформирующих артрозах III стадии тазобедренного сустава применяются: артродез (ликвидирует боли ценой формирования костного анкилоза), различные виды артропластических оперативных вмешательств, краевую моделирующую резекцию головки бедра и впадины, эндопротезирование суставов. При коксартрозе, протекающем без нарушения конгруэнтности суставных поверхностей, предпочтение отдают внесуставным операциям, в частности, различным видам остеотомии проксимального отдела бедренной кости, которые изменяют топографию нагрузок в тазобедренном суставе. Применяют также декомпрессионную миотомию (операция Брандеса — Фосса) у лиц пожилого возраста при удовлетворительной амплитуде движений в тазобедренном суставе. При этом отсекают большой и малый вертелы с прикрепляющимися мышцами, рассекают широкую фасцию бедра, приводящие мышцы. В течение 2 нед осуществляют вытяжение конечности с постепенной разработкой тазобедренного сустава, Затем — ходьба на костылях, ЛФК, массаж, физиотерапевтические процедуры. Наиболее эффективные результаты восстановления утраченной опороспо-собности и подвижности в патологически измененном суставе обеспечиваются тотальным эндопротезированием, особенно при двустороннем поражении. В настоящее время за рубежом и в нашей стране разработаны разнообразные типы эндопротезов тазобедренного сустава. Абсолютными показаниями к имплантации тотального эндопротеза тазобедренного сустава являются двусторонний коксартроз III стадии, асептический некроз головки бедренной кости, односторонний анкилоз тазобедренного и коленного суставов, сочетание тяжелых дегенеративно-дистрофических процессов в тазобедренном суставе и пояснично-крестцовом отделе позвоночника, двусторонний анкилоз при болезни Бехтерева, а также последствия повреждений головки, шейки, межвертельной области и новообразования проксимального конца бедренной кости. Относительным показанием к тотальному эндопротезированию является одностороннее поражение тазобедренного сустава. Абсолютными противопоказаниями к полной замене тазобедренного сустава являются сопутствующие тяжелые хронические заболевания сердечно-сосудистой системы, легких, почек; воспалительный процесс в области тазобедренного сустава; очаги хронической инфекции (тонзиллит, отит, кариес зубов и т. д. ); искривленный и очень узкий костномозговой канал бедренной кости, тонкие тазовые кости. Относительным противопоказанием к этой операции является молодой и очень преклонный возраст больного. В случаях дисплазии уже на ранних стадиях артроза рекомендуются кроме остеотомий бедра – остеотомии таза, т. е. проводят внесуставные операции, улучшающие взаимоотношение суставных поверхностей, и увеличивающие площадь покрытия головки бедра крышей вертлужной впадины, распределяя равномерно нагрузку на суставные поверхности. При деформирующих артрозах коленных суставов прибегают чаще к корригирующим остеотомиям с целью создания правильной нагрузки на суставные поверхности. В крайних случаях проводят артродез. Эндопротезирование сустава в нашей стране пока еще не получило должного распространения. В некоторых случаях, когда больной не соглашается на операцию по каким-то причинам, проводят консервативное лечение, которое при вторичных артрозах не приводит к выздоровлению, а только облегчает течение патологического процесса. |
| № 87 Эндопротезирование тазобедренного сустава при его заболеваниях и повреждениях. Показания, типы эндопротезов. Эндопротезирование тазобедренного сустава является эффективным и часто единственным способом восстановления утраченной функции конечности. Тотальное, т. е. замена всех компонентов сустава, эндопротезирование является методом выбора при лечении следующих болезней: · болезнь Бехтерева (с преимущественным поражением тазобедренных суставов); · дегенеративно-дистрофические заболевания (артрозы-артриты); · ревматоидный полиартрит; · асептический некроз головки бедра; · ложные суставы шейки бедра и несросшиеся переломы шейки бедра. Эндопротез имитирует естественный тазобедренный сустав с головкой и вертлужной впадиной. Наиболее часто встречается комбинация керамической головки с полиэтиленовой вертлужной впадиной. Перед операцией определяются индивидуальные размеры вертлужной впадины. В зависимости от возраста, индивидуальных анатомических особенностей и веса определяется тип эндопротеза тазобедренного сустава. Все части протеза выполненны из высокопрочных материалов. Существуют разные виды компонентов эндопротезов тазобедренного сустава. Нецементированный эндопротез. Вертлужная впадина и стержень эндопротеза имеют специальное покрытие для врастания в костную ткань. Оба компонента закрепляются специальной пресс-фит техникой (без цемента). Нецементированные эндопротез тазобедренного сустава применяют преимущественно для молодых активных пациентов. Цементированный эндопротез. Вертлужная впадина и стержень эндопротеза закрепляются специальным цементом-" палякост". Этот тип эндопротезов тазобедренного сустава рекомендуется для пожилых пациентов. Нагрузка возможна сразу после эндопротезирования. Гибридно-полный эндопротез. При данном виде эндопротезирования закрепление вертлужной впадины осуществляется без цемента-путём вкручивания, стержень эндопротеза цементируется в бедренной кости. Компоненты тазобедренного сустава (головка и вертлужная впадина) могут состоять из различных материалов - полиэтиленового материала, керамики или металла и отличаться степенью износа эндопротеза. Абсолютными показаниями к имплантации тотального эндопротеза тазобедренного сустава являются двусторонний коксартроз III стадии, асептический некроз головки бедренной кости, односторонний анкилоз тазобедренного и коленного суставов, сочетание тяжелых дегенеративно-дистрофических процессов в тазобедренном суставе и пояснично-крестцовом отделе позвоночника, двусторонний анкилоз при болезни Бехтерева, а также последствия повреждений головки, шейки, межвертельной области и новообразования проксимального конца бедренной кости. Относительным показанием к тотальному эндопротезированию является одностороннее поражение тазобедренного сустава. |
№ 88 Доброкачественные опухоли костей. Классификация, принципы лечения. 1. Первичные опухоли остеогенного происхождения: А. Доброкачественные (остеома, остеоид-остеома, остеобластокластома, хондрома, хондробластома, фиброма, доброкачественная хордома и др. ) Б. Злокачественные (остеогенная саркома, хондросаркома, злокачественная остеобластокластома, злокачественная хордома). 2. Первичные опухоли неостеогенного происхождения: А. Доброкачественные (гемангиома, лимфангиома, липома, фиброма, нейрома). Б. Злокачественные (опухоль Юинга, ретикулосаркома, липосаркома, фибросаркома). 3. Вторичные опухоли, параоссальные и метастатические. Остеома — довольно частый вид опухоли. По происхождению различают компактные, губчатые (спонгиозные) и смешанные (медуллярные) остеомы. Остеомы поражают, как правило, одну кость с единичным очагом, но нередко можно встретить и множественные остеомы, располагающиеся в симметричных участках одноименных костей конечностей. Лечение больных с остеомой только оперативное. Необходимо помнить, что остеомы легко рецидивируют, поэтому удалять ее следует всегда только радикально с надкостницей. Остеоидная остеома — небольшая по размерам опухоль (1—2 см), локализуется преимущественно в диафизарных отделах длинных трубчатых костей. Лечение — хирургическое. Удаляют опухоль двояким методом — частичной резекцией кости или сегментарной резекцией с последующим замещением дефекта ауто- или аллотрансплантатом. Остеобластокластома (гигантокле-точная опухоль) относится к группеновообразований, состоящих из собственно костной ткани. Лечение больных с остеобластокластомой оперативное. При поражении одной стенки кости производят краевую резекцию; при полном разрушении кости на весь поперечник — резекцию пораженного участка с замещением дефекта аллотрансплантатом, консервированным замораживанием. Хондрома наблюдается в основном в возрасте до 20 лет. Локализуется опухоль в виде солитарного узелка, преимущественно в диафизарных отделах коротких трубчатых костей кисти и стопы, а также в ребрах, позвонках и костях таза, т. е. в костях, имеющих наибольшее количество хряща. Лечение. Различные оперативные вмешательства в зависимости от локализации и характера опухоли—краеваярезекция или резекция на протяжении с заполнением дефекта ауто- или аллотрансплантатом. Остеохондрома — хрящевая опухоль (хондрома), в которой развиваются остеоидная ткань и костные структуры. Лечение. Резекция пораженной части кости с последующим замещением дефекта ауто- или аллотрансплантатом. Хондробластома относится к довольно редко встречающимся новообразованиям и наблюдается у детей и лиц молодого возраста, преимущественно мужского пола. Лечение. Радикальная резекция с замещением дефекта ауто- или аллотрансплантатами. Прогноз после оперативного лечения благоприятный. Экхондрома — опухоль, исходящая из кости и растущая в сторону мягких тканей. Лечение хондром только хирургическое — экскохлеация опухоли, резекция кости с костной пластикой. При подозрении на малигнизацию — сегментарная резекция поражённой кости. Хондромиксоидная фиброма — безболезненная доброкачественная опухоль. Лечение — оперативное (экскохлеация опухоли с последующим замещением дефекта кости трансплантатом). Остеобластокластома (гигантоклеточная опухоль) возникает в молодом возрасте (у лиц моложе 30 лет), поражает как эпифиз, так и метафиз длинных трубчатых костей. Лечение остеобластокластом хирургическое. Щадящая резекция кости с удалением опухоли и одномоментной костной пластикой (ауто-, гомотрансплантаты либо замещение метилметакрилом) — метод выбора. При поражении опухолью позвоночника применяют лучевую терапию. Гемангиома — врождённая аномалия, при которой пролиферация клеток эндотелия приводит к образованию скоплений, напоминающих опухоль. Лечение — разгрузка позвоночника: ношение жёсткого корсета, лучевая терапия, при компрессии спинного мозга — ламинэктомия. |
|
|
№ 101 Определение величины кровопотери по клиническим признакам. Методы восполнения кровопотери. Возможности компенсации острой кровопотери на этапах медицинской эвакуации. Объем циркулирующей крови (ОЦК) составляет 6, 5% от массы тела у женщин и 7, 5% от массы тела у мужчин. Потеря до 5—10% ОЦК (около 500 мл) у здорового человека может быть компенсирована за счет веномоторного эффекта, приводящего в соответствие сниженный ОЦК и емкость сосудистого русла. Такая кровопотеря непосредственно не угрожает жизни, не сопровождается выраженными отклонениями от нормы клинических и лабораторных показателей и соответствует доклинической степени тяжести. Объем циркулирующей крови при этом восстанавливается за счет транскапиллярного перемещения внеклеточной жидкости в сосудистое русло (феномен гемодилюции). При массивной кровопотере объем такого перемещения может быть весьма значительным и составить 4—7 л. Дефицит белков плазмы восполняется за счет мобилизации лимфы из лимфатических сосудов в венозные коллекторы. Восполнение же дефицита форменных элементов крови, особенно эритроцитов, даже при относительно небольшой (до 15% ОЦК) кровопотере занимает 2—3 нед, а при более значительном кровотечении растягивается до нескольких месяцев. Умеренная степень кровопотери (10—20% ОЦК) вызывает более значительную «централизацию» кровообращения и приводит к выраженному спазму прекапиллярных сфинктеров и посткапиллярных венул, вследствие чего из периферического кровотока выключается капиллярное русло. ОЦК снижается еще больше, перфузия тканей уменьшается. Дефицит кислорода в тканях создает предпосылки для постепенного перехода тканевого обмена на анаэробный метаболизм. Такой объем кровопотери, как правило, сопровождается развитием компенсированного обратимого шока. Кровопотеря средней степени тяжести (20—30% ОЦК) приводит к дальнейшему углублению гипоксии, нарастанию метаболического ацидоза и развитию развернутой клинической картины декомпенсированного обратимого геморрагического шока. Тяжелая степень кровопотери (свыше 30% ОЦК) является критической. При отсутствии своевременной и адекватной коррекции она может привести к развитию необратимого геморрагического шока и летальному исходу. Важное значение имеет не только объем, но и скорость кровопотери. При хроническом малоинтенсивном кровотечении, достигающем порой нескольких литров, состояние пациента может оставаться субкомпенсированным за счет того, что успевают включиться компенсаторные механизмы (мобилизация внеклеточной жидкости, крови из кровяных депо; активизация кроветворения). Одномоментная же потеря даже 500—700 мл крови (например, из поврежденного крупного сосуда) может привести к коллапсу и острой сердечно-сосудистой недостаточности. Доврачебная помощь: инфузионная терапия с целью восполнения ОЦК. Показанием к введению растворов в сосудистое русло служат такие признаки, как низкое артериальное давление, частый пульс, бледность кожных покровов, а также обильное пропитывание одежды или ранее наложенных повязок кровью, что также может говорить о продолжающемся или состоявшемся массивном кровотечении. Производят пункцию периферической вены с подключением одноразовой системы для переливания. Внутривенно струйно или быстро капельно вводят до 800—1200 мл кристаллоидных растворов. Врачебная помощь: Компенсация острой кровопотери пострадавшему проводится параллельно с другими лечебными манипуляциями, а также в процессе транспортировки. Задержка дальнейшей эвакуации с целью проведения инфузионно-трансфузионной терапии допустима только при наличии декомпенсированного шока, когда любая транспортировка абсолютно противопоказана. Вместе с тем, если кровотечение продолжается, самая активная инфузионно-трансфузионная терапия не может быть эффективной. Техника инфузионной терапии. Введение растворов при массивной острой кровопотере производится, как правило, в центральную вену (верхнюю или нижнюю полые вены). Наиболее часто для катетеризации верхней полой вены используют подход через подключичную вену. Внутрикостный метод введения растворов является по существу разновидностью внутривенного и применяется тогда, когда по каким-либо причинам вообще нельзя использовать вены для инфузий. Техника его состоит в том, что после анестезии раствором новокаина места вкола специальной широкопросветной («внутрикостной») иглой с мандреном прокалывают мягкие ткани в области гребня подвздошной, пяточной костей, бугристости большеберцовой кости и вращательным движением проникают через кортикальный слой в губчатое костное вещество. Содержание инфузионно-трансфузионной терапии. При оказании первой врачебной помощи нет возможности для определения лабораторных параметров крови (плотность, гемоглобин, гематокрит), характеризующих величину кровопотери. В этой ситуации ориентироваться в примерном объеме кровопотери можно по индексу Алговера (индекс 0, 7—0, 8 соответствует примерно утрате 10% ОЦК; индекс 0, 9—1, 2 — 20%, а индекс свыше 1, 2—30%). Кроме того, существуют ориентировочные цифры кровопотери при переломах костей голени (400—500 мл), бедра (500—1000 мл), таза (односторонние переломы — до 1500, двусторонние — до 3000 мл) и др. Начинают кровезамещение с введения кристаллоидных растворов (400—800 мл), обеспечивающих восстановление не только внутрисосудистого, но и интерстициального объема жидкости (при тяжелом геморрагическом шоке — параллельно струйно в две вены). Затем переходят на введение коллоидных сред с высоким волемическим коэффициентом (400—800 мл полиглюкина). При оказании первой врачебной помощи кровь переливается только в случаях массивной кровопотери при надежно остановленном наружном кровотечении. Квалифицированная помощь: Если ранее не был введен катетер в вену, катетеризация должна быть осуществлена. Для определения необходимого объема инфузий следует ориентироваться на величину кровопотери, рассчитываемую на основе таких показателей, как относительная плотность крови, гемоглобин, гематокрит. Важной задачей является восстановление кислородной емкости крови. Умеренная гемодилюция, развивающаяся при переливании кристаллоидных и коллоидных растворов, улучшая реологические свойства крови, существенно не влияет на ее кислородную емкость. Однако при показателях гематокрита ниже 25—30 % требуется переливание трансфузионных сред, способных увеличить кислородную емкость. Для этих целей используют кровь или эритроцитную массу, а также искусственные среды — переносчики кислорода, созданные на основе фторорганических соединений. |
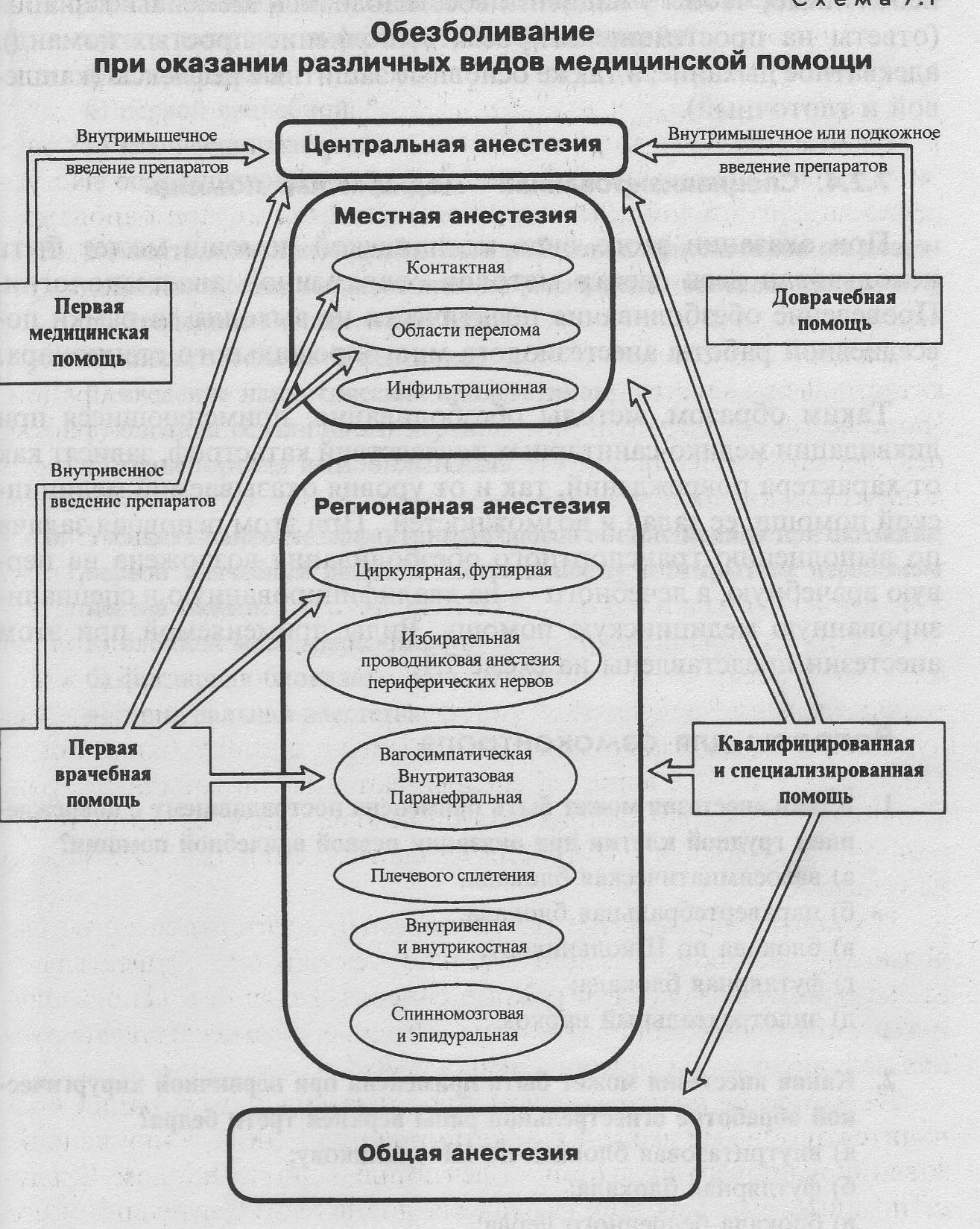
№ 102 Показания и техника проведения гемотрансфузии на этапах медицинской эвакуации, ее особенности. Показания к реинфузии крови. При кровопотере средней тяжести (до 20-30% ОЦК) и тяжелой (свыше 30%). При тяжелой кровопотере (свыше 30% ОЦК) общий объем вводимой жидкости должен на 300% превысить кровопотерю, причем гемотрансфузия приобретает уже первостепенное значение. Чаще всего при необходимости гемотрансфузий используют консервированную кровь (гематокрит около 40%). При подготовке к переливанию консервированной крови необходимо выполнить следующие действия. 1. Определить группу крови пациента. Групповая принадлежность крови человека определяется агглютиногенами А и В, содержащимися в эритроцитах, и агглютининами а и в, содержащимися в плазме. Для определения группы крови применяют двойной набор стандартных сывороток всех групп крови (I группа — желтого цвета, II — синего, III — красного, IV — бесцветная), содержащих только агглютинины. В последние годы используется упрощенный (но не менее надежный) способ определения группы крови при помощи стандартных сывороток ЦОЛИПК. Наносятся всего две капли специальных сывороток II и III групп. Результаты интерпретируются следующим образом: Кроме групповой принадлежности важное значение имеет резус-фактор — специфический антиген, содержащийся в эритроцитах у 85 % людей (резус-положительная кровь, или Rh+). 2. Подобрать кровь для переливания и проверить ее пригодность. На флаконе с кровью следует проверить наличие этикетки с указанием группы и резус-фактора и т. д. 3. Определить групповую совместимость. 4. Определить индивидуальную совместимость. 5. Провести биологическую пробу. Проводится троекратно. Внутривенно струйно вводится 25 мл крови из флакона, после чего делается перерыв на 10 мин. Необходимо именно быстрое введение, так как при медленном переливании симптомы несовместимости (затруднение дыхания, боли в пояснице, чувство беспокойства, озноб, учащение пульса и дыхания, снижение артериального давления) могут проявиться в стертой форме и не быть вовремя замеченными. Огромное значение для спасения жизни пострадавшего имеет реинфузия аутокрови , излившейся в серозные полости и собранной в процессе операции. Эта кровь не может оказаться несовместимой, в ней отсутствуют изменения, связанные с консервированием и хранением. Реинфузия позволяет вернуть пострадавшему почти всю потерянную кровь. Кроме того, экономится время, связанное с поисками и совмещением крови необходимой группы. Частичный гемолиз при этом неопасен, так как гемоглобин реинфузируемой аутокрови по структуре идентичен белкам организма и, появляясь в плазме в свободном состоянии, быстро выводится почками, не вызывая осложнений при наличии адекватного диуреза. Аутокровь благодаря своим бактерицидным свойствам длительное время остается стерильной, что позволяет использовать ее даже при проникающих ранениях. Реинфузию в любых случаях следует предпочесть переливанию консервированной крови, прямому переливанию, переливанию препаратов крови. Показаниями к реинфузии крови могут являться: — закрытые и проникающие ранения груди с повреждением сердца, легких и крупных сосудов; — закрытые и проникающие травмы живота с повреждением паренхиматозных органов и крупных сосудов; — разрывы матки и маточных труб; — острая массивная кровопотеря, возникшая в процессе операции (в том числе — и на сосудах конечностей). | № 103 Объем и характер анальгетической терапии при оказании различных видов медицинской помощи при катастрофах.
| |
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|