
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
3. Примеры
а) CO2. Центральный атом С, 2 партнёра по связи О. Свободных электронных пар у углерода нет:
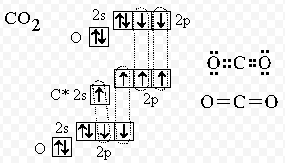
n=2, m=0, 2+0=2 → sp-гибридизация → расположение пар линейное.
Формула по Гиллеспи: АВ2Е0 → геометрия молекулы линейная; угол 180⁰:
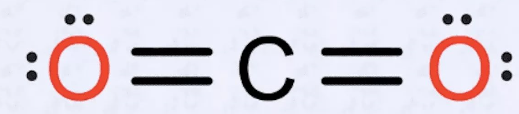
б) SO2 n=2, m=1, 2+1=3 → sp2-гибридизация → расположение пар тригональное.
Формула по Гиллеспи: АВ2Е1 → геометрия молекулы уголковая; угол чуть меньше 120⁰ из-за отталкивания одной неподелённой электронной пары:
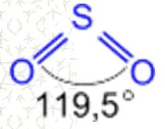
в) SO3
n=3 3+0=3 → sp2-гибридизация → расположение пар тригональное.
m=0
Формула по Гиллеспи АВ3Е0 → геометрия молекулы тригональная (плоский треугольник); угол составляет чётко 120⁰:
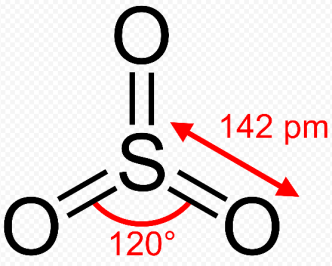
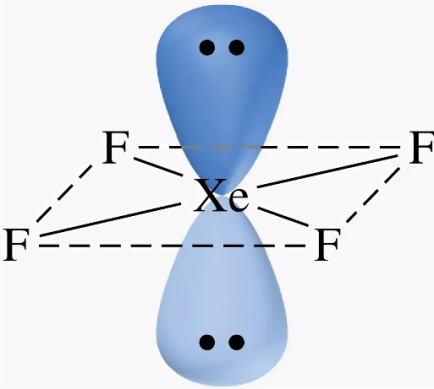
г) ХеF4 n=4, m=2, 4+2=6 → sp3d2-гибридизация → расположение пар октаэдрическое.
Формула по Гиллеспи: АВ4Е2 → геометрия молекулы квадратная; угол составляет 90⁰:
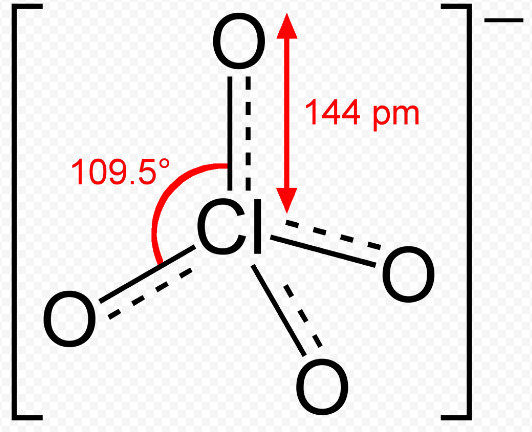
д) ClO4 - n=4 4+0=4→ sp3-гибридизация → расположение пар тетраэдрическое.
m=0
Формула по Гиллеспи: АВ4Е0 → геометрия молекулы тетраэрическая; угол составляет 109⁰ 28ʹ:
е) (ClF2)- n=2, m=3, 2+3=5 → sp3d-гибридизация → расположение пар тригонально- бипирамидальное.
Формула по Гиллеспи: АВ2Е3 → геометрия молекулы линейная (аналогично CO2); угол составляет 180⁰.
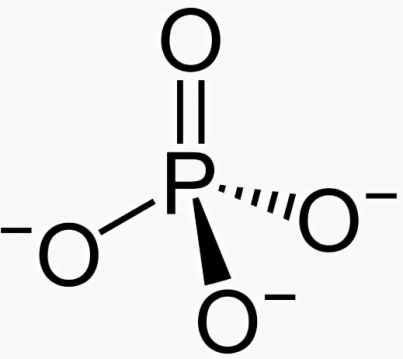
ж) РО43-
n=4, m=0, 4+0=4 → sp3-гибридизация → расположение пар тетраэдрическое.
Формула по Гиллеспи: АВ4Е0 → геометрия молекулы тетраэдрическая; угол составляет чуть меньше 109⁰ 28ʹ из-за отталкивания пи-электронов:
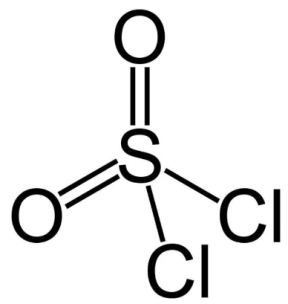
з) SO2Cl2
n=4, m=0, 4+0=4 → sp3-гибридизация → расположение пар тетраэдрическое.
Формула по Гиллеспи: АВ4Е0 → геометрия молекулы тетраэдрическая; угол составляет чуть меньше 109⁰ 28ʹ из-за отталкивание пи-электронов:
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|