
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Практическая работа. Альдегиды. Карбоновые кислоты
Практическая работа
Альдегиды. Карбоновые кислоты
Знать: функциональные группы альдегидов, кетонов и карбоновых кислот; виды изомерии и номенклатуру альдегидов, кетонов и карбоновых кислот; классификацию карбоновых кислот; химические свойства альдегидов и кетонов; химические свойства предельных одноосновных и двухосновных карбоновых кислот, способы получения и применения альдегидов, кетонов и карбоновых кислот; состав и свойства производных карбоновых кислот; особые свойства отдельных представителей кислот; качественные реакции на альдегиды и кислоты
Уметь: составлять структурные формулы альдегидов, кетонов и карбоновых кислот по названию и называть предложенные вещества; составлять структурные формулы изомеров альдегидов, кетонов и карбоновых кислот; выявлять связь физических свойств и строения веществ; составлять уравнения реакций, характеризующих химические свойства и получение альдегидов, кетонов и карбоновых кислот; прогнозировать химические свойства веществ исходя из строения; составлять уравнения реакций, иллюстрирующих генетическую связь между классами соединений.
Основные понятия: карбонильная группа, карбоксильная группа, кетоны, енол, моно- и дикарбоновые кислоты, оксикислоты, хлорангидриды, амиды, мыла.
Алгоритм 7.1. Изомерия и номенклатура карбоновых кислот
Задание 1. Составить формулы изомеров состава C5H10O2. Назвать вещество.
Решение:
Молекулярная формула C5H10O2 подчиняется общей формуле CnH2nO2, это может быть предельная одноосновная кислота или сложный эфир.
1. Составить структурные формулы карбоновых кислот, отвечающих составу С5H10O2:
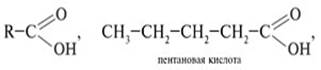
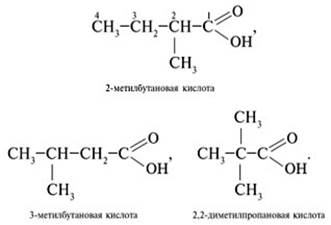
2. Составить формулы сложных эфиров, отвечающих составу C5H10O2:
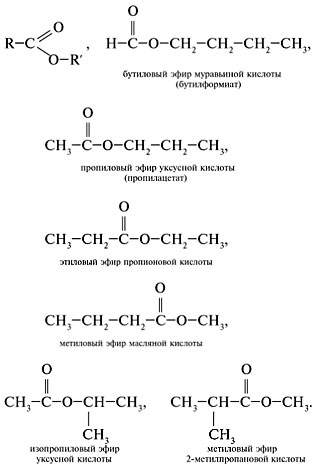
Задание 2. Составить формулу пентен-2-овой кислоты. Для этого вещества составить формулы изомеров и назвать их.
Решение:
1. Составить структурную формулу по названию: «пентен-2-овая».
а) «пентен» – 5 атомов углерода в цепочке:
С–С–С–С–С.
б) Слово «кислота» означает, что присутствует карбоксильная группа:
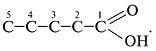
в) Запись «ен-2» сообщает о двойной связи между 2-м и 3-м атомами С:
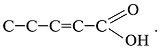
г) Расставить недостающие атомы водорода:
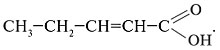
2. Составить формулы изомеров по положению двойной связи.
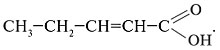
3. Составить формулы структурных изомеров:
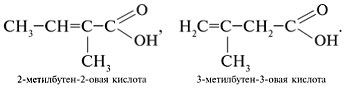
4. Составить формулы изомерных сложных эфиров:

Алгоритм 7.2. Решение расчетных задач по теме «Альдегиды. Карбоновые кислоты»
Задача 1. Какой объем уксусной эссенции плотностью 1,07 г/мл надо взять для приготовления столового уксуса объемом 200 мл и плотностью 1,007 г/мл? Массовая доля уксусной кислоты в уксусной эссенции равна 80%, а в уксусе – 6%.
Решение:
1. Записать условие задачи.
Дано:
р(укс. эссенции) = 1,07 г/мл,
р(уксуса) = 1,007 г/мл,
V(уксуса) = 200 мл,
w (СН3СООН) = 80% (в эссенции),
w (СН3СООН) = 6% (в уксусе).
Найти:
V(эссенции).
2. Определить массу раствора уксуса:
m = •V, m = 200•1,007 = 201,4 г.
3. Определить массу уксусной кислоты в уксусе:
m = 201,4•0,06 = 12,1 г.
4. Определить массу уксусной эссенции, которая содержит 12,1 г уксусной кислоты:
m = 12,1/0,8 = 15,1 г.
5. Определить объем уксусной эссенции:
V = 15,1/1,07 = 14,1 мл.
Ответ. V(уксусной эссенции) = 14,1 мл.
Задача 2. Уксусная кислота содержит примеси уксусного альдегида и этанола. Образец кислоты массой 20 г обработали избытком аммиачного раствора оксида серебра и получили 13,5 г осадка. На нейтрализацию такого же образца кислоты израсходовали 25,65 мл раствора с массовой долей гидроксида натрия 30% и плотностью 1,3 г/см3. Вычислить массовые доли примесей в кислоте.
Решение:
1. Записать условие задачи.
Дано:
m(кислоты) = 20 г,
m(Ag) = 13,5 г,
V(р-ра NaOH) = 25,65 мл,
w (NaOH) = 30%,
p(р-ра NaOH) = 1,3 г/см3.
Найти:
w (СН3С(О)Н),
w (С2Н5ОН).
2. Составить уравнения реакций:
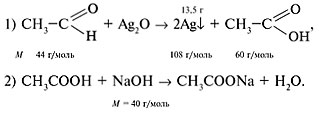
3. Найди массу альдегида по уравнению реакции (1):
m(СН3С(О)Н) = 44•13,5/216 = 2,75 г.
4. Вычислить массу NaOH, вступившего в реакцию:
m(NaOH) = 25,65•1,3•0,3 = 10 г.
5. Определить массу уксусной кислоты, расходуемой в реакции (2):
m(СН3СООН) = 10•60/40 = 15 г.
6. Найти массу этанола в исходной смеси:
m(С2Н5ОН) = 20 – 15 – 2,75 = 2,25 г.
7. Рассчитать массовые доли спирта и альдегида в кислоте:
w(С2Н5ОН) = 2,25/20 = 0,1125, или 11,25%;
w(СН3С(О)Н) = 2,75/20 = 0,1375, или 13,75%.
Ответ.w (С2Н5ОН) = 11,25%, w(СН3С(О)Н) = 13,75%.
Задания для самоконтроля:
1. Составить формулы веществ по их названиям:
а) 3-метилпентаналь;
б) 2-метилпентанон-3;
в) 5-метилгексен-3-овая кислота;
г) 2,3-диметилбутановая кислота;
2. Осуществить превращения:
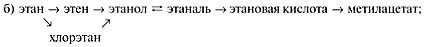
3. Плотность по водороду вещества, имеющего состав: углерод – 54,55%, водород – 9,09%, кислород – 36,36%, равна 22. Оно легко восстанавливает оксид серебра в аммиачном растворе, образуя кислоту. Определить структурную формулу этого вещества.
4. При взаимодействии 120 г уксусной кислоты с хлором получили 170 г. хлоруксускной кислоты. Найти выход продукта. Ответ. 89,95%.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|