
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Номенклатура. Классификация пептидов. Синтез пептидов
Номенклатура
Аминокислотный остаток пептида, который несет a-аминогруппу, называют N-концевым, несущий свободную a-карбоксильную группу – С-концевым. Название пептида состоит из перечисления тривиальных названий аминокислот, начиная с N-концевой. При этом суффикс «ин» меняется на «ил» для всех аминокислот, кроме С-концевой.
Пример:
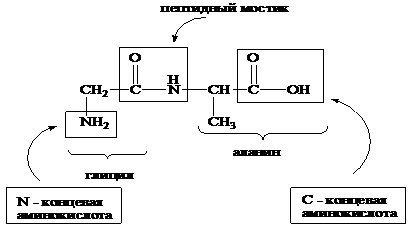
Глицилаланин или Gly-Ala
Классификация пептидов
1. Гомомерные– при гидролизе образуют только аминокислоты.
2. Гетеромерные – при гидролизе кроме a-аминокислот, образуются неаминокислотные компоненты, например: а) гликопептиды; б) нуклеопептиды; в) фосфопептиды.
Синтез пептидов
В процессе синтеза пептида должна образоваться пептидная связь между карбоксильной группой одной аминокислоты и аминной группой другой аминокислоты (при синтезе дипептида) или другого пептида (при синтезе три- и более полипептидов).
Из двух аминокислот возможно образование двух дипептидов:
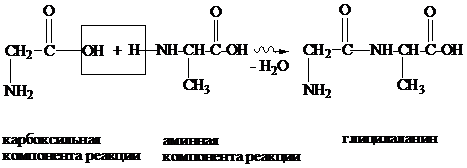
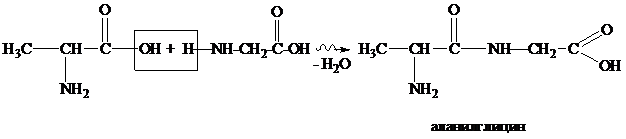
Из трёх аминокислот можно получить трипептиды. То есть для синтеза пептида заданного строения эти формальные схемы не подходят. Для синтеза пептида необходимы следующие преобразования исходных аминокислот:
1) Предварительная временная защита всех (или некоторых) функциональных групп, которые не участвуют в образовании пептидной связи.
Существуют два типа защитных групп:
а) N-защитные (временная защита NH2-группы);
б) С-защита (временная защита -СООН-группы).
2) Дополнительная активация тех групп, которые непосредственно образуют пептидную связь.
3) Удаление защитных групп после образования пептидной связи.
Для того чтобы синтезировать, например, глицилаланин необходимо преобразовать исходные аминокислоты, и проведя соответствующие модификации аминокислот. Тогда получение глицилаланина можно представить следующей схемой:


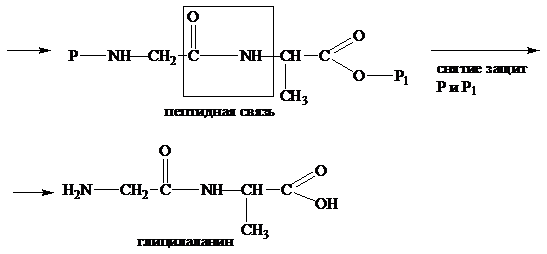
После образования пептидной связи защитные группы снимаются. Защитные группы должны сниматься легко, в мягких условиях, так чтобы при этом пептидная связь (амидная группа) не затрагивалась.
Применение аминокислот
Аминокислоты играют исключительную роль в жизнедеятельности живого организма, так как они входят в состав белков. При попадании в желудочно-кишечный тракт белки пищи под действием ферментов распадаются на составляющие их аминокислот, которые затем используются организмом для построения собственных белков тканей, кожи и т.д. Отдельные аминокислоты используются в разнообразных синтезах, в аналитической химии, в пищевой промышленности в качестве вкусовых добавок, например, мононатриевая соль глутаминовой кислоты имеет вкус и запах куриного бульона.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|