
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
330.Анилин құрылысы төмендегідей аминдерге жатады: С6Н5NH2 бірінші ароматты
айтады
79. Тө менде берілген қ оспалардың ішінде буферлік ә сер танытатыны: CH3COOH + CH3COONa.
80. Еріген заттың массалық ү лесі кө рсетеді: 100 г ерітіндідегі еріген заттың массасы
81. И. М. Сеченов заң ы бойынша: Газдың электролит ерітіндісінде ерігіштігі қ ысым ө скен сайын тө мендейді
82. Дұ рыс тұ жырымды таң дап алың дар. Ерітінділер: кем дегенде екі қ ұ рамдас бө ліктен тұ ратын қ ұ рамы ө згермелі гомогенді жү йелер (кө пкомпоненнтті гомогенді жү йе)
83. Жасушаны тұ здың гипертонды ерітіндісіне батырғ анда байқ алатын қ ұ былыс: Плазмолиз
84. Қ антты емес диабет кезінде кө п мө лшерде сұ йылтылғ ан несеп бө лінеді, оның осмостық қ ысымы 154, 6 кПа-ғ а дейін тө мендейді. Осындай несептің ерітіндісі қ ан плазмасына (Росм =740-780 кПа) қ атысты........ ерітінді болып саналады : Гипотонды
85. Мына тең деу С = kP газдар ү шін кімнің заң ының математикалық ө рнегі болып табылады: Генри заң ы
86. Ерітіндідегі сутек иондарының концентрациясы ө скенде: Ph ерітіндісінің сандық мағ ынасы тө мендейді
87. Мына жұ птардың буферлік ә рекет танытатыны: Н2CO3 + NaHCO3.
88. Молярлық концентрациясы 0, 01 моль/л калий гидроксиді КОН ерітіндісінің рН мә ні: рН = 12.
89. Тө менде келтірілген жұ птардың ішінен қ анның буферлік жү йесіне кіретінін таң дап алың дар: H2CO3 +KHCO3
90. Ерітіндінің молялдық концентрациясы дегеніміз: 1000г еріткіштегі еріген зат мө лшері
91. Коллигативтік қ асиеттерді анық тайтын қ асиеттер: Еріген зат пен еріткіш арасындағ ы ә рекеттесу
92. Ерітіндінің осмостық қ ысымы тә уелді: жартылай ө ткізгіштің мембрананың екі жағ ының концентрациясының айырымына тә уелді
93. Жасушаны гипотонды ерітіндіге батырғ анда байқ алатын қ ұ былыс: Эндоосмос
94. Газдардың ерігіштігінің температурағ а байланысты тә уелділігі: газдың ерігіштігі темп жоғ арылағ ан сайын тө мендейді газдың ерігіштігі -экзотермиялық процесс
95. Буферлік ерітінділерді дайындау ү шін мына заттардың жұ бын алуғ а болады: H2CO3+NaHCO3
96. Ерітіндінің молярлық концентрациясы дегеніміз: 1 л ерітіндідегі еріген заттың мө лшері
97. Ерітінді бетіндегі еріткіштің қ анық қ ан бу қ ысымының салыстырмалы тө мендеуін анық тайтын кө рсеткіш: Еріген заттың мольдік ү лесіне
98. Ерітіндінің осмостық қ ысымы мынағ ан тә уелді : жартылай ө ткізгіштің мембрананың екі жағ ының концентрациясының айырымына тә уелді
99. Қ айнау температурасы кезінде : Қ анық қ ан бу қ ысымы атмосфера қ ысымына тең
100. Берілген ерітіндімен салыстырғ анда осмостық қ ысымы жоғ ары ерітінді былайша аталады: Гипертонды
101. Ерітінді бетіндегі еріткіш қ анық қ ан бу қ ысымының салыстырмалы тө мендеуі тура пропорционал болады: еріген заттың молдік мө лшеріне тең
102. Эбуллиоскопиялық тұ рақ ты тә уелді: еріткіштің табиғ атына
103. Буферлік ә рекет танытын ерітінді: H2CO3+KHCO3
104. рН мә ні берілген буферді дайындау ү шін мына шамаларды білу қ ажет : буферлік жү йенің компоненттерінің сә йкестігін есептеу
105. Сілті бойынша да, қ ышқ ыл бойынша да ерітіндінің буферлік сыйымдылығ ы жоғ ары болуы ү шін рН =9, 2 буферлік ерітінді дайындағ ан кезде мына қ оспаны алу керек : D. Боратную, К = 6, 0∙ 10-10.
106. Қ анғ а изотонды глюкоза ерітіндісінің концентрациясы : 5%
107. Қ анғ а изотонды натрий хлориді ерітіндісінің концентрациясы: 0, 9 пайыз
108. Байланыс полюстілігі жоғ арырақ молекула: HF
109. Адамдар мен жануалардың тіршілігіне хлор мына формада қ ажет: Хлорид
110. Атомдары иондық байланыспен қ осылғ ан қ осылыс: NaF
111. Адамдар мен жануарлар организміндегі минералдық алмасуды зерделеу ү шін қ олданылады: Радиоизотоптар
112. Органоген-элементтер қ атарын кө рсетің дер: C. N. O. H. S
113. Организмдегі кальцийдің мө лшері шамамен 1, 4% (70кг дене массасына 1 кг). Бұ л элементті мына топқ а жатқ ызуғ а болады: Макроэлементтің
114. Медициналық практикада дезинфекциялайтын зат жә не цианидтер ү шін уқ айтарғ ыш ретінде қ олданылатын маргенецтің қ осылысын кө рсетің дер. Оны қ олдану мына химиялық қ асиетіне негізделген: KMnO4. Қ ышқ ылдық /окислитель
115. Уланғ анда, толассыз қ ұ су, жедел қ ан жоғ алтқ анда, шок кезінде, жараны, сілемей қ абатын жуу ү шін қ олданылады: натрий хлориді
116. Мына кешенді иондағ ы [Al(OH)x]ˉ кешентү зушінің координациялық санын анық таң дар, егер орталық атомның заряды +3, ал лигандтың заряды -1 болса: 4
117. Калий гексанитрокобальтатының (III) химиялық формуласы: . K3[Co(NO2)6].
118. Электрстатикалық тартылыс кү штерінің нә тижесінде тү зілген химиялық байланыс былайша аталады: иондық
119. Азот молекуласындағ ы байланыстың тү рі: ковалентті полюссіз
120. Кө п ретте кешентү зуші ретінде бола алады: катиондар
121. Мына қ осылыс ү шін кешеннің заряды нө лге тең: [Pt+2(NH3)2Cl2)
122. Қ ұ рамы [Pt(NH3)3Cl]Cl болатын кешенді қ осылыстың аталуы: хлоротриаминплатина II валентті хлориды
123. Кешенді қ осылыстарда кешентү зуші мен лигандтардың арасында міндетті тү рде байланыстың мынатү рі болады: донорлы акцепторлы механизм бойынша тү зілген
124. Қ алқ анша безі тироксиннің негізгі элементі (массалық ү лесі бойынша 65%): иод
125. Ауыз суындағ ы бұ л элементтің аздағ ан концентрациялары қ осылыстар тү рінде тіс жегісінің алдыналады, ал жоғ ары концентрациялары – тіс эмалінде дақ тардың пайда болуын тудырады: фтор
126. Микроэлементтердің қ атарын кө рсетің дер: Fe. Zn. F. Mo. Cu
127. Адам жә не жануарлар тіршілігі ү шін фосфор мына тү рде қ ажет: фосфат
128. d-Қ атарының микроэлементтерін кө рсетің дер: Fe CO CR
129. Адам жә не жануарлар тіршілігі ү шін фтор мына тү рде қ ажет: фторид
130. Организмде иод кө п мө лшерде кездесетін ағ за: Қ алқ анша без
131. Организмге ауыз суы жә не тағ амдық заттардың қ ұ рамында келіп тү сетін су былайша аталады: Экзогенді
132. Донорлық -акцепторлық механизм бойынша коваленттік байланыс тү зілетін қ осылыс: 𝑵 𝑯 𝟒 𝑪 𝒍
133. Екі ортақ тасқ ан электрон жұ птары арқ ылы екі атомның арасында тү зілетін байланыс былайша аталады: Ковалентті байланыс
134. Кешенді қ осылыстарда лигандтар мынадай қ асиеттер кө рсетеді: электронды жұ птың доноры
135. Мына кешенді қ осылыстағ ы [Ni(NH3)6]Cl3 электрон жұ птарының доноры мен акцепторын кө рсетің дер: 𝑵 𝒊 +𝟑 - акцептор, 𝑵 𝑯 𝟑 -донор
136. Бромопентаамминкобальт(III) сульфаты атауына сә йкес келетін кешен: [Co(𝑵 𝑯 𝟑 )𝟓 𝑩 𝒓 ]𝟐 𝑺 𝑶 𝟒
137. Тұ рақ тырақ кешенді ион болып табылады: . Кн[Fe(CN)6]3- = 1, 0∙ 10-31.
138. р-Қ атарының микроэлементтерін кө рсетің дер: Br, I, F
139. Хлор молекуласындағ ы химиялық байланыстың тү рі: Коваленттік полюсті
140. Байланысқ ан атомдар ядроларының арасындағ ы қ ашық тық тың аталуы: ұ зақ байланыс
141. Кешентү зуші – металл ионының координациялық саны ең алдымен мынағ ан тә уелді: МЕТАЛЛ ТАБИҒ АТЫНА
142. Тө менде келтірілген қ осылыстардың ішінен ішкі кешенді қ осылыстарғ а (хелаттар) жататыны: гемоглобин
143. Органоген-элементтер қ атарын кө рсетің дер: C, O, N, P, S, H
144. Организм ү шін уытты элементке жатқ ызуғ а болады: Қ ОРҒ АСЫН,
145. Табиғ аттағ ы (бү кіл Ә лемдегі) ең кө п тарағ ан элемен: ОТТЕГІ
----146. Атомның заряды тең болады : элементтің реттік нө меріне жә не протон санына тең.
147. Молекуладасында байланыс s- жә не p-электрон бұ лттарының қ абысуынан пайда болғ ан: NH3
148. Қ ышқ ылдық қ асиеттері ө те айқ ын байқ алатын заттың формуласы HCl
149. Кальций мен фтор негізінен жинақ талатын нысан: ТІС ЭМАЛІ
150. Асқ азан сө лінің қ ұ рамына кіретін қ ышқ ыл: ТҰ З Қ ЫШҚ ЫЛЫ
151. Уыттылығ ы ө те жоғ ары (улы) элементтердің қ атары: As, Tl, Hg, Cd, U
152. Антисептикалық, кү йдіргіш ә сер кө рсететін зат: AgNO3
153. Адамдар мен жануарлардың тыныс алу ферметтерінің қ ұ рамына кіретін топтар: ФЕРРОПОРФИН
154. Мына кешендегі Na4[Сd(ОН)6] кешентү зуші-ионның координациялық санын (КС) кө рсетің дер :: 6
155. Кешенді қ осылыстардың мына белгілерінің ішінен оларды жіктеуге негіз болатындарын таң дап алың дар:
1. Лигандтардың табиғ аты 2. Кешентү зушінің табиғ аты.
3. Кешеннің бояуы. 4. Кешенді ионның заряды.
5. Кешентү зушінің координациялық саны.
ЖАУАБЫ: 1, 4
156. Лигандтың дентаттылығ ы дегеніміз: ІШКІ КООРДИНАЦИЯДАҒ Ы ЛИГАНДТАР АЛАТЫН ОРЫН САНЫ
157. Орбитальдық квант саны атомның мына қ асиеттерін анық тайды: АТОМДАҒ Ы ЭЛЕКТРОННЫҢ ЭНЕРГИЯСЫН ЖӘ НЕ ЭНЕРГЕТИКАЛЫҚ ДЕҢ ГЕЙІН, ЯҒ НИ АО Ө ЛШЕМІН АНЫҚ ТАЙДЫ.
158. s-Орбитальдағ ы электрондардың максимал саны: 2
159. р-Орбитальдағ ы электрондардың максимал саны: 6
160. Бас квант санының n қ абылдайтын мә ндері: 1-7 МӘ НДЕРІН (ПЕРИОДТЫҚ ЖҮ ЙЕДЕГІ ПЕРИОД НОМЕРІНЕ СӘ ЙКЕС) Қ АБЫЛДАЙДЫ.
----161. d-Элементтеріне жататын элементтер жұ бы:
162. Тө менде келтірілген ү шінші период элементтерінің ішінен айқ ын бейметалдық қ асиеттер кө рсететіні: P, S, CL
163. Иондық байланыс дегеніміз: ИОНДЫҚ БАЙЛАНЫС КАТИОНДАР МЕН АНИОНДАРДЫН АРАСЫНДА ЭЛЕКТРО-СТАТИКАЛЫҚ ТАРТЫЛУ КҮ ШІНІҢ НӘ ТИЖЕСІНДЕ ПАЙДА БОЛАДЫ.
164. Коваленттік байланыс дегеніміз: КОВАЛЕНТТІК БАЙЛАНЫС – ОРТАҚ ЭЛЕКТРОН ЖҰ БЫН ТҮ ЗУ АРҚ ЫЛЫ ПАЙДА БОЛАТЫН ХИМИЯЛЫҚ БАЙЛАНЫС.
165. Донорлық -акцепторлық байланыс дегеніміз: БІР АТОМНЫҢ ЭЛЕКТРОН ЖҰ БЫ (ДОНОРЫ) ОРТАҚ, АЛ ЕКІНШІ АТОМНАН БОС ОРБИТАЛЬ (АКЦЕПТОР) БОЛАДЫ
166. Мына қ атарда N2O3, P2O3, As2O3, Sb2O3, Bi2O3: ОКСИДТЕР
167. Сутектік байланыс дегеніміз: СУТЕК АТОМЫ МЕН ЭЛЕКТРТЕРІСТІЛІГІ ЖОҒ АРЫ АТОМДАР АРАСЫНДА БОЛАТЫН ХИМИЯЛЫҚ БАЙЛАНЫС ТҮ РІ
----168. Периодта элементтің реттік нө мірі ө скенде оксидтер қ атарындағ ы қ ышқ ылдық қ асиеттер: Қ ышқ ылдық қ асиет кү шейед
169. Бейметалдарғ а жататын элементтердің қ атары: H, B, C, Si. P, O, S, ГАЛОГЕНДЕР, АСЫЛ ГАЗДАР
170. Бір элементтің екі изотопының атомдары ерекшеленеді: ПРОТОН САНЫ БІРДЕЙ, БІРАҚ АТОМДЫҚ МАССАЛАРЫ ЖӘ НЕ НЕЙТРОН САНЫ Ә РТҮ РЛІ
171. Кү рделі бейорганикалық заттарды ә детте тө рт топқ а бө леді: ТҰ ЗДАР, НЕГІЗДЕР, ОКСИДТЕР, Қ ЫШҚ ЫЛДАР
172. Оксидтер деп мына қ осылыстарды айтады: БІРЕУІ ОТТЕК БОЛЫП КЕЛЕТІН БИНАРЛЫ Қ ОСЫЛЫС
----173. Пероксидтер деп мына қ осылыстарды айтады: Оттегінің екі атомынын тұ ратын қ осылыстар. Тотығ у дә режесі 0, ал келесінікі -2 тең. Переоксидті қ осылыс Н2О2, ВаО2
----174. Екідайлы оксидтерге жататын қ атар: Be, Al, Ga, Ge, Sn, Pb, Sb, Bi, Po осы элементтердің оксидттері
----175. Негіздерге қ ышқ ылдармен реакция тә н, олар....... реакциясы деп аталады.
----176. Н2 молекуласындағ ы байланыстың тү рі: Ковалентті полюссіз
177. Сутектің тотығ у дә режесі -1 болатын қ осылыс : LiH, KH, NaH, RbH, CsH, BeH2, MgH2, CaH2, AlH3
178. Оттектің тотығ у дә режесі -1 болатын қ осылыс: СУТЕГІ АСҚ ЫН ТОТЫҒ Ы H2O2
----179. Байланыстың сипатын былайша болжауғ а болады: ә ртү рлі электртерістіктер
180. Химиялық реакция міндетті тү рде энергияны бө ліп немесе сің іріп жү реді, себебі : СЕБЕБІ ХИМИЯЛЫҚ РЕАКЦИЯ КЕЗІНДЕ БІР БАЙЛАНЫСТАР Ү ЗІЛІП, БАСҚ АЛАРЫ ТҮ ЗІЛЕДІ
----181. Иондық қ осылыстардан тұ ратын қ атар: Металлды бар қ осылыстар
----182. Табиғ атта тек ионды қ осылыстар тү рінде кездесе алатын металдардың қ атарын кө рсетің дер: Қ алайыдан кейін металлдар
----183. Сумен сутекті бө ле ә рекеттесетін металдардың қ атарын кө рсетің дер: К, Na, Са
----184. Стандартты сутек электродынан жә не ө зінің тұ зына батырылғ ан металл электродынан тұ ратын гальваникалық элементте сутек бө ле жү ретін реакция жү реді. Металды кө рсетің дер:
----185. Ерітіндінің рН-ын мына тізбектің кө мегімен ө лшеуге болады: хингидритті электрод немесе фазалық электрод
----186. Электродтық потенциалды есептеу ү шін қ олданылатын формула: Е=E0+(RT/nF)*ln(a0x/aRed)
----187. Тү рлі электродтардың тепе-тең діктегі потенциалының температура мен электролиттің концентрациясына тә уелділігі:
----188. Мембраналық потенциал негізінен мына иондар жұ бының концентрациясымен анық талады:
189. Концентрациялары ә р тү рлі бір электролиттің екі ерітіндісінің немесе екі ә р тү рлі электролит ерітінділерінің жанасу шекарасында пайда болатын потенциал былайша аталады: ДИФФУЗЛЫҚ
190. Бейстандартты жағ дайлардағ ы тотығ у-тотық сыздану потенциалын анық тайтын фомула : E=E0 + (0. 059/n)*lg[ОКИС]/[ВОССТ]
191. Потенциометрлік титрлеу деп титрлеу барысында эквиваленттік нү кте былайша анық талатын титриметрлік талдау ә дісін айтады: ЕРІТІНДІ МЕН ГАЛЬВАНИКАЛЫҚ ТІЗБЕК ЭЛЕКТРӨ ТКІЗГІШ КҮ ШІН Ө ЛШЕУІ
----192. Кондуктометрлік титрлеу деп титрлеу барысында эквиваленттік нү кте былайша анық талатын титриметрлік талдау ә дісін айтады:
----193. Молярлық концентрациясы бірдей электролиттердің сулы ерітінділерінің арасында электрө ткізгіштігі ең жоғ ары болатын электролит:
----194. Молярлық концентрациясы бірдей электролиттердің сулы ерітінділерінің арасында иондық кү ші ең жоғ ары болатын электролит:
----195. Молярлық концентрациясы бірдей электролиттердің сулы ерітінділерінің арасында электрө ткізгіштігі ең жоғ ары болатын электролит:
196. Тотығ у-тотық сыздану электроды дегеніміз: Қ Ұ РАМЫНДА ИНЕРТТІ МЕТАЛЫ БАР, ЕРІТІНДІГЕ БАТЫРЫЛҒ АН БІР УАҚ ЫТТА ТОТЫҒ АТЫН ЖӘ НЕ Қ АЛПЫНА КЕЛГЕН ЗАТТЫҢ ФОРМАСЫ
197. Мембраналық потенциал негізінен мына катионның концентрациясымен анық талады: K, Na
198. Тотығ у-тотық сыздану потенциалының шамасы тә уелді болады: ЕРІТІНДІДЕГІ ЗАТТЫҢ ТОТЫҚ Қ АН ЖӘ НЕ ТОТЫҚ СЫЗДАНҒ АН ФОРМАСЫНЫҢ КОНЦЕНТРАЦИЯСЫ
199. Тотығ у-тотық сыздану электроды - қ ұ рамында.... бар ерітіндіге батырылғ ан.... тұ ратын жү йе. Дұ рыс сө здерді орнына қ ойың дар. ИНЕРТТІ МЕТАЛЛ, БІРУАҚ ЫТТА ТОТЫҚ Қ АН ЖӘ НЕ ТОТЫҚ СЫЗДАНҒ АН ЗАТ ФОРМАСЫНДА
200. Электрө ткізгіштігінің мә ні ең жоғ ары болатын биологиялық сұ йық тық ты немесе адам организмінің тінін кө рсетің дер: Қ АН, ЛИМФА
201. Электрө ткізгігштігінің мә ні ең тө мен адам организмінің тінін кө рсетің дер: СҮ ЙЕК, МАЙ, ЖҮ ЙКЕ
-----202. Электролиттер ерітінділеріндегі электр тогын тасымалдаушылар -....., олар электролиттің ....... нә тижесінде тү зіледі. Жіберілген сө здерді орнына қ ойың дар. Электролиттер, электрондар
-----203. Стандартты сутектік электрод – бұ л: гальваникалық элементтер мне ә ртү рлі электрохимиялық ө лшеулерде салыстырмалы ө лшем ретінде қ олданылатын элкетрод
-----204. Мыс электродының потенциалын мына формула бойынша анық тауғ а болады: по уравнению Нернста ECu/Cu2+ = E0Cu/Cu2+ + (R • T / z • F) • ln [Cu2+] = E0Cu/Cu2+ + (0, 059 / z) • lg [Cu2+]
205. Мембраналық потенциал – мына шекарада пайда болатын потенциал: ЕКІ ЕРІТІНДІНІ БӨ ЛІП ТҰ РАТЫН Ә РТҮ РЛІ Қ Ұ РАМДЫ НЕМЕСЕ СОЛ ЭЛЕКТРОЛИТТІҢ Ә РТҮ РЛІ КОНЦЕНТРАЦИЯСЫН БӨ ЛІП ТҰ РАТЫН МЕМБРАНАНЫҢ ЖАРТЫЛАЙ Ө ТКІЗГІШТІК Қ АБАТЫ АРАСЫНДА
----206. Тө мендегі кондуктометрлік титрлеу қ исығ ы мына реакцияғ а сә йкес келеді: гидролиз дә режесі ө згергенде
207. Фазааралық бө ліну ауданы ө скенде беттік энергияның ө згеруі: Ө СЕДІ
208. Кө міртек(IV) оксиді қ атты кальций оксидіне адсорбцияланғ анда СаСО3 тү зіледі. Бұ л ү дерістің атауы: ХИМИЯЛЫҚ АДСОРБЦИЯ
209. Мына берілген заттардың қ айсылары: Nа2SО4 (1), Н3РО4 (2), КОН (3), изоамил спирті (СН3)2СН(СН2)2ОН (4), анилин С6Н5NН2 (5), пальмитин қ ышқ ылы СН3(СН2)14СООН (6) суғ а қ атысты беттік белсенділік қ асиеттер танытады : 4-5-6
210. Адсорбция изотермасы адсорбцияның мына факторғ а тә уелділігін кө рсетеді: КОНЦЕНТРАЦИЯСЫ
----211. Мына қ атардағ ы СН3СН2СН2СООН > СН3СН2СООН > СН3СООН беттік керілістің заң дылығ ын сипаттайтын ереже:
212. Қ атты дененің немесе сұ йық тық тың газ тә різдес немесе еріген затты сің іруі былайша аталады: Адсорбция
213. Пластмасса пластинкасына бір тамшыдан: бензин, сынап жә не су тамызылды. Бұ л кезде бензиннің тамшысы жайылып кетеді, сынап тамшысының формасы шар тә різді болады, ал су тамшысы жалпаяды: сынап
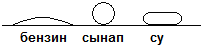
Осы заттарды беттік керілістерінің тө мендеуі бойынша қ атарғ а орналастырың дар.
214. Оң адсорбция кезіндегі адсорбенттің беттік керілісі....... жә не оң адсорбцияланатын заттар........ деп аталады: Тө мендейді, жоғ арғ ы-активті заттар
215. Панет-Фаянс ережесіне сә йкес Ca2+, Mg2+, Cl‾ , Br‾ , J‾ , K+ иондарының ішінен АgCl бетінде талғ амды адсорбциялана алатындары: Cl. Br. I
216. Қ атты дененің бетінде жү ретін молекулалық адсорбция мына заттарғ а тә н: электролиттік емес жә не газдарғ а
----217. Судың бетінде ББЗ молекуласының дұ рыс бағ ытталуына сә йкес келетін сурет:
218. Мына берілген иондардың: NO3‾, Na+, PO43-, Sr2+, Al3+, Br‾, SO42- адсорбент SrSO4 бетінде адсорбциялана алатындары: Sr2+, So42-
219. Г = –С/RT(Δ σ /Δ C) тең деуі қ андай фазалардың бө ліну шекарасындағ ы адсорбцияны сипаттайды: сұ йық тық -сұ йық тық , сұ йық тық -газ
220. Мына тұ жырымдама: «Қ анық қ ан қ ышқ ылдар мен спирттердің қ атарында тізбек бір СН2-тобына ұ зарғ анда сулы ерітіндіде гомологтың беттік белсенділігі 3-3, 5 есе ө седі» сә йкес келетін ереже (заң ): Дюило-Траубе ережесі
----221. Коллоидтық химияда қ ос электрлік қ абат тү зілген кезде бет аудан зарядының таң басын анық тау ү шін қ олданылатын тұ жырым (ереже):
222. Бір заттың екінші бір зат бетінде жинақ талу ү дерісі былайша аталады: адсорбция
223. Атмосфералық қ ысымның кү рт тө мендеуі кессон ауруын тудыруы мү мкін. Мұ ндай сырқ атты емдеу ү шін: Ауруды барокамерағ а апарып жоғ ары қ ысымғ а тү сіріп кейін қ ысымды жайлап тү сіреді
224. Мына тең деу Г = Гmax P/ (K + P)..... тең деуінің математикалық ө рнегі болып табылады: Ленгмюра
225. Талғ амды адсорбцияны анық тайтын ереже: Панет Фаянс
226. Бү йректің жұ мыс жасауының негізінде жатқ ан ү деріс: Диализ
227. Пластинкағ а бір тамшыдан ү ш сұ йық тық тамызылды:
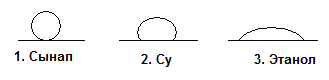
Осы заттарды беттік керілістерінің ө суіне қ арай бір қ атарғ а орнналастырың дар: 1, 3, 2
----228. Ө кпенің жоғ ары адсорбциялық ә сері мына физикалық сипаттаманың салдарына байланысты:
229. Сумен талғ амды суланатын беттердің аталуы: Гидрофилді
----230. Газ фазадан адсорбенттің қ атты бетіне сә йкес келетін адсорбция изотермасының қ исығ ы:
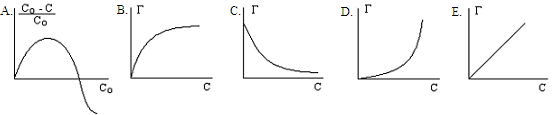
231. Беттік белсенді зат: НСl
232. Коллоидтық ерітінді арқ ылы жарық шоғ ын ө ткізгенде байқ алатын қ ұ былыс: Жарық тың шашырауы, (дифрокатция)
233. Коллоидтық ерітінділерді тазарту ә дісі: Диализ, Электродиализ, Ультрафильтрозия
234. Электрофорез кезінде қ озғ алады: дисперсті фазаның зарядталғ ан бө лшегі
235. Мыс(ІІ) гидроксидінің золі теріс зарядталғ ан бө лшектерден тұ рады. Мына қ осылғ ан электролиттердің ішінде коагуляция табалдырығ ы ең тө мен: алюминий хлориді (III) AlCl3
236. Салмақ кү штерінің ә серінен қ алқ ып жү рген (диспергацияланғ ан) бө лшектердің тұ ну жылдамдығ ы ескермеуге болатындай ө те аз жү йелер былайша аталады: Кинетикалық жә не агрегаттық тұ рақ тылық
237. Теріс зарядталғ ан бө лшектері бар коллоидтық ерітіндінің бө лшектері қ ай электродқ а қ арай қ озғ алады: Анод
238. Нә руыздың ісіну дә режесінің ортаның рН-ына тә уелділігі екі максимумы жә не бір минимумы бар қ исық пен сипатталады. Минимумғ а сә йкес келетін нү ктені былайша атайды: изоэлектрлік нукте
239. Коллоидтық бө лшектердің аттас зарядтарының жә не (немесе) еріткіш молекулаларынан тұ ратын сольват қ абығ ының болуымен байланысты тұ рақ тылық тың тү рін былайша атайды: агрегаттық седиментациялық тұ рақ тылық
240. Тө менде келтірілген анық тамалардың ішінен электрофорезге сә йкес келетінін таң дай алың дар: сыртқ ы электр ө рісі ә серінен дисперсті фазаның зарядталғ ан бө лшектердің дисперсті ортағ а қ атысты қ озғ алуы
241. Бө лшектері теріс зарядталғ ан кремний қ ышқ ылының золі ү шін мына қ атарда СrС13 (1), Ва(NО3)2 (2), К2SО4 (3) коагуляция табалдырығ ы былайша орналасады: 3> 2> 1
242. Дисперстік фазасы сұ йық ортада қ алқ ып жү рген ө лшемдері 10-5 м-ден (100 мкм) жоғ ары болатын қ атты бө лшектерден тұ ратын микрогетерогенді жү йенің аталуы: cуспензия
243. Дисперстік фаза бө лшектерінің ірірек агрегаттарғ а жабысуы (бірігуі) былайша аталады: коагуляция
244. Оң зарядталғ ан бө лшектері бар зольге теріс зарядты бө лшектері бар зольді қ осқ ан кезде байқ алатын ү деріс: Ө ЗАРА КОАГУЛЯЦИЯ
245. Коллоидтық ерітінділердің молекулалық -кинетикалық қ асиеттеріне жатады: БРОУНДЫҚ Қ ОЗҒ АЛЫС
246. Каучуктың ісіну дә режесі ең тө мен болатын еріткіш: СУ
247. Ионданғ ан негіздік жә не қ ышқ ылдық топтарының саны тең полиэлектролит молекуласының зарядтары бірдей болатын кү йі былайша аталады: ИЗОЭЛЕКТРИЧЕСКИМ СОСТОЯНИЕМ
248. Температура жоғ арылағ анда қ ұ рылымданғ ан жү йелердің тұ тқ ырлығ ы: Қ Ұ РЫЛЫМЫН БҰ ЗЫЛУЫНА БАЙЛАНЫСТЫ ТӨ МЕНДЕЙДІ
249. Артық мө лшерде алынғ ан кү міс нитратының сулы ерітіндісіне баяу натрий хлоридінің сулы ерітіндісі қ осылды. Кү міс хлоридінің коллоидтық ерітіндісі тү зілді. Золь бө лшектерінің заряды: ОҢ
250. Оң зарядталғ ан бө лшектері бар коллоидтық ерітіндіге мына иондарды қ осқ ан кезде жоғ ары коагуляциялық белсенділік жә не тез коагуляция байқ алады: РО4 3-
251. Фарадаей-Тиндаль эффекті мына жү йелерде байқ алады: КОЛЛОИДТЫ ЕРІТІНДІЛЕРГЕ
252. Дисперстік фазасы сұ йық ортада қ алқ ып жү рген ө лшемдері 10-7 – 10-9 м (1-100 мкм) болатын қ атты бө лшектерден тұ ратын микрогетерогенді жү йенің аталуы: КОЛЛОИДТЫ - ДИСПЕРСТІ
253. Жартылай ө ткізгіш мембраналардың кішімолекулалық қ оспаларды (иондар мен молекулаларды) ө ткізіп, коллоидтық бө лшектерді ұ стап қ алу қ асиеттеріне негізделген қ ұ былыс: ДИАЛИЗ
254. Дисперстік фазасы сұ йық ортада қ алқ ып жү рген ө лшемдері 10-5 см (100 мкм) болатын сұ йық бө лшектерден тұ ратын микрогетерогенді жү йелердің аталуы: СУСПЕНЗИЯ
----255. Сұ йық тық тың беттік керілісі температура жоғ арылағ анда:
256. “Агрегаттық тұ рақ тылық ” дегеніміз: БӨ ЛШЕКТЕРДӘ І ФАЗАЛЫҚ ІРІЛЕТУІНЕ ЖЕТЕТІН ПРОДУЦЕНТТЕРГЕ ЖҮ ЙЕНІҢ Қ АРСЫ ТҰ РУ Қ АБІЛЕТІ
257. Артық мө лшерде алынғ ан NaJ сулы ерітіндісіне баяу AgNO3 сулы ерітіндісі қ осылды. Кү міс иодидінің коллоидтық ерітіндісі тү зілді. Золь бө лшектерінің зарядын кө рсетің дер: ТЕРІС
258. Электроосмос кезінде электр ө рісінде қ озғ алатын бө лшектер : ДИСПЕРСТТІК ОРТА
259. Ас қ орыту кезіндегі майларды эмульгациялайтын зат: Ө Т Қ ЫШҚ ЫЛЫ
260. Инсулиннің изоэлектрлік нү ктесі 6-ғ а тең. Нә руыздың электрофорездік қ озғ алғ ыштығ ы ең тө мен болатын рН-тың мә ні: 6
261. ЖМҚ концентрациясы ө скенде олардың осмостық қ ысымы тезірек ө седі де, Вант-Гофф заң ына бағ ынбайды. Ауытқ удың себебі мынада: ЖМҚ ИКЕМДІ ТІЗБЕКТЕР БІРНЕШЕ Қ ЫСҚ А МОЛЕКУЛАЛАР РЕТІНДЕ Ә РЕКЕТ ЕТЕДІ
----262. Сынауық тағ ы суғ а шайқ ай отырып, бірнеше тамшы шайыршық тың (канифоль) ерітіндісі қ осылды. Коллоидтық ерітіндіні алу ә дісінің аталуы:
263. Кө п мө лшерде алынғ ан кү міс нитратының сулы ерітіндісіне натрий хлоридінің сулы ерітіндісі абайлап қ осылды. Коллоидтық ерітіндіні алу ә дісінің аталуы: ОҢ
264. Дисперстік фазасы сұ йық ортада қ алқ ып жү рген ө лшемдері 10-5 см-ден (100мкм) жоғ ары қ атты бө лшектерден тұ ратын микрогетерогенді жү йенің аталуы: СУСПЕНЗИЯ
265. Ә р тү рлі зарядталғ ан бө лшектері бар зольдерді араластырғ ан кезде орын алатын қ ұ былыс: КОЛЛОИДТЫ Ө ЗАРА Ұ ЙҚ АС
266. Теріс зарядталғ ан бө лшектері бар мыс(ІІ) сульфиді золінің ерітіндісіне қ осылғ ан иондардың ішінде коагуляциялық қ абілеті ең жоғ арысы: Al(3+)
267. Жекелеген электролиттің ә серіне қ арағ анда электролиттер қ оспасының тиімдірек ә сері былайша аталады: cинергизм электролит
268. Эмульсияғ а жататын жү йе: гетерогенді
----269. Коллоидтық бө лшектердің ірірек агрегаттар тү зіп, бір-біріне жабысу ү дерісі былайша аталады:
----270. Желатиннің сулы ерітіндісіне спиртті қ осқ анда ерітіндіге еріген затпен байытылғ ан тамшылардың бө лінуі байқ алады. Бұ л қ ұ былыстың аталуы:
----271. Жоғ арымолекулалық заттарды (крахмал, желатин, альбумин) қ осқ анда лиофилді зольдердің электролиттердің коагуляциялық ә серіне тұ рақ тылығ ының ө суі былайша аталады:
----272. Медицинада менингитті диагностикалау ү шін жұ лын сұ йық тығ ының «алтын санын» анық тайды. «Алтын саны» мынаны сипаттайды:
273. «Протаргол» жә не «Колларгол» препараттары..... дисперсті жү йе болып табылады, ондағ ы химиялық элемент......: КОЛЛОИДТЫ ДИСПЕРСТІ ЖҮ ЙЕ, КҮ МІС, ОТТЕК, АЗОТ
274. Сірнелер мен гельдердің кө лемінің сұ йық тық тың бө лінуі салдарынан ө здігінен кішірею қ ұ былысын былайша атайды: СИНЕРЕЗИС Қ Ұ БЫЛЫСЫ
275. Субстанциялардың (бірқ атар химиялық ерітінділер немесе биологиялық қ ұ рылымдар, мысалы, жасушалардың цитоплазмалары) механикалық ә сердің нә тижесінде тұ тқ ырлық тарының тө мендету жә не тыныштық кү йде тұ тқ ырлық тарын ө сіру қ абілеті былайша аталады: ТИКСОТРОПИЯ
276. Полимердің массасы жә не кө лемінің ө суі арқ ылы жү ретін жоғ арымолекулалық қ осылыстың кішімолекулалық еріткішті ө здігінен таң дамалы сің іру ү дерісі былайша аталады: ПОЛИМЕРЛЕРДІҢ ІСІНУІ ЖӘ НЕ ЕРУІ
----277. Мицелланың формуласын жазғ ан кезде потенциаланық тағ ыш иондарды мына ережеге сә йкес таң дайды:
----278. Физиотерапевтік ә діс – дә рілік заттың ерітіндісін (иондарын) электр ө рісінің ә серінен тері немесе сілемейлі қ абат арқ ылы денеге енгізу мына қ ұ былысқ а негізделген:
279. Эмульсиядағ ы дисперстік фаза мен дисперсиялық ортаның агрегаттық кү йлерін кө рсетің дер: 1, 2- дибромэтан
280. Дұ рыс тұ жырымды кө рсетің дер: «Этиленді бромдау кезінде.... »: электрофил G- байланыстарды шабуылдайды
281. Мына формуладағ ы CH3→ CH2→ Br атомдардың арасындағ ы бағ дар кө рсете: G- бай ланыстардың тізбегі бойынша электрондық тығ ыздық тың ығ ысуы
282. Спирттер, аминдер, тиолдарғ а тә н реакцияның тү рі жә не механизмі: АN Нуклеофильді қ осып алу
283. Спирттер, аминдер, тиолдарғ а тә н реакцияның тү рі жә не механизмі: АN Нуклеофильді орынбасу
284. Спирттердің дегидратациялануы қ андай механизм бойынша жү реді: E Мономолекулярлық (элминдеу)
285. Алкендерге тә н реакцияның тү рі жә не механизмі: Электрофильді қ осылу
286. Арендерге кө бірек тә н реакцияның тү рі жә не механизмі: SE Электрофильді орынбасу
287. Қ анық қ ан кө мірсутектерге тә н реакцияның тү рі жә не механизмі: SR Радикалды орынбасу
288. Пропеннің хлорсутекпен ә рекеттесу реакциясының тү рі жә не механизмі: Электрофилді қ осып алу
289. Марковников ережесі бойынша жү ретін ә рекеттесу реакциясы: Пропеннің сутекпен
------290. Тө менде келтірілген органикалық қ осылыстың қ айсысында sp3-гибридтік кү йдегі кө міртек атомы бар: 4-хлорлы кө мірсу
291. Ацетилен молекуласының С2Н2геометриялық формасын кө рсетің дер: Сызық тық жә не диагональды
------292. Нуклеофилді бө лшектің ең маң ызды белгісін таң дап алың дар: Электрон жұ бының донорлығ ы
293. Электрофилді бө лшектің ең маң ызды (негізгі) белгісін таң дап алың дар: Электрон жұ бының акцепторлығ ы(Бос валентті орбитальдің болуы)
294. Жұ птаспағ ан электроны бар жә не заряды жоқ бө лшектің аталуы: Бос радикал жә не нейтрон
295. Ароматты кө мірсутекке жатады: Толуол, арен, финол, бензол
296. sp3-, sp2- жә не sp-гибридтік кү йдегі кө міртек атомдарына сә йкесінше қ андай валенттік бұ рыштар тә н 10905, 1200, 1800
297. Ең жоғ ары теріс индуктивтік ә сер (–Ј) танытатын топ СL
298. Қ осарланғ ан жү йеге жатады: Жауабы: С.
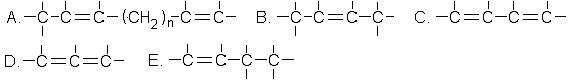
299. Бензолдың гомологтарын алғ ан кезде (Фридель-Крафтс реакциясы) алкилдеуші реагент болып табылады: R-Cl, AlCl3
300. Полимерлену реакциясы мына кө мірсутекке тә н: Изопрен
301. Бензолды синтездеуге болатын қ анық пағ ан кө мірсутек..... жә не бұ л кезде реакцияғ а заттың ...... мө лшері қ атысады: Ацетиленнің 3 молі
302. -С6Н5радикалының аталуы: Фенил
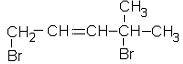
303. Қ осылысты халық аралық номенклатура бойынша атаң дар: 1, 4-дибром – 4метилпентен-2
304. Наркоз ү шін келтірілген заттардың ішінен С2Н5-О-С2Н5 формуласына сә йкес келетін затты кө рсетің дер: Диэтилді эфир (этоксиэтан)
305. Электрофилді реагенттер дегеніміз – бұ л: Электрон жұ бының акцерторы болатын бө лшектері
306. Нуклеофил – бұ л: Электрон жұ бының доноры болатын бө лшек
-----307. Радикалды реагенттер болып табылады: бос атомдар жә не жұ п емес электрондар
308. Электрофилді қ осып алу реакциясы мына қ осылыс ү шін мү мкін болады: Бутен-2 қ ышқ ылы
-----309. Келтірілген қ осылыстардың ішінде монофункциялық қ осылысқ а жатады: 1 группа Гидроксибензол (фенол)
-----310. Келтірілген қ осылыстардың ішінде полифункциялық қ осылысқ а жатады: кө п группа Жү зім (шарап) қ ышқ ылы
-----311. Келтірілген қ осылыстардың ішінде монофункциялық қ осылысқ а жатады: Пальмитин қ ышқ ылы, алкан, алкен, алкодиен, алкины
312. Келтірілген қ осылыстардың ішінде монофункциялық қ осылысқ а жатады: Ацетон
313. Бренстед қ ышқ ылдары дегеніміз мына бө лшектер: (донор)Протон беруге бейім бейтарап молекула жә не иондар
314. Бренстед негіздері дегеніміз мына бө лшектер : (акцептор) Протон қ осып алуғ а бейтарап молекула жә не иондар
-----315. Мына анық тама «Бос орбитальдары бар жә не электрон жұ бын қ осып алып коваленттік байланыс тү зуге қ абілетті атом, молекула немесе ион» сә йкес келеді : электрофил(Льюис қ ышқ ылы)
316. Коваленттік байланыс гомолиттік ү зілген кезде тү зілетінбө лшектер: Бос радикалдар
317. Бутадиен-1, 3 молекуласындағ ы С2 – С3байланысының ұ зындығ ы бутан молекуласындағ ығ а қ арағ анда қ ысқ арақ. Мұ ны немен тү сіндіруге болады: С2 мен С3 атом арасындағ ы қ осымша π -байланыстың тү зілуі
318. Брёнстед-Лоури теориясына сә йкес кү штірек қ ышқ щыл болып табылады: С2Н5ОН
319. Келтірілген орынбасарлардың қ айсысы бензол сақ инасындағ ы орто- жә не пара-орындардағ ы кө міртек атомының электрондық тығ ыздығ ын арттырады: Этил –С2Н5
-----320. Кетондар осы спирттерден тотық тырғ ан кезде алынады: Екіншілік спирттерден
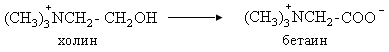
-----321. Бетаинді алу реакциясының типін кө рсетің дер: Ферменттік тотығ у
-----322. Ү шіншілік спирт: 2-метилпропанол-2
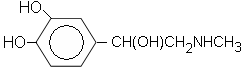
323. Адреналинге мына органикалық қ осылыстардың қ асиеттері сә йкес келеді: Аминдер, спирт
324. Этанаминді ацетамидтен жә не хлорэтаннан алу реакцияларының сә йкесінше типтерін кө рсетің дер: нуклеофильді орын басу, тотығ у
1) СН3CONH2→ С2Н5NH2 2) С2Н5Cl → С2Н5NH2
325. Хлорлы этилге NaOH сулы ерітіндісімен ә сер еткенде алынатын қ осылыс: спирт жә не натрий хлориді С2Н5ОН
326. 1, 2-диолды фрагментке сапалық реакцияны жү ргізетін қ осылыс: CuOH2
-----327. Фенолды бромдау реакциясының типі мен механизмі: Электрофильді орын басу
328. Этиленгликоль этиленнің мына затпен ә рекеттесуі кезінде тү зіледі: Калий перманганатының сулы ерітіндісі
329. Элиминдеу реакциясымен этиленді алу ү шін қ ажет бастапқ ы қ осылыс: Этанол
330. Анилин қ ұ рылысы тө мендегідей аминдерге жатады: С6Н5NH2 бірінші ароматты
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|