
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Задания районной олимпиады. по учебному предмету «Химия» 8 класс. 2018/2019 учебный год . Особенности проведения олимпиады по химии в 8 классе. Максимальное количество – 100 баллов. Выберите один правильный ответ.
УТВЕРЖДАЮ
Заведующий сектором общеобразовательной подготовки управления по образованию Полоцкого райисполкома
 А. И. Кострица
«01» апреля 2019 А. И. Кострица
«01» апреля 2019
|
Задания районной олимпиады
по учебному предмету «Химия» 8 класс
2018/2019 учебный год
Особенности проведения олимпиады по химии в 8 классе
Олимпиада по химии состоит из двух туров.
Часть А – теоретический тур, состоит из тестовых заданий. Ответы на задания части А вносятся в таблицу. В части А предусмотрен только один правильный ответ из предложенных. Максимальное количество за задания части А – 20 баллов.
Часть В – практический тур. Максимальное количество за задания части В – 80 баллов. Задания части В выполняются на листах тетради.
Обращаем ваше внимание!!! Свои данные (ФИО, учреждение, класс) вы записываете только на личной карточке. На выполнение всех заданий отводится 3 часа.
Максимальное количество – 100 баллов
Часть А ТЕСТОВОЕ ЗАДАНИЕ
Выберите один правильный ответ.
Правильный вариант ответа внесите в таблицу.
| 1 | |||||||||
1. Какая из реакций неосуществима на практике:
а) S + О2 → ;
б) Fе + О2→ ;
в) СО + О2 → ;
г) СО2 + О2 → .
2. В растворах кислот:
| а) фенолфталеин малиновый; | ||
| б) метилоранж желтый; | ||
| в) лакмус красный; | ||
| г) лакмус синий. | ||
3. Укажите пару веществ, не взаимодействующих между собой:
| а) Аl(ОН)3 и NаОН; |
| б) Р2О5 и NаОН; |
| в) SiО2 и К2О; |
| г) Р2О5 и SiО2. |
4. Атомы изотопов хрома различаются:
| а) числом нейтронов; |
| б) порядковым номером в Периодической системе; |
| в) числом электронов; |
| г) числом протонов. |
5. Выберите схему получения гашеной извести:
| а) СаО + С → ; |
| б) СаО + Н2О → ; |
в) СаСО3 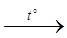 ; ;
|
| г) СаСО3 + С →. |
6. Наибольшее число атомов содержится в объеме 10 дм3 (н. у. ) газа, название которого:
| а) озон; |
| б) азот; |
| в) кислород; |
| г) гелий. |
7. С сульфатом цинка в водном растворе взаимодействует каждое из веществ, формулы которых:
| а) НСl, NаNО3, О2; |
| б) СuО, Сu(ОН)2, СuСl2; |
| в) КОН, Nа2SiО3, К2СО3 |
| г) Сu(ОН)2, Nа2S, Н2. |
8. Укажите формулу простого вещества, которое растворяется в щелочи, но не растворяется при комнатной температуре в концентрированной азотной кислоте:
| а) Аl; |
| б) Zn; |
| в) Са; |
| г) Nе. |
9. Формулы только слабых кислот приведены в ряду:
| а) НNО3, НF, НСl; |
| б) НF, НNО2, Н2S; |
| в) Н2S, Н2SО4, НNО3; |
| г) Н2SО4, НСl, НF. |
10. Степень окисления одного из атомов равна нулю в:
| а) Н2О2; |
| б) СО(NН2)2; |
| в) СН2Сl2; |
| г) FеS2. |
11. Ионная связь имеется во всех веществах, формулы которых:
а) SО2, СО2, NО2;
б) КСl, ; I2, НNО3;
в) Вr2, НВr, КВr;
г) СаО, Са(ОН)2, СаСl2.
12. Об азоте как о простом веществе можно сказать следующее:
а) расположен во втором периоде Периодической системы;
б) содержит 7 электронов;
в) реагирует с водородом обратимо;
г) расположен в V группе Периодической системы.
13. При умеренном нагревании с образованием трех продуктов
разлагается:
а) СаСO3; б) H2СO3; в) КМnО4; г) H2SiO3.
14. Число молекул, содержащихся в оксиде серы (VI) массой 8 г, равно
числу молекул в оксиде серы (IV) химическим количеством:
а) 1 моль; б) 10 моль; в) 0, 1 моль; г) 0, 5 моль.
15. Кислота образуется в результате реакции:
а) SiO2 + H2O; б) N2O5 + H2O; в) CO + H2O; г) NO + H2O.
16. 9, 03 · 1022 молекул газа (н. у. ) занимает объем (дм3):
а) 22, 4; б) 3, 36; в) 11, 2; г) 33, 6.
17. В процессе химической реакции атомы:
а) изменяются; в) разрушаются;
б) сохраняются; г) превращаются в атомы других элементов.
18. Масса атомов серы количеством 6, 02 · 1023 по сравнению с массой
такого же количества атомов меди:
а) больше в 2 раза; в) больше в 12 раз;
б) меньше в 2 раза; г) меньше в 12 раз.
19. При растворении в виде оксида Mn2O7 образуется:
а) соль; б) оксид; в) кислота; г) основание.
20. Элемент образует оксид Э2О5, его водородное соединение содержит 3, 85% водорода. Этим элементом является:
а) Р; б) V; в) As; г) Sb.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|