
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Получение.
1. Общий способ получения алкинов — отщепление двух молекул галогеноводорода от дигалогеналканов, которые содержат два атома галогена либо у соседних, либо у одного атома углерода, под действием спиртового раствора щелочи.
| С2Н5ОН | ||
| СН2Вr - СН2Вr + 2КОН | → | НС ≡ СН + 2КВr + 2Н2О, |
| С2Н5ОН | |||
| СН3 - СВr2 - СН3 + 2КОН | → | СН3-С ≡ СН + 2КВr + 2Н2О, |
2. Гомологи ацетилена можно также получать, действуя галогеналканами на соли ацетиленовых углеводородов (ацетилениды):
CH3 - C ≡ CNa + I-R → CHg - C ≡ C-R + NaI.
3. Ацетилен получают в промышленности путем высокотемпературного крекинга метана:
| 1500°С | ||
| 2СН4 | → | CH ≡ NCH + ЗН2 |
или его ближайших гомологов — этана и пропана, причем в этом случае ацетилен образуется при более низких температурах:
| 1200°С | ||
| 2С3Н8 | → | ЗС2Н2 + 5Н2 |
В лабораторных условиях ацетилен получают гидролизом карбида кальция:
СаС2 + 2Н2О = Са(ОН)2 + С2Н2 ↑
Химические свойства алкинов сходны с алкенами обусловлены наличием в их молекулах тройной связи. Типичными реакциями для ацетилена и его гомологов являются реакции электрофильного присоединения АE. Отличие алкинов от алкенов заключается в том, что реакции присоединения могут протекать в две стадии. На первой стадии идет присоединение к тройной связи с образованием двойной связи, а на второй стадии — присоединение к двойной связи.
1. Галогенирование. Галогены присоединяются к алкинам в две стадии. Например, присоединение брома к ацетилену приводит к образованию дибромэтена, который, в свою очередь, реагирует с избытком брома с образованием тетрабромэтана:
| Вr2 | Вr2 | |||
| СН ≡ СН | → | СНВr = СНВr | → | СНВr 2- СНВr2 |
Алкины, так же, как и алкены, обесцвечивают бромную виду.
2. Гидрогалогенирование. Галогеноводороды присоединяются к тройной связи труднее, чем к двойной. Для активации галогеноводорода используют АlСl3 — сильную кислоту Льюиса. Из ацетилена при этом можно получить винилхлорид (хлорэтен), который используется для получения важного полимера поливинил-хлорида.
| АlСl3 | ||
| СН ≡ СН + HCI | → | СН2 = СНСl |
В случае избытка галогеноводорода происходит полное гидрогалогенирование, причем для несимметричных алкинов на каждой стадии присоединение идет по правилу Марковникова, например:
| Аl Вr3 | ||
| СН3 - С ≡ СН + 2НВr | → | СН3 - СВr2 - СН3. |
3. Гидратация. Присоединение воды к алкинам катализируется солями ртути (II)'
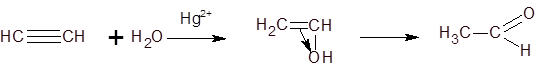
Енол альдегид
На первой стадии реакции образуется непредельный спирт, в котором гидроксильная группа находится непосредственно у атома углерода при двойной связи. Такие спирты принято называть виниловыми или енолами. Енолы - неустойчивы. В момент образования они изомеризуются в более стабильные карбонильные соединения (альдегиды или кетоны) за счет переноса протона от гидроксильной группы к соседнему атому углерода при двойной связи. При этом пи-связь между атомами углерода разрывается, и образуется пи-связь между атомом углерода и атомом кислорода. Причиной изомеризации является большая прочность двойной связи С = О по сравнению с двойной связью С = С.
В результате реакции гидратации только ацетилен превращается в альдегид; гидратация гомологов ацетилена протекает по правилу Марковникова; и образующиеся енолы изомеризуются в кетоны. Так, например, пропин превращается в ацетон:
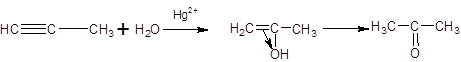
Енол ацетон
Реакция гидратации алкинов была открыта М. Г. Кучеровым (1881 г. ) и носит название реакции Кучерова.
4. Кислотные свойства. Особенностью алкинов, имеющих концевую тройную связь, является их способность отщеплять протон под действием сильных оснований, т. е. проявлять слабые кислотные свойства. Возможность отщепления протона обусловлена сильной поляризацией пи-связи: ≡ С← Н. Причиной поляризации является высокая электроотрицательность атома углерода в sp-гибридном состоянии. Поэтому алкины, в отличие от алкенов и алканов, способны образовывать соли, называемые ацетиленидами:
R - C ≡ C-H + NaH → R-C ≡ C - Na + Н2
Ацетилениды серебра и меди (I) легко образуются и выпадают в осадок при пропускании ацетилена через аммиачный раствор оксида серебра или хлорида меди (I). Эти реакции служат для обнаружения алкинов с тройной связью на конце цепи.
| НС ≡ СН + 2[Ag(NH3)2]OH → Ag-C ≡ C-Ag | ↓ | + 2NH3 + Н2O |
| белый осадок |
| R-C ≡ CH + [Cu(NH3)2]Cl → R-C ≡ C- Cu | ↓ | + NH4Cl + NH3. |
| красный осадок |
Ацетилениды серебра и меди как соли очень слабых кислот легко разлагаются при действии хлороводородной кислоты с выделением исходного алкина:
R-C = C-Cu + HCl → R-C = CH + CuCl.
Таким образом, используя реакции образования и разложения ацетиленидов, можно выделять алкины из смесей с другими углеводородами.
5. Полимеризация. В присутствии катализаторов алкины могут реагировать друг с другом, причем в зависимости от условий образуются различные продукты. Так, под действием водного раствора CuCl и NH4Cl ацетилен димеризуется, давая винилацетилен:
СН ≡ СН → СН2 = СН-С = СН
Винилацетилен обладает большой реакционной способностью; присоединяя хлороводород, он образует хлоропрен, используемый для получения искусственного каучука:
СН2 = СН-С = СН + HCl → СН2 = СН – ССl = СН2.
При пропускании ацетилена над активированным углем при 600 °С происходит тримеризация ацетилена с образованием бензола: ( реакция Зелинского ):
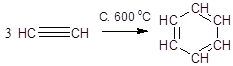
В аналогичные реакции тримеризации могут вступать также и ближайшие гомологи ацетилена, например: пропин тримеризуется в 1, 3, 5-триметилбензол.

6. Реакции окисления и восстановления. Алкины легко окисляются различными окислителями, в частности перманганатом калия, раствор перманганата калия обесцвечивается, что служит указанием на наличие тройной связи. При окислении происходит расщепление тройной связи, и образуются карбоновые кислоты:
R - C ≡ C-R' + 3[О] + Н2О → R - COOH + R' - COOH.
3CH≡ CH + KMnO4 +4H2O→ 3 HOOC-COOH +8MnO2 ↓ + 8KOH
В присутствии металлических катализаторов алкины восстанавливаются путем последовательного присоединения молекул водорода, превращаясь сначала в алкены, а затем в алканы:
| Н2 | Н2 | |||
| СН3 — С ≡ СН | → | СН3 — СН — СН2 | → | СН3 — СН2 — СН3. |
Применение. Ацетилен - основа органического синтеза, из него возможно получить уксусный альдегид, уксусную кислоту, бензол- вещества являющиеся сырьем фармацетического синтеза.
Составить конспект лекции и ответить на вопросы:
1. Дайте название алкена и составьте изомеры

2. Напишите реакцию получения ацетиленида бутина-1
3. Напишите реакцию гидратации бутина -2
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|