
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Задачи№№ 1, 2, 3, 7, 8, 9 стр. 33-37.
Задачи№№ 1, 2, 3, 7, 8, 9 стр. 33-37.
Тесты№№ 1 – 5 стр. 31, 32.
Решите задачи: Т. Н. Литвинова Т. Н. Сборник задач по общей химии. Задачи по общей химии с медико-биологической направленностью: учебное пособие для студентов медицинских вузов - 3-е изд., перераб. Гриф УМО МЗ и СР РФ//– М: ООО «Изд-во Оникс»: ООО «Издательство «Мир и образование», 2007 – 224 с. - (Высшее образование).
№1, 2, 5, 12, 15, 22 стр. 62-65. (можно любого издания)
1. Вычислите тепловой эффект реакции получения диэтилового эфира из этанола при с. у., пользуясь справочными значениями стандартных энтальпий образования веществ.
Ответ: Δ Нор-ции= –9, 2 кДж/моль.
2. Рассчитайте при с. у. тепловой эффект реакции спиртового брожения 54 г глюкозы: С6Н12О6(к) ® 2СО2(г) + 2С2Н5ОН(ж), исходя из стандартных энтальпий сгорания глюкозы и этанола.
Ответ: DНр-ции = –68 кДж/моль; Q = 20, 4 кДж.
3. В 100 г трески в среднем содержится 11, 6 г белков и 0, 3 г жиров. Рассчитайте (в кДж и ккал) энергию, которая выделится при усвоении порции трески массой 228 г. Калорийность белков17, 1 кДж/г, жиров 38, 8 кДж/г. Ответ: Q= 478, 8 кДж; Q= 114, 5 ккал.
4. Стандартная энтальпия растворения CuSO4 равна –66, 5 кДж/моль, стандартная энтальпия гидратации до пентагидрата равна –78, 22 кДж/моль. Вычислите стандартную теплоту растворения пентагидрата. Ответ: DНор-ния = 11, 72 кДж/моль.
5. Вычислите изменение энтропии (с. у. ) при протекании следующей реакции:
H2N–СН2–СООН(р-р) + H2N–СН2–СООН(р-р)®H2N-СН2–СО–NH–CH2–COOH(р-р)+Н2О(ж) Ответ: DS 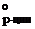 = –15, 8 Дж/(моль× K).
= –15, 8 Дж/(моль× K).
6. Возможна ли при с. у. биохимическая реакция гликолиза: С6Н12О6(aq)® 2C3H6O3(aq)?
Ответ: возможна, т. к. DG0р-ции = –161 кДж/моль.
Занятие № 5 (02. 10-06. 10)
Тема: «Основы химической кинетики. Катализ. Химическое равновесие. »
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|