
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Диссоциация солей в водных растворах
Диссоциация солей в водных растворах
NaCl Na+ + Cl-
Средние соли – это сложные вещества, при диссоциации которых в водных растворах образуются катионы металлов и анионы кислотных остатков.
CaCl2 ↔ Ca2+ + 2Cl-
NaCl Na+ + Cl-
Характерные свойства:
1. Кислый вкус кислот обусловлен наличием катиона H+
2. Мылкость растворов обеспечивает - анион OH-
3. Окраска раствора зависит от окраски ионов: Na+ К+ NO3- SO42- Cl- - бесцветные
Cu2+ голубой Cr2 O42- - желтый MnO42- - малиновый
Степень электролитической диссоциации
Отношение числа диссоциированных молекул к общему числу молекул, находящихся в растворе, называют степенью диссоциации.
Степень диссоциации (α – греческая буква альфа) - это отношение числа молекул, распавшихся на ионы (n), к общему числу растворенных молекул (N):
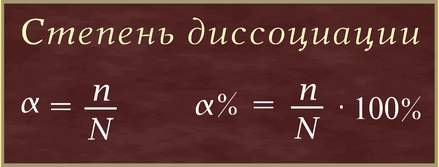
Решение задач.
1-я пара: Чему равна степень диссоциации электролита, если из каждых 300 его молекул на ионы распалось 50?
IV. Закрепление.
Самостоятельная работа учащихся (10 мин)
1. Определите на какие ионы диссоциируют следующие электролиты:
HCl, HBr, HNO3, NaOH, Ca(OH)2, KOH, NaCl, KNO3, Al2(SO4)3.
2. Напишите уравнения электролитической диссоциации следующих веществ:
А) H2SO4, HNO3
Б) KOH, Ca(OH)2
В) AgNO3, K3PO4, Na2SO4
По окончании работы взаимопроверка тетрадей и взаимооценивание, выставление окончательной оценки учителем.
Na2SO4 = 2Na+ + SO42-
V. Домашнее задание.
§7, 8 № 2 стр. 29, 1 любую задачу
Чему равна степень диссоциации электролита, если из каждых 350 его молекул на ионы распалось 70?
Чему равна степень диссоциации электролита, если из каждых 200 его молекул на ионы распалось 20?
Чему равна степень диссоциации электролита, если из каждых 600 его молекул на ионы распалось 60?
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|