
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
2. ТӘЖІРИБЕЛІК ҚОНДЫРҒЫНЫҢ СИПАТТАМАСЫ
Ө лшеу ү лкен шыны баллоннан Б, компрессордан Н жә не су манометрден Мтұ ратын қ ондырғ ыда (1 сур. ) жасалады. Баллон К краны арқ ылы компрессормен, К0 краны арқ ылы атмосферамен жалғ анғ ан.
Ұ сынылғ ан Клеман-Дезорм ә дісі (1819ж. ) бір кү йден екінші кү йге ө тетін екі тізбектелген процестермен, яғ ни адиабаталық жә не изохоралық процестермен жү ретін газдың параметрлерін зерттеуге негізделген. Бұ л процестер P-V диаграммасында 1-2 жә не 2-3 қ исық тарына сә йкес ұ сынылғ ан. Егер баллонғ а ауаны толтырып жә не сыртқ ы ортамен жылулық тепе-тең дік орнағ анша ұ стасақ, онда алғ ашқ ы кү йде газ P1, V1, T1 параметрлеріне ие болады. Бұ л кезде баллондағ ы газдың температурасы сыртқ ы ортаның температурасына тең, ал қ ысымы Р1=Р0+Р¢ атмосфералық қ ысымнан кішкене ү лкен болады. K0 кранды ашқ ан кезде баллондағ ы ауа 2-ші кү йге ө теді. Оның қ ысымы атмосфералық қ ысымғ а дейін P2=P0 тө мендейді. Ауаның 1 кү йдегі қ алғ ан массасы баллонның бір бө лік кө леміне ұ лғ ая отырып, барлық V2кө лемді алады.
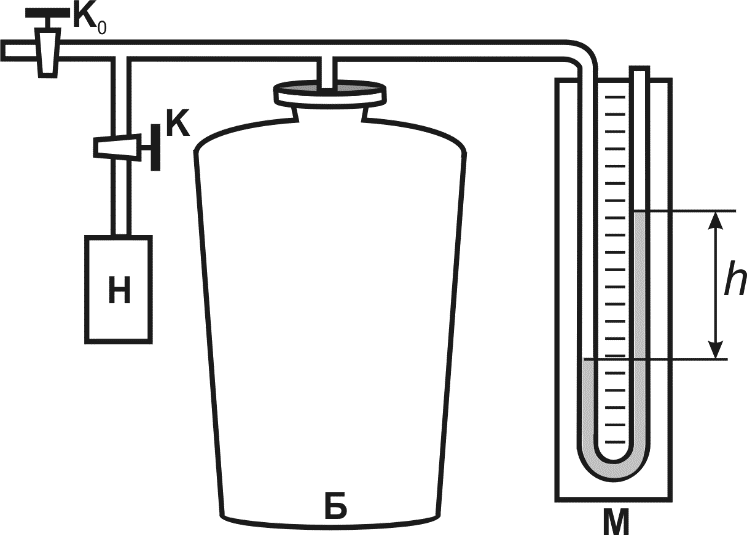 1 сурет.
1 сурет.
| 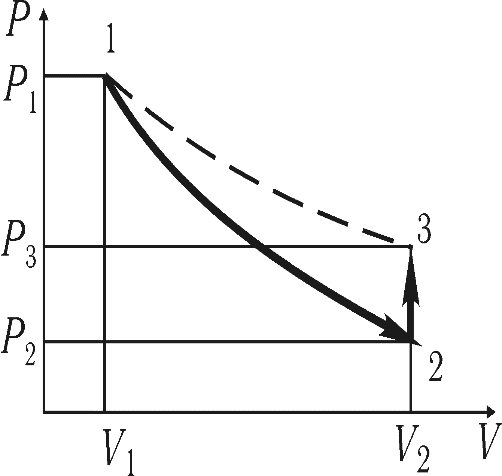 2 сурет.
2 сурет.
|
Бұ л кезде баллонда қ алғ ан ауа температурасы тө мендейді. Газдың тез ұ лғ аюы кезінде газдың баллон қ абырғ асы арқ ылы сыртқ ы ортамен жылу алмасуды ескермеуге болады. Онда 1-2 процесті адиабаталық деп есептейміз:
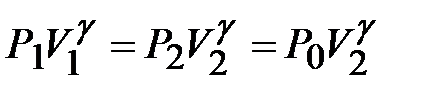 . (12)
. (12)
К0 кранды жапқ аннан кейін баллондағ ы адиабаталық ұ лғ айғ ан салқ ын ауа тұ рақ ты кө лем V2=V3кезде (2 сур. ) сыртқ ы ортаның температурасына T3=T1 дейін (2-3 процесс аралығ ында) қ ызады. Бұ л кезде баллондағ ы қ ысым Р3=Р2+Р¢ ¢ дейін артады.
Ауаның артық қ ысымдары Р' жә неР'' U -формалы манометрдегі тығ ыздығ ы r сұ йық тың дең гейлерінің айырымы бойынша ө лшенеді:
Р' = rgH; P'' = rgh, (13)
мұ ндағ ы Hжә неh -1 жә не 3 кү йлерге сә йкес манометрдің кө рсетуі.
Онда:
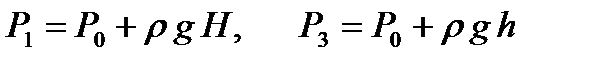 .
.
Ауаның 1 жә не 3 кү йлері изотермиялық процеске сә йкес келеді, сондық тан:
P1V1 = P3V3. (14)
(12)жә не (14) тең деулерден кө лемдердің қ атынасын қ ысымдардың қ атынасымен алмастырып, қ ысымдардың байланысын табамыз:
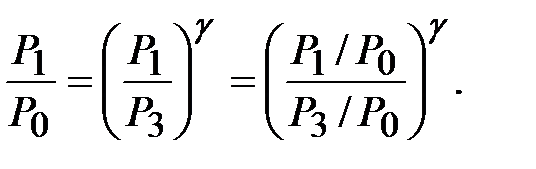
(13) ө рнекті ескеріпР1 жә не Р2 қ ысымдарды Р0 арқ ылы ө рнектеп жә не логарифмдейміз:

Егер х< < 1 болса, онда мына математикалық қ атынастан ln(1+х)=х, мұ ндағ ы x=ρ gHсол жақ тағ ы тең деуге тең шама, ал оң жақ тағ ы тең деу ү шін сә йкесінше x=ρ ghтең болады. Сонда:
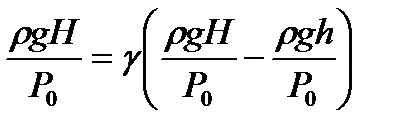 .
.
Осыдан адиабаталық кө рсеткіш γ есептейтін формуланы аламыз:
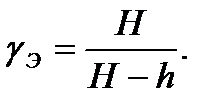 (15)
(15)
Сонымен, ауа ү шін жылу сыйымдылық тарының қ атынасын анық тау ү шін(1-2-3) процестерін алу қ ажет жә не газдың 1 жә не 3 кү йлеріне сә йкес манометрдің Н жә не һ кө рсетулерін ө лшеу керек. Бірақ бірқ алыпты адиабаттық процесті алу қ иын: егер газдың тез ұ лғ аюын жү ргізсек, онда процесс бірқ алыпты болмайды, ө йткені газдың температурасы мен қ ысымы кө лем бойынша тең есіп ү лгермейді. Баяу адиабаталық процесті жү ргізу ү шін баллонның жылулық изоляциясы қ ажет. Берілген қ ондырғ ыда t уақ ытта жылу шығ арылумен газ ұ лғ аяды. Сондық тан соң ғ ы изохоралық қ ызуда газдың қ ысымы аздап кө теріледі, яғ ни ө лшенетін һ '< һ адиабат кө сеткішін 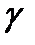 есептеу ү шін қ ажет. Уақ ыттың артуымен
есептеу ү шін қ ажет. Уақ ыттың артуымен 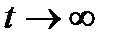 изотермиялық ұ лғ аю 1-3 газдың ұ лғ аюы кезіндегі һ ' мә ні тө мендей отырып нө лге ұ мтылады. Тә жірибелік жолмен тө мендегі тең деу анық талғ ан:
изотермиялық ұ лғ аю 1-3 газдың ұ лғ аюы кезіндегі һ ' мә ні тө мендей отырып нө лге ұ мтылады. Тә жірибелік жолмен тө мендегі тең деу анық талғ ан:
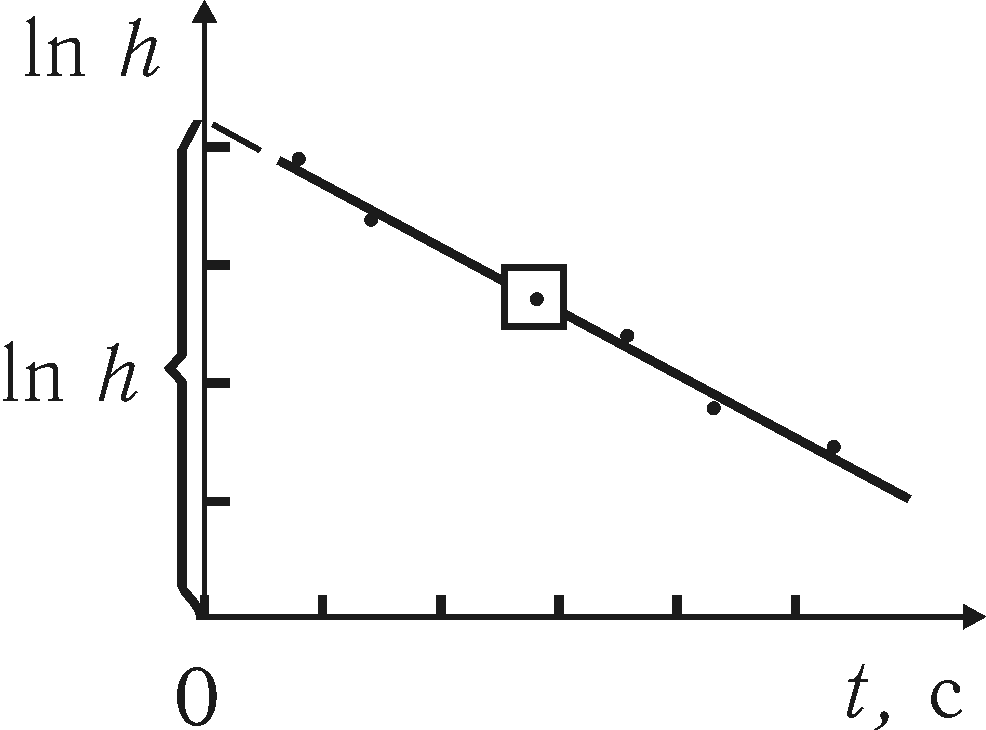 3 сурет.
3 сурет.
|
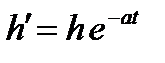 .
.
Бұ л ө рнекті логарифмдеп уақ ытқ а тә уелді функцияны аламыз:
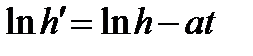 , (16)
, (16)
мұ ндағ ы а‒ қ ондырғ ы тұ рақ тысы; t ‒ процестің жү ру уақ ыты.
(16) тең деуі бойынша баллондағ ы ауаның соң ғ ы артық қ ысымының уақ ытқ а тә уелділігі3суретте кө рсетілген. Берілген тә жірибе бойынша график тұ рғ ызып, экстрополяция жолымен тә жірибелік тү зуді t=0 дейін соза отырып lnһ мә ні мен һ мә ні анық талады. һ мә нін анық тау (15) формула бойынша адиабаттық кө рсеткішті γ э есептеу ү шін қ ажет.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|