
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Е. тепе-теңдікке ұмтылу
$$$C
Су молекуласының ассоциация тү зү і тө мендегі қ асиеттермен тү сіндіріледі:
А. байланыстың қ анық пауы
B. ковалентті байланыстың тү зілуімен
C. сутектік байланыстың тү зілуімен
D. молекуланың полюстілігімен
Е. оттегінің электртерістілігімен
$$$C
Бас жә не орбиталь квант сандарының суммасы (n+l=5) беске тең болатын орбитальді кө рсет:
A. 3s
B. 3p
C. 3d
D. 4d
Е. 4f
$$$B
Ядросында 19 протоны жә не 20 нейтроны бар элементтің атомдық массасын анық та:
A. 19
B. 39
C. 20
D. 38
Е. 40
$$$D
Оттегі атомындағ ы орбитальдар санының суммамсы мынығ ан тең :
A. 2
B. 3
C. 4
D. 5
Е. 6
$$$A
Ионизациялану энергиясы ядро зарядының ө суімен элементтер қ атарында жоғ арыдан тө мен қ арай:
А. кемиді
B. артады
C. ө згермейді
D. негізгі қ атарларда артады
Е. заң дылық жоқ
$$$D
Электрондық аналогтар болатын элементтерді кө рсет:
A. N, P, S, CI
B. O, S, CI
C. S, CI, Ar
D. N, P, As
Е. O, S, N
$$$D
Байланысқ а атомдық орбитальін беретін атом тө мендегідей аталады:
A. катион
B. анион
C. донор
D. акцептор
Е. ион
$$$C
Ең тө мен энергиялы орбитальді кө рсет:
A. 3s
B. 3p
C. 2p
D. 3d
Е. 4s
$$$A
Екінші ретті периодтылық деп:
A. топшалардағ ы элементтер қ асиеттерінің монотонды емес ө згеруі
B. топшалардағ ы элементтер қ асиеттерінің монотонды ө згеруі
C. топтардағ ы металдық қ асиеттердің ө згеруі
D. топшалардағ ы бейметалдық қ асиеттердің ө згеруі
Е. бұ л тү сініктің мә ні жоқ
$$$A
Негізгі топшаларды қ ұ райтын элементтер:
А. s жә не р-элементтер
B. s жә не d-элементтер
C. s жә не f-элементтер
D. р жә не d-элементтер
Е. р жә не f-элементтер
$$$E
Химиялық байланыстың тү зілуі кезінде қ андай энергетикалық эффект орын алады:
А. энергия сің ірілуі
B. энергия ө згермейді
C. заң дылық жоқ
D. тек қ ана иондық байланыс тү зілуі кезінде
Е. энергия бө лінеді
$$$E
Тө мендегі байланыстардың қ андай типіне неғ ұ рлым жоғ ары энергия тә н:
А. ковалентті
B. ковалентті полюсті
C. ковалентті полюссіз
D. металлдық
Е. иондық
$$$B
Иондық байланыстың қ асиеттерін кө рсет (толық жауапты таң дау қ ажет):
1. қ анық қ андық, 2. бағ ытталғ андық, 3. қ анық пағ андық, 4. бағ ытталмағ андық, 5. полюстену.
A. 1, 2
B. 3, 4, 5
C. 4, 5
D. 1, 2, 5
Е. 1, 3, 5
$$$D
Қ озбағ ан кү йдегі атомнан электронды жұ лып алуғ а жұ мсалатын энергия тө мендегідей аталады:
A. электрон тартқ ыштық
B. электртерістілік
C. байланыс энергиясы
D. бірінші ионизациялану энергиясы
Е. электроң дылық
$$$B
Бір атомның электрон жұ бы жә не екінші бір атомның бос орбитальдарының ә рекеттесуі нә тижесінде тү зілетін химиялық байланыс тө менднгідеі аталады:
A. ковалентті полюсті
B. ковалентті байланыстың донорлық -акцепторлық механизмі
C. иондық
D. металлдық
Е. ковалентті полюссіз
$$$E
Қ осымша топшалар қ ұ рамына кіретін элементтер:
A. s-элементтер
B. р-элементтер
C. s- жә не р-элементтер
D. s- жә не d-элементтер
Е. d-элементтер
@@@ Химиялық процесстердің негізгі теориялары
$$$B
Қ оршағ ан ортамен энергиясымен жә не заттарымен алмасатын жү йе:
A. оқ шауланғ ан жү йе деп аталады
B. ашық жү йе деп аталады
C. жабық жү йе деп аталады
D. гомогенді жү йе деп аталады
E. гетерогенді жү йе деп аталады
$$$B
Тү зілу энтальпиясы нольге тең заттар:
A. НСІ, СО
B. О2, СІ2
C. СН4, СаО
D. РН3, КОН
E. НІ, Na2O
$$$D
Химиялық термодинамика нені зерттейді:
A. реакция ретін
B. реакция жылдамдығ ын
C. реакцияның молекулалығ ын
D. реакция энергиясының ө згеруін
E. қ айтымсыз реакцияларды
$$$B
Гиббс энергиясының ө згеруі қ ай формуламен есептеледі:
A. DG = T × DG
B. DG = DH - TDS
C. DG = T × DS - DH
D. DG = DH
E. DG = DH + DS
$$$A
Қ оршағ ан ортамен тек қ ана энергиясымен алмасатын жү йе:
A. жабық жү йе деп аталады
B. ашық жү йе деп аталады
C. оқ шауланғ ан жү йе деп аталады
D. гомогенді жү йе деп аталады
E. қ айтымды жү йе деп аталады
$$$B
Оқ шауланғ ан жү йелерде ө здігінен жү ретін процесстер мына бағ ытта жү реді:
A. энтропияның тө мендеуі
B. энтропияның жоғ арылауы
C. энтропияның нольге ұ мтылуы
D. энтропияның біртексіз ө згеруі
E. энтропияның ө згеруінде заң дылық жоқ
$$$B
Мынга реакцияғ а (аА + вВ = сС + дД) массалар ә сер заң ының математикалық тең деуі қ алай ө рнектелген:
A. Р = CRT
B. v = k CaA. CвВ
C. Dtзам = K. Cm
D. Dtкип = E. Cm
E. E = h v
$$$E
Температураны 200 (g =2) тө мендетсе, реакция жылдамдығ ы да тө мендейді:
A. 2 есе
B. 6 есе
C. 8 есе
D. 16 есе
E. 4 есе
$$$D
Мына реакция (Н2+СІ2 =2НСІ) жү ретін жү йеде қ ысымды 2 есеге арттырғ ан. Реакция жылдамдығ ы неше есе артады:
A. 3 есе
B. 6 есе
C. 8 есе
D. 4 есе
E. 27 есе
$$$B
Тепе-тең дік константасын қ ай формуламен есептейді:
A. К = kпр. + kобр.
B. K = kпр. /kобр.
C. K = kпр. × kобр.
D. K = kпр. – kобр.
E. K = kобр.
$$$A
Мына реакцияда (N2+3H2 = 2NH3) қ ысымның тө мендеуіне байланысты реакция тепе-тең дігі қ ай жақ қ а ығ ысады:
A. солғ а
B. оң ғ а
C. ешқ айда ығ ыспайды
D. заң дылық жоқ
E. тепе-тең дік орнамайды.
$$$E
Реакция жылдамдығ ына ә сер етпейтін фактор:
A. концентрация
B. температура
C. катализатор
D. ә рекеттесетін заттар табиғ аты
E. кө лем
$$$D
Температураны 300 жоғ арылатқ анда реакция жылдамдығ ы 8 есе артты. Температуралық коэффициентті есепте:
A. 9
B. 8
C. 6
D. 2
E. 1
$$$D
Мына реакцияда (N2+3H2 = 2NH3+ 92, 0 кДж, ) тепе-тең дікті аммиак тү зілу жағ ына қ арай ығ ыстыру ү шін не істеу керек:
A. қ ысыммен температураны тө мендету керек
B. қ ысымды тө мендетіп, ал температураны жоғ арылату керек
C. қ ысымды да, температураны да жоғ арылату керек
D. қ ысымды жоғ арылатып, ал температураны тө мендету керек
E. сутегінің корнцентрациясын тө мендету керек
$$$E
Мына реакцияда (2NOг. +O2 г. = 2NOг. ) қ ысымның 2 есе жоғ арылауымен байланысты реакция жылдамдығ ы:
A. 6 есе артада
B. 6 есе кемиді
C. 8 есе артады
D. 16 есе кемиді
E. 27 есе артады.
$$$D
Қ ай жағ дайда тепе-тең дік орнайды:
A. vпр. = vобр. DG < O
B. vпр. > vобр. DG = O
C. vпр. < vобр. DG > O
D. vпр. = vобр. DG = O
E. vпр. = vобр. DH > O
$$$C
Гомогенді реакцияның жылдамдық константасы осы реакцияның сандық мә ніне қ андай жағ дайда тең болады:
A. егер ә ректтесуші заттар концентрациясы нө льге тең болса
B. катализатора қ атысында
C. егер ә рекеттесуші заттар концентрациясы 1 моль/л тең болса
D. егер t = 2980 K
E. егер Еакт. = 1.
$$$A
Температураны ә рбір 100 кө терген сайын, Вант-Гофф ережесі бойынша реакция жылдамдығ ы неше есе артады:
A. 2-4 есе
B. 15-18 есе
C. 12-14 есе
D. 5-7 есе
E. 2-8 есе
$$$D
Жү йедегі температураны (g =2 ) 200 –тан 400-қ а дейін кө терді, реакция жылдамдығ ы неше есе артты:
A. 32 есе
B. 16 есе
C. 12 есе
D. 4 есе
E. 2 есе
$$$C
Мү мкін болатын термодинамикалық реакцияның жылдамдығ ын ө згертіп, ал бірақ ө здері реакция барысында ө згеріссіз қ алатын заттар:
A. индикаторлар деп аталады
B. регуляторлар деп аталады
C. катализаторлар деп аталады
D. промоторлар деп аталады
E. константалар деп аталады
$$$E
Тепе-тең дік жағ дайда тұ рғ ан жү йеге қ андай да бір жағ даймен ә сер етсе ( мысалы t, Р, C-ны ө згертсе), онда тепе-тең дік осы ә серді ә лсірететін бағ ытқ а қ арай ығ ысады. Бұ л заң:
A. массалар ә сер заң ы
B. зат массасының сақ талу заң ы
C. энергия сақ талу заң ы
D. Гесс заң ы
E. Ле-Шателье принципі
$$$B
Химиялық реакция нә тижесінде бө лінетін немесе сің ірілетін жылу:
A. жү йенің ішкі энергиясы деп аталады
B. реакцияның жылу эффектісі деп аталады
C. жү йенің энтропиясы деп аталады
D. Гиббс энергиясы деп аталады
E. жуйенің кинетикалық энергиясы деп аталады
$$$E
Жү йенің энтальпиясы арта жү ретін химиялық реакциялар қ алай аталады:
A. нейтралдай реакциясы
B. алмасу реакциясы
C. тотығ у-тотық сыздану реакциясы
D. экзотермиялық реакциялар
E. эндотермиялық реакциялар
$$$D
Қ оршағ ан ортамен энергиясымен жә не затымен ауысатын жү йе тө мендегідей аталады:
А. гомогенді
B. жекеленген
C. гетерогенді
D. ашық
Е. тұ йық
$$$D
Химиялық реакциы жылдамдығ ы немен анық талады:
A. ә рекеттесетін заттардың моль санымен
B. бө лшектердің соқ тығ ысу санымен
C. бө лшектердің активті соқ тығ ысу санымен
D. бір кө лемде бір уақ ыт ішінде реакцияғ а қ атысатын заттардың моль с. нымен
Е. реакция ө німінің моль санымен
$$$E
Тө мендегі комплексті иондардың ішіндегі неғ ұ рлым тұ рақ тысы:
A. [Zn(NH3)4]2+ Кнест=4*10-14
B. [Ag(NH3)2]+ Кнест=6, 3*10-18
C. [Zn(CN)4]2- Кнест=1*10-16
D. [Ag(CN)2]- Кнест=6, 8*10-8
Е. [PtCl4]2- Кнест=6, 4*10-24
$$$C
К4[Fе (CN)6] қ осылысындағ ы комплекстү зушінің тотығ у дә режесі:
A. 4+
B. 6+
C. 2+
D. 3+
Е. 1+
$$$B
Вант-Гофф заң ы бойынша осмостық қ ысым тө мендегіге тура пропорционал:
А. зат эквивалентіне
B. молярлы концентрацияғ а жә не температурағ а
C. электрө ткізгіштікке
D. процентті концентрацияғ а
Е. иондар қ озғ алғ ыштығ ына жә не температурағ а
$$$C
Сутегі ионының концентрациясы [Н+]=10-3 моль/л. рОН нешеге тең?
A. 3
B. 6
C. 11
D. 7
Е. 2, 7
$$$A
Na3PO4 тұ зы ерітіндісінің реакция ортасы қ андай:
А. сілтілік
B. қ ышқ ылдық
C. нейтрал
D. ә лсіз-қ ышқ ылдық
Е. кү шті қ ышқ ылдық
$$$D
HNO2 диссоциациясы константасының дұ рыс тең деуі:
D. 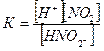
$$$C
Тотық сыздандырғ ыштың реакцияда жоғ алтатын электрон санын анық та:
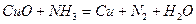 :
:
A. 1
B. 2
C. 3
D. 4
Е. 5
$$$D
Mn2O7 қ осылысындағ ы марганецтің тотығ у дә режесін анық та:
A. +5
B. +3
C. +2
D. +7
Е. +1
$$$D
Ішкі энергия, энтальпия, энтропия, температура нені білдіреді:
А. энергетикалық сипаттамалар
B. ауыспалы қ асиеттер
C. заттардың тұ рақ ты қ асиеттері
D. кү й функциясы
Е. жекеленген жү йені сипаттайтын шамалар
$$$A
Реакцияның молекулярлығ ы деп нені атайды:
А. реакцияның элементарлы актіне қ атысатын молекулалар саны
B. реакция нә тижесінде тү зілген молекулалар саны
C. соқ тығ ысқ ан молекулалар саны
D. ә рекеттесуші заттар жә не реакция ө німі молекулаларының санының суммасы
Е. бұ л реакция тә ртібі
$$$B
[Cu (NH3)4]SO4 қ осылысындағ ы комплекстү зушінің тотығ у дә режесін анық та:
A. +3
B. +2
C. +4
D. +6
Е. +8
$$$B
Координациялық сан тө мендегіні кө рсетеді:
А. лиганд зарядын
B. лиганд санын
C. комплекстү зуші санын
D. комплекстү зуші зарядын
Е. комлекстү зуші дә режесін
$$$A
Дихлортетрамминкобальт (III) хлоридінің формуласын кө рсет:
A. [Со (NH3)4Cl2]Cl
B. [Со (NH3)3Cl3]
C. [Со (NH3)5Cl]Cl2
D. [Со (NH3)2Cl4]Cl2
Е. [Со (NH3)4Cl4]Cl
$$$B
Криоскопиялық жә не эбулиоскопиялық константалар темендегіге тә уелді:
A. температурағ а
B. еріткіш табиғ атына
C. еріген зат табиғ атына
D. температура жә не концентрацияғ а
Е. еріген зат жә не ерітінді табиғ атына
$$$D
Тү зілу энтальпиясының стандартты мә ніне сү йене отырып, неғ ұ рлым тұ рақ ты қ осылысты кө рсет:
A. D Н0AgCl=-127, 1 кДж/моль
B. D Н0Н2О=- -285, 8 кДж/моль
C. D Н0НCl=-92, 3 кДж/моль
D. D Н0AL2O3=-1676 кДж/моль
Е. D Н0Al=-0 кДж/моль
$$$C
Химиялық тепе-тең діктің ығ ысуына не ә сер етпейді:
A. зат концентрациясы
B. температура
C. катализатор
D. қ ысым
Е. қ ысым жә не концентрация
$$$C
Химиялық реакция жылдамдығ ы неге тә уелсіз:
A. концентрацияғ а
B. температурағ а
C. катализаторғ а
D. рітінді кө леміне
Е. ә рекеттесуші заттар табиғ атына
$$$C
Тұ рақ ты температурадағ ы қ айтымсыз процесстер ү шін термодинамиканың ІІ заң ының математикалық тең деуін кө рсет:
A. 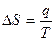
B. 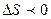
C. 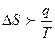
D. 
Е. 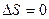
$$$C
Катализді қ ай жағ дайда гомогенді деп атайды:
A. ә рекеттесуші заттар жә не катализатор - газдар
B. ә рекеттесуші заттар жә не катализатор - сұ йық тық тар
C. ә рекеттесуші заттар жә не катализатор бір фазада
D. ә рекеттесуші заттар жә не катализатор ә ртү рлі фазада
Е. катализатор қ атты зат
$$$C
[Со (NH3)5SO4]Br- қ осылысындағ ы комплекстү зушінің тотығ у дә режесін кө рсет:
A. 0
B. 12
C. +3
D. +4
Е. +6
$$$B
Na3[Со (NO2)6] қ осылысындағ ы лигандамен комплекстү зуші иондарының арасындағ ы химиялық байланыстың табиғ аты:
А. иондық
B. донорлық -акцепторлық
C. металлдық
D. сутектік
Е. ковалентті полюсті
$$$A
450г суда 50 г тұ зды ерітті. Тұ здың ерітіндідегі массалық ү лесін (%) анық таң дар:
A. 10%
B. 5%
C. 50%
D. 1%
Е. 2%
$$$C
Қ анық пағ ан ерітінді деп:
A. еріткішке қ арағ анда, еріген зат мө лшері азарақ ерітінді
B. қ анық қ ан ерітіндіге қ арағ анда, еріген зат мө лшері кө бірек ерітінді
C. қ анық қ ан ерітіндіге қ арағ анда, еріген зат мө лшері азырақ ерітінді
D. еріткіш пен еріген зат мө лшері бірдей ерітінді
Е. концентрленген
$$$E
Қ ай заттың ерітіндісі бірдей концентрацияда неғ ұ рлым жоғ ары рН мә нін кө рсетеді:
A. HCl
B. CH3COOH
C. NaCl
D. NH4OH
Е. NaOH
$$$C
Бренстед теориясы бойынша негіз деп тө мендегіні атайды:
A. протон доноры
B. сутек атомының доноры
C. акцептор
D. гидроксил акцепторы
Е. протон доноры, гидроксил акцепторы
$$$C
Қ ай еріткіште заттардың электролиттік диссоциация орын алады:
А. СН3СООН (e=6, 2)
B. НСООН (e=5, 3)
C. Н2О (e=78)
D. С6Н6 (e=2, 3)
Е. СНСl3 (e=5, 1)
$$$E
HIO4 иод қ ышқ ылында иодтың тотығ у дә режесі нешеге тең:
A. +5
B. +6
C. +8
D. +3
Е. +7
$$$B
НСlО3 мына қ осылыстағ ы хлордың тотығ у дә режесін кө рсет:
A. +4
B. +5
C. +6
D. +2
Е. +7
$$$D
Таза еріткішпен салыстырғ анда ерітіндінің қ айнау температурасының артуы, қ ату температурасының азаюы тө мендегіге тура пропорционал:
A. қ ысымғ а
B. нормальді концентрацияғ а
C. еріткіштің диэлектрлік ө ткізгіштігіне
D. ерітіндінің моляльді концентрациясына
Е. процентті концентрацияғ а
$$$E
NH4[Сr (CNS)4 (NH3)2] мына қ осылыстағ ы лигандты кө рсет:
A. NH4+
B. Cr+3
C. Cr3+, NH3
D. NH4+, CNS-
Е. CNS-, NH3
$$$C
Нейтрал ортадағ ы сутек иондарының концентрациясы тө мендегіге тең:
A. 7*10-7
B. 14
C. 1*10-7
D. 7
Е. 10-14моль/л
$$$C
Na3РО4 тұ зының гидролизі кезінде тү зілетін заттарды кө рсет:
A. Н3РО4 жә не NаОН
B. NаН2РО4 жә не NаОН
C. Nа2НРО4 жә не NаОН
D. Nа2НРО4 жә не NаН2РО4
Е. Н3РО4 жә не Nа2НРО4
$$$C
ТТР нә тижесінде тө мендегі иондардың тотығ у дә режесі артады:
As2S3 + HNO3+ H2O ® H3AsO4 + H2SO4 + NO
A. N+5, O-2
B. N+5, S-2
C. As+3, S+2
D. As+3, O-2
Е. N+5, As+3
$$$B
Жекеленген жү йедегі процесстер тө мендегі бағ ыт бойынша ө здігінен жү ре бастайды (термодинамиканың ІІ заң ы):
A. энтропияның кемуі
B. энтропияның артуы
C. энтропия нө лге тең
D. энтропи ү немі ө згеріп отырады
Е. энтропияның біртіндеп кемуі
$$$E
Мына процессте хлор шығ ымын қ алай кө бейтуге болады:
4НСl(г) + О2 (г) Û 2Сl2 (г) + 2Н2О(г)
A. оттегі концентрациясын кеміту
B. температураны арттыру
C. қ ысымды азайту
D. қ ысымды азайту жә не температураны арттыру
Е. қ ысымды арттыру
$$$D
Реакция жылдамдығ ының константасы тө мендегіге тә уелді:
A. концентрацияғ а
B. концентрацияғ а, температурағ а
C. концентрацияғ а жә не реагенттер табиғ атына
D. температурағ а, ә рекеттесуші заттар табиғ атына
Е. еріткіш табиғ атына
$$$B
200 мл 0, 1М ерітіндідегі кү кіт қ ышқ ылының қ ұ рамы тө мендегідей (граммен):
A. 1, 5г
B. 1, 96г
C. 2, 5г
D. 9, 8г
Е. 4, 5г
$$$E
Ерітінділеге дә л анық тама берің дер:
A. еріген зат жә не еріткіштен тұ ратын жү йе
B. гомогенді жү йе
C. гетерогенді жү йе
D. еріген заты бар жү йе
Е. екі немесе оданда кө п компоненттері бар жә не олардың ә рекеттесуі нә тижесінде тү зілген ө німдері бар, гомогенді жү йе
$$$B
Ә лсіз электролит ерітіндісіне аттас иондарды енгізген кезде, диссоциации дә режесі:
A. артады
B. кемиді
C. артады, сосын кемиді
D. ө згермейді
Е. заң дылық жоқ
$$$B
Оствальдтың сұ йылту заң ы:
A. 
B. 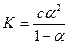
C. 
D. 
Е. С=kp
$$$A
Гидролиз константасы тө мендегіден тә уелсіз:
A. тұ з концентрациясынан
B. температурадан
C. тұ з табиғ атынан
D. тұ з табиғ атынан жә не температурадан
Е. температура артуынан
$$$B
Тотық сыздану процессі деп:
A. атомдардын электрондарын беруі
B. атомдар мен иондардың электрондарды қ осып алуы
C. тотығ у дә режесінің ө згеруі
D. атомның тотығ у дә режесінің артуы
Е. молекула тү зілуі
$$$E
ТТР тө мендегі реакциялардың қ айсысы жатады:
A. HCl + NaOH = NaCl + H2O
B. CaCO3 ® CaO + CO2
C. FeO + SO3 = FeSO4
D. ZnO + H2SO4 = ZnSO4 + H2O
Е. Cr2O3 + Mn2O7= CrO3 + MnO
$$$D
[PtCl (NH3)5]Cl3 мына комплексті қ осылыс қ айсысына жатады:
A. анионды
B. нейтралды
C. аквакомплекс
D. катионды
Е. циклді
$$$B
2л 0, 1н Н3РО4 ерітіндісінде қ анша фосфор қ ышқ ылы бар:
A. 3, 26г
B. 6, 54г
C. 32, 6г
D. 65, 0г
Е. 16, 3г
$$$C
Осмостық қ ысым қ андай факторларғ а тә уелді:
A. ерітінді концентрациясына
B. температурағ а
C. ерітінді концентрациясына, температурағ а
D. еріген зат табиғ атына
Е. ерітінді концентрациясына, еріген зат табиғ атына
$$$D
Концентрациясы 0, 01 моль/л болатын натрий хлориді ерітіндісінің иондық кү ші тө мендегіге тең:
A. 0, 02
B. 0, 05
C. 0, 04
D. 0, 01
Е. 0, 005
$$$C
Диссоциация константасының мә ні бойынша ең ә лсіз электролитті кө рсет:
A. КHF=6, 6*10-4
B. КCH3COOH=1, 8*10-5
C. КHCN=7, 9*10-10
D. КHCOOH=1, 8*10-4
Е. КHNO2= 4*10-4
$$$E
Сутек иондарының концентрациясы 10-4 моль/л. Ерітіндінің рН-ын анық та:
A. 6
B. 8
C. 10
D. 2
Е. 4
$$$A
Жартылайө ткізгіш мембрана арқ ылы еріткіш молекулаларының біржақ ты диффузиясы тө мендегідей аталады:
A. осмос
B. сұ йылту
C. ерітіндіні концентрлеу
D. Доннан эффектісі
Е. тепе-тең дікке ұ мтылу
$$$D
Кальций фосфаты, кальций оксиді, фосфорлы ангидрид қ осылыстарының тү зілу жылуы DН0298 осығ ан сә йкес: -4137, 5 кДж/моль, -635, 5 кДж/моль, -1492 кДж/моль. Реакцияның жылу эффектісін есепте:
3 СаО(к) + Р2О5(к) = Са3(РО4)2 (к)
A. –3502кДж
B. –2127кДж
C. –2010, 5кДж
D. –739кДж
Е. +739кДж
$$$C
Егер температураны 300С –қ а кө тергенде, реакция жылдамдығ ы 27 есе артқ ан, реакцияның температуралық коэффициентін анық та:
A. 9
B. 2
C. 3
D. 2, 7
Е. 2, 2
$$$A
0, 5М сахароза ерітіндісінің осмостық қ ысымы 270С (R=0, 082) градуста тө мендегі мә нге тең:
A. 12, 3 атм
B. 1, 23 атм
C. 8, 2 атм
D. 1, 5 атм
Е. 16, 4 атм
$$$A
Моляльді концентрация тө мендегі мә ндермен анық талады:
A. 100 г ерітіндідегі заттардың грамм санымен
B. 1 л ерітіндідегі заттардың моль санымен
C. 1 л ерітіндідегі заттардың грамм санымен
D. 1 л ерітіндідегі моль-эквиваленттер санымен
Е. 1 кг еріткіштегі заттардың моль санымен
$$$B
Реакцияның температуралық коэффициенті тө мендегі мә ндерді қ абылдай алады:
A. 10-нан 100-ге дейін
B. 2-ден 4-ке дейін
C. 2-ден 10-ғ а дейін
D. 0-ден 4-ке дейін
Е. 0-ден 10-ғ а дейін
$$$C
Катализатор тө мендегілердің қ айсысына ә сер етпейді:
A. реакция жылдамдығ ына
B. реакция энергиясының активациясына
C. реакцияның жылу эффектісіне
D. ә рекеттесуші заттар концентрациясына
Е. кері реакция жылдамдығ ына
$$$A
NH4Cl тұ зының гидролизі кезіндегі реакция ортасын кө рсет:
A. рН< 7
B. рН> 7
C. рН=7
D. рН=10
Е. рН> 8
$$$C
Тө мендегі заттардың қ асысы жағ дайғ а тә уелді тотық тырғ ыштың да, тотық сыздандырғ ыштың да қ асиетін кө рсете алады:
1)KNO3 2) H2SO4 3) HClO2 4) KNO2
A. 1, 2, 3
B. 1, 4
C. 3, 4
D. 1, 2, 4
Е. 2, 3, 4
$$$D
Сутек иондарының концентрациясы 1*10-5М. Ерітіндінің рН-ын анық та:
A. 0, 1
B. 7
C. 9
D. 5
Е. 2, 8
$$$B
Кү й функциясына тә н қ асиеттер:
A. ауыспалы мә н
B. ө згеріс ө ту жолына тә уелсіз
C. жағ дайғ а тә уелді белгілі бір мә н
D. ө згеріс уақ ыт ішінде ү здіксіз
Е. тұ рақ ты мә н
$$$E
Қ ысымды 2 есе арттырғ анда тура реакция жылдамдығ ы 2СО(Г)=СО2(Г)+С(ТВ) тө мендегідей ө згереді:
A. 2 есе артады
B. 3 есе артады
C. 4 есе азаяды
D. 6 есе артады
Е. 4 есе артады
$$$B
Гидролизге ұ шырайтын тұ здарды кө рсет:
A. NaNO3, K2SO4
B. AlCl3, Na2S
C. KCl
D. NaCl
Е. NaCl, BaCl2
$$$E
200 мл ерітіндіде 4 г натрий гидроксиді бар. Ерітіндінің молярлы концентрациясын тап:
A. 0, 1М
B. 0, 2 М
C. 0, 3 М
D. 0, 4 М
Е. 0, 5 М
$$$D
Молекуланың немесе ионның активтілігі деп:
A. ион немесе молекула энергиясы
B. олардың концентрациясы
C. реакцияғ а қ атыса алу қ абілеті
D. олардың химиялық реакцияда соғ ан сә йкес ә сер ететін концентрациясы
Е. заттар концентрациясы
$$$B
Гиббстің еркін энергиясы тө мендегі қ атынаспен анық талады:
A. H=U+PV
B. G=H-TS
B. H=q
D. S= 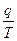
Е. S> 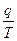
$$$A
Тұ рақ ты қ ысымда, химиялық реакцияларда сің ірілетін немесе бө лінетін жйлу ө лшемі қ алай аталады:
A. энтальпия
B. энтропия
C. Гиббстің еркін энергиясы
D. потенциал
Е. энергия
$$$C
Электродта тү зілген зат массасы, ө ткізілген электр мө лшеріне пропорционал:
A. Генри заң ы
B. Рауль заң ы
C. Фарадейдің І-ші заң ы
D. Вант-Гофф заң ы
Е. Оствальд заң ы
@@@ Электролит ерітінділердегі иондық тепе-тең дік
$$$C
300 г, 5 %-ті ерітіндідегі зат массасы:
A. 5 г.
B. 10 г.
C. 15 г.
D. 20 г.
E. 30 г.
$$$B
1литрінде 6, 3 г. азот қ ышқ ылы бар ерпітіндінің молярлы концентрациясы:
A. 0, 5
B. 0, 1
C. 0, 3
D. 0, 2
E. 0, 01
$$$C
500 мл, 0, 01н. кү кірт қ ышқ ылының ерітіндісін даярлау ү шін қ ажет массасы:
A. 0, 546 г.
B. 0, 214 г.
C. 0, 245 г.
D. 0, 235 г.
E. 0, 045 г.
$$$C
Ерітінді бетіндегі еріткіштің қ анық қ ан буының салыстырмалы тө мендеуі қ андай шамағ а тең:
A. ерітіндінің молярлы концентрациясына
B. нормальді концентрациясына
C. мольдік есесіне
D. процентті концентрациясына
E. титріне
$$$D
Келтірілген дисперсті жү йелердің қ айсысын ерітіндіге жатқ ызуғ а болады:
A. аэрозоль
B. тү тін
C. тұ ман
D. таза ауа
E. шаң ды ауа
$$$C
Мына заттардың қ айсысы электролит:
A. С10Н8
B. С6Н12О6
C. НСІ
D. С3Н8О3
Е. С12Н22О11
$$$E
0, 1 М СаСІ2 ерітіндісінің иондық кү ші:
A. 0, 6
B. 0, 5
C. 0, 4
D. 0, 2
E. 0, 3
$$$D
Электролиттік диссоциация дегеніміз электролит молекуласының, қ ай фактор ә серінен иондарғ а ыдырау процессі:
A. электр тоғ ының
B. иондар энергиясының
C. қ ыздырудың
D. еріткіштің полюсті молекулаларының
E. сұ йылту
$$$B
Ә лсіз электролиттер диссоциациясының константасы қ ай факторғ а тә уелсіз:
A. температурағ а
B. концентрацияғ а
C. еріткіш табиғ атына
D. еріген зат табиғ атына
E. еріген зат жә не еріткіш табиғ атына
$$$C
Қ ай зат кү шті электролит:
A. НҒ
B. Н3РО4
C. НСІ
D. Н2СО3
E. НNO3
$$$A
Қ ай зат ә лсіз электролит:
A. НNO2
B. НNO3
C. NaOH
D. CaCl2
E. HCl
$$$C
Мына реакцияның Ғ е(ОН)3+НСІ =Ғ е(ОН)2СІ + Н2О қ ысқ артылғ ан иондық тең деуін кө рсет:
A. Ғ е+3+3(ОН)- + Н+ = Ғ е(ОН)2+ + Н2О
B. Ғ е+3+2(ОН)- = Ғ е(ОН)2+
C. Ғ е(ОН)3 + Н+ = Ғ е(ОН)2+ + Н2О
D. Н++ОН-= Н2О
E. Ғ е(ОН)3 + Н+ = Ғ е(ОН)2+
$$$D
Концентрация [Н+]= 10-5моль/л тең. рОН мә нін тап:
A. 5
B. 8
C. 10
D. 9
E. 14
$$$B
Ерітінді рН-ы 8-ге тең. Гидроксид- иондарының концентрациясын анық та:
A. 6
B. 10-6
C. 8
D. 10-8
E. 10-14
$$$A
Қ ай зат еғ рітіндісі нейтрал ортаны кө рсетеді:
A. NaCl
B. NaOH
C. NH4OH
D. CH3COOH
E. HCl
$$$E
Қ ай зат сатылы гидролизге тү седі:
A. СН3СООН
B. NH4NO3
C. KNO2
D. CH3COONH4
E. AlCl3
$$$E
Қ ай тұ з гидролизге тү спейді:
A. NH4NO3
B. AlCl3
C. Na2CO3
D. BaCl2
E. KCl
$$$E
Ерітіндісінің рН-шы »7 тең болатын тұ зды кө рсет:
A. К3РО4
B. АІСІ3
C. ZnCl2
D. K2CO3
E. NaCl
$$$B
Қ айтымсыз гидролизге тү сетін тұ зды кө рсет:
A. К2СО3
B. Ғ е2(СО3)3
C. NH4Cl
D. NaCN
E. NH4NO3
$$$C
Cілтілік ортаны тү зе жү ретін тұ зды кө рсет:
A. NH4Cl
B. KCl
C. K2CO3
D. NaNO3
E. Ca(NO3)2
$$$C
Нейтрал ортадағ ы сутегі иондарының концентрациясы:
A. 7× 10-7
B. 14
C. 10-7
D. 7
E. 10-1
$$$A
Тек А1С13 тұ зының гидролизі кезінде тү зілетін иондар:
A. А1ОН+2, Н+, С1-
B. А1(ОН)2+, А1+3, С1-
C. А1+3, ОН-, С1-
D. А1(ОН)3, Н+, С1-
E. А1+3, Н+, С1-
$$$D
Неғ ұ рлым жоғ ары дә режеде гидролизденетін қ осылысты кө рсет:
A. К2СО3
B. NH4Cl
C. NaNO2
D. Al2S3
E. Li2SO3
@@@ Тотығ у-тотық сыздану реакциялары (ТТР)
$$$C
Калий дихроматындағ ы калийдің тотығ у дә режесін кө рсет:
A. +4
B. +5
C. +6
D. +3
E. +2
$$$D
КС1О4 қ осылысы бос хлорғ а дейін тотық сызданатын болса, осы тұ здың эквиваленттік массасын тап:
A. 138, 5 г/моль
B. 109, 8 г/моль
C. 27, 7 г/моль
D. 19, 8 г/моль
E. 69, 3 г/моль
$$$B
Марганецтің қ ай қ осылысы тек қ ана тотық сыздантырғ ыштық касиет кө рсетеді:
A. КМnO4
B. MnCl2
C. MnO2
D. HМnO4
E. H2MnO4
$$$A
Қ ай қ осылыста марганецтің тотығ у дә режесі 6-ғ а тең:
A. К2МnO4
B. MnO2
C. MnO
D. KMnO4
E. HMnO4
$$$D
Тотығ у процессін кө рсет:
A. С+4®С0
B. MnO4-®MnO4-3
C. 2H+®H20
D. NH4+®N20
E. NO3-®NO
$$$B
Мына (С12+Н2S+H2O®HCl+H2SO4) ТТР-ның коэффициенттерінің суммасы:
A. 20
B. 28
C. 18
D. 8
E. 5
$$$E
Тотығ у дә режесі дегеніміз:
A. молекуладағ ы атомдар зарядының суммасы
B. атомдағ ы электрондар саны
C. валенттілік
D. ядро запряды
E. молекуладағ ы атомдардың заряды
$$$B
Мына (2НВr+H2SO4=Br2+SO2+2H2 O)ТТР-на қ атысқ ан кү кірт қ ышқ ылының эквиваленттік массасы:
A. 98 г/моль
B. 49 г/моль
C. 4, 9 г/моль
D. 41, 9 г/моль
E. 12, 3 г/моль
$$$D
МnO2-нің Mn+2-ге дейін тотық сызданғ андағ ы эквивалентін тап:
A. 55, 0
B. 45, 5
C. 71, 0
D. 43, 5
E. 158, 0
$$$A
РО3-3-ионындағ ы фосфордың тотығ у дә режесін кө рсет:
A. +3
B. +5
C. 0
D. -3
E. -2
$$$A
Диспропорционирлену (молекула ішілік ТТР) реакциясын кө рсет:
A. КС1О3 ®КС1О4+ КС1
B. НС1+О2®С12+Н2О
C. КС1О3®КС1+О2
D. НNO3®NO2+H2O+O2
E. Cu+HNO3®Cu(NO3)2+NO+H2O
$$$C
Мына реакцияғ а (HNO3+S®H2SO4+NO) қ атысқ ан кү кірттің эквивалентін тап:
A. 32
B. 16
C. 5, 3
D. 8
E. 4, 3
$$$B
Тотығ у-тотық сыздану реакциясы дегеніміз:
A. нейтралдау реакциясы
B. ә рекеттесуі заттардың тотығ у дә режесі ө згере жү ретін реакциялар
C. катализатор қ атысында жү ретін реакциялар
D. жылу эффектісі ө згере жү ретін реакциялар
E. алмасу реакциялары
$$$C
Тотық тырғ ышты кө рсет:
A. Na
B. Al
C. O2
D. K
E. Li
$$$A
Тотық сыздандырғ ышты кө рсет:
A. Mg
B. O2
C. F2
D. S
E. Cl2
@@@ Электрохимиялық процесстер.
$$$D
Стандартты сутекті электродтың потенциалын кө рсет (В):
A. 1, 66
B. 1, 36
C. –0, 76
D. 0
E. 1, 4
$$$B
Гальваникалық элементте жү ретін реакциялар:
A. алмасу реакциясы
B. тотығ у-тотық сыздану реакциясы
C. нейтралдау реакциясы
D. қ айтымды реакциялар
E. диссоциация
$$$E
Ионының концентрациясы қ ай шамағ а тең болғ анда, металдың электродты потенциалы стандартты деп аталады:
A. 0, 1 моль/л
B. 0, 2 моль/л
C. 3 моль/л
D. 2 моль/л
E. 1 моль/л
$$$C
Магний тұ зы ерітіндісіндегі Мg+2 концентрациясы 0, 001 моль/л (Е= -2, 38 B). Магнийдің электродты потенциалын тап:
A. –2, 38 В
B. 3, 85 В
C. –2, 47 В
D. –4, 12 В
E. –3, 61 В
$$$A
Нернст тең деуін кө рсет:
A. Е = E0+ 0, 059 /n. lgC
B. E = mc2
C. E = h× g
D. E = A/b
E. l = h/mv
$$$D
Химиялық реакция энергиясы, электрлік энергияғ а айналатын қ ондырғ ы қ алай аталады:
A. ионометр
B. потенциометр
C. вольметр
D. гальваникалық элемент
E. электролизер
$$$C
Қ орғ асын мен мырыштың стандартты электродты потенциалы –0, 12 В, -0, 76В.
Стандартты жағ дайдағ ы қ орғ асын- мырыштық гальваникалық элементтің электр қ озғ аушы кү шінің шамасын кө рсет:
A. 0, 43 В
B. 6, 3 В
C. 0, 64 В
D. –0, 88 В
E. 0, 76 В
$$$E
Тепе- тең дік орнағ ан кезде, ө з тұ зының ерітіндісіне батырылғ ан металл мен оны қ оршағ ан орта арасында туындайтын потенциал айырмашылығ ы:
A. стандартты потенциал
B. диффузды потенциал
C. кинетикалық потенциал
D. тепе-тең дік потенциал
E. электродты потенциал
$$$B
Металдың электродты потенциалы қ ай шартқ а тә уелсіз:
A. металл табиғ атына
B. ерітінді кө леміне
C. ерітіндідегі металл иондарының концентрациясына
D. температурағ а
E. металл иондарының активтілігіне
$$$A
Алюминий мен никель пластинкаларынан қ ұ рылғ ан жә не осы тұ здардың ерітіндісіне батырылғ ан гальваникалық элементтің электрохимиялық схемасын
кө рсет:
A. (-)А1/А1+3//Ni+2/Ni/ (+)
B. (-)Al/Al+3//Ni (+)
C. (-)Al+3//Ni+2/ (+)
D. (-)Al//Ni (+)
E. (+)Ni/Ni+2//Al+3/Al (-)
$$$C
Магний мен мырыштың стандартты потенциалдары –2, 38 В, -0, 76 В екенін ескере отырып, мына элементтің (-) Mg/Mg+2//Zn+2/Zn (+) концентрация СMg+2= 1 моль/л, СZn+2 = 0, 1 моль/л боғ андағ ы, электр қ озғ аушы кү шінің шамасын кө рсет:
A. 1, 8 В
B. 1, 7 В
C. 1, 6 В
D. 1, 5 В
E. 1, 3 В
$$$D
Қ ай элементтер жұ бынан неғ ұ рлым жоғ ары электр қ озғ аушы кү штің шамасын байқ ауғ а болады:
A. Na-Ca
B. K-Mg
C. Ag-Cu
D. Ca-Ag
E. Ag-Au
$$$D
Электролиз барысында тү зілетін зат мө лшері қ ай шартқ а пропорционал
A. ерітінді концентрациясына
B. температурағ а
C. балқ ыма кө леміне
D. ө ткен тоқ мө лшеріне
E. қ ысымғ а
$$$A
Фарадей заң ының математикалық тең деуі:
A. m = Э× I× t/F
B. m = k
C. m = a× F
D. m = i × t
E. m = Na× e
$$$E
СuSO4 ерітіндісі арқ ылы 10 минут арасында 5А тоқ ө ткізгенде бө лінген мыс массасын анық та:
A. 0, 58 г
B. 0, 69 г
C. 0, 73 г
D. 0, 86 г
E. 0, 99 г.
$$$C
Қ оршағ ан орта ә серінен металл немесе оның балқ ымасының бү лінуін қ алай атайды:
A. электролиз
B. диссоциация
C. коррозия
D. коагуляция
E. дисперсия
$$$B
Na2SO4 ерітіндісінің электролизі кезінде анодта бө лінетін зат:
A. Н2
B. О2
C. Na
D. S
E. SO2
$$$E
Егер элементтердің кернеулік қ атарында мына метыллдар K-Ca-Na-Mg-Al,
былай орналысқ ан болса, NaCl, K2SO4, CaCl2, MgCl2 тұ здарының сулы ерітінділерінің электролизі кезінде катодта тотық сызданатын зат:
A. K
B. Ca
C. Na
D. Mg
E. H2
@@@ Комплексті қ осылыстар.
$$$C
Комплексті қ осылыстардың сыртқ ы жә не ішкі сфералары арасындағ ы байланыс сипаты:
A. металдық
B. донорлы-акцепторлық
C. иондық
D. сутектік
E. коваленттік
$$$E
Мына қ осылыстағ ы [Co(NH3)5NO2]Cl комплекстү зушінің координациялық санын кө рсет:
A. 1
B. 5
C. 4
D. 3
E. 6
$$$D
Комплекстү зуге неғ ұ рлым қ абілетті элементтерді кө рсет:
A. s-элементтер
B. р-элементтер
C. f-элементтер
D. d-элементтер
E. инертті элементтер
$$$B
К4[Fe(CN)6] комплексті қ осылысындағ ы ішкі сфера заряды:
A. +2
B. -4
C. 0
D. +4
E. +3
$$$A
Қ ұ рамында 0, 1 моль [Co(H2O)5Cl]Cl2 бар ерітіндіден С1- тұ нбағ а тү сіру ү шін қ ажет AgNO3-тің мольдік мө лшерін кө рсет:
A. 0, 2
B. 0, 1
C. 0, 3
D. 0, 4
E. 0, 5
$$$A
[PtCl(NH3)5]Cl3 комплексті қ осылысындағ ы орталық ионның тотығ у дә режесі:
A. +4
B. +2
C. +3
D. +1
E. +6
$$$B
Неғ ұ рлым тұ рақ ты комплексті ион:
A. [Fe(CN)6]4- Kнест = 10-37
B. [Fe(CN)6]3- Kнест = 10-44
C. [AlF6]3- Kнест = 10-23
D. [Ag(CN)2]- Kнест = 10-23
E. [Ag(NH)3]+ Kнест = 10-9
$$$B
Комплекстү зуші мен лиганда арасындағ ы химиялық байланыс:
A. сутектік
B. донорлы-акцепторлы
C. ковалентті полюссіз
D. ковалентті полюсті
E. иондық
$$$C
[Au(CN)4]— ионындағ ы комплекстү зушінің тотығ у дә режесі:
A. 1+
B. 2+
C. 3+
D. 4+
E. 5+
$$$E
Магний трифторогидроксобериллиатындағ ы ішкі сфера заряды:
A. 1-
B. 2+
C. 3-
D. 4-
E. 2-
$$$D
(NH4)2[Pt(OH)2Cl4] комплексті қ осылысындағ ы орталық ионның координациялық саны:
A. 6
B. 5
C. 2
D. 4
E. 8
$$$B
[Co(NH3)5(H2O)]Cl3 комплексті қ осылысының типін кө рсет:
A. анионды
B. катионды
C. нетралды
D. аммиакатты
E. гидроксокомплекс
$$$A
Ва[Cr(NH3)2(CN)2]2 комплексті қ осылысындағ ы акцептор болып табылатын атомды кө рсет:
A. Сr
B. Ba
C. N
D. C
E. H
$$$C
Ғ е(СО)5 комплексті қ осылысының типін кө рсет:
A. анионды
B. катионды
C. нейтралды
D. ацидикомплекс
E. аммиакатты
@@@ Биогенді элементтер химиясы
$$$D
Фарадей заң ы бойынша электролиз кезінде бө лінген зат мө лшері тө мендегі тең деумен ө рнектеледі: 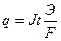
$$$A
Цинктің сұ йытылғ ан кү кірт қ ышқ ылымен ә рекеттесуі кезінде не тү зіледі:
A. Н2
B. SO2
C. H2S
D. S
Е. SO3
$$$B
Ө неркә сіпте ас содасын алу ү шін Сольве ә дісін пайдаланады, соның реакция тең деуін кө рсет:
A. Na2SO4+C+CaCO3 ®
B. NaCl + NH3 + CO2 + H2O ®
C. NaOH + CO2 + H2O ®
D. Na2O + CO2 ®
Е. (NH4)2CO3 + NaOH ®
$$$B
Магний боридінің гидролизі кезінде не тү зіледі:
A. H3BO3
B. B2H6
C. B2O3
D. H4B2O7
Е. HBO2
$$$C
Кү кіртсутекті алу ә дісін кө рсет:
A. NaOH + S ®
B. S + H2O ®
C. FeS + HCl(конц) ®
D. CuS + H2SO4 (разб) ®
Е. CuS + HNO3 (разб) ®
$$$D
Қ ышқ ыл ангидриді болып келесі оксидтер табылады:
A. N2O
B. NO
C. N2O жә не NO
D. N2O3 жә не N2O5
Е. NO жә не N2O
$$$C
Ө неркә сіпте оттекті қ андай ә діспен алатынын кө рсет:
A. KМnO4 термиялық ыдыратумен
B. MnO2 термиялық ыдыратумен
C. сұ йық ауаны фракциялық айдаумен
D. KClO3 ыдырауымен
Е. K2MnO4 ыдырауымен
$$$D
Мыс пластинкасын неде ерітуге болады:
A. HClсұ йыт
B. NaOHсұ йыт
C. H3PO4
D. HNO3 конц
Е. СН3СООН
$$$A
Марганецтің қ ай қ осылысы текқ ана тотық тырғ ыштық қ асиет кө рсетеді:
A. KМnO4
B. K2MnO4
C. MnO2
D. MnO
Е. MnSO4
$$$C
Сынап-каломель қ осылысының формуласы тө мендегідей:
A. HgSO4
B. HgCl2
C. Hg2Cl2
D. Hg2(NO3)2
Е. HgO
$$$D
Суда неғ ұ рлым жақ сы еритін гидроксидті кө рсет:
A. Mg(OH)2
B. Ca(OH)2
C. Sr(OH)2
D. Ba(OH)2
Е. Be(OH)2
$$$A
Хлорлылау қ ышқ ылының формуласын кө рсет:
A. HClO
B. HClO2
C. HClO3
D. HClO4
Е. HCl
$$$D
Фтордың сумен реакциясында не тү зілетінін кө рсет:
A. HFO, HF
B. HFO
C. HF, O2, H2
D. HF, O2
Е. HFO, O2
$$$E
SiO2 –ні ерітетін қ ышқ ылды кө рсет:
A. HCl
B. HNO3
C. H2SO4
D. H3PO4
Е. HF
$$$C
Кү йдіргіш натрды кремний диосидімен балқ ытқ анда не тү зілетінін кө рсет:
А. H2SiO3
B. NaHSiO3
C. Na2SiO3, H2O
D. Na2SiO3 жә не H2
Е. Na2O жә не H2SiO3
$$$C
Са3(PO4)2 + C + SiO2 ® мына реакция қ ай затты алуғ а пайдаланылады:
A. Si
B. CaO
C. P
D. P2O5, CO2
Е. Ca, Si
$$$A
Аммоний нитратын қ ыздырғ анда не тү зілетінін кө рсет:
A. N2O
B. N2
C. NO
D. NO2
Е. NH3
$$$B
Сілтілік металлдардың арасында неғ ұ рлым тұ рақ ты гидрид тү зетінін кө рсет:
A. К
B. Li
C. Na
D. Rb
Е. Cs
$$$E
Планетаның жылу баллансына жә не кү ннің УФ-сә улелердінің сің ірілуіне,
атмосфераның жоғ арғ ы қ абатында орналасқ ан қ андай газ ә сер етеді:
A. О2
B. СО
C. СО2
D. Н2
Е. О3
$$$C
Ө неркә сіпте кү кірт (IV) оксидін алу ү шін қ андай реакция пайдаланылатын кө рсет:
A. Cu + H2SO4 конц ®
B. Na2SO3 тв + H2SO4 ®
C. FeS2 + O2 ®
D. Na2S2O3 + HCl ®
Е. Na2SO4 + S + H2O (t0) ®
$$$E
Кү кірт қ осылыстарының ішіндегі, тек қ ана тотық сыздандарғ ыштық қ асиет кө рсететін затты кө рсет:
A. SO2
B. H2SO3
C. H2SO4
D. S
Е. H2S
$$$B
Қ ыздыру арқ ылы ақ фосфордың кү йдіргіш калий ерітіндісімен ә рекеттесуі нә тижесінде не тү зілетінін кө рсет:
А. К3РО4
B. РН3, КН2РО2
C. К3РО4 жә не РН3
D. К2НРО3
Е. К3РО4 жә не Н2О
$$$C
Бө лме температурасында сутек қ ай затпен ә рекеттеседі:
A. О2
B. N2
C. F2
D. S
Е. P
$$$E
Қ ай реакция нә тижесінде кө мірқ ышқ ыл газы тү зілмейді:
A. СаСО3 (t0) ®
B. С + О2 (t0) ®
C. СО + О2 (t0) ®
D. Н2С2О4 (t0) ®
Е. НСООН (t0, H2SO4) ®
$$$D
Табиғ атта темір қ андай қ осылыс тү рінде кездеседі:
A. FeSO4*7H2O
B. FeCl3*6H2O
C. K4[Fe(CN)6]
D. Fe3O4, FeS2
Е. Fe(OH)3, Fe(OH)2
$$$D
SO2 + H2S ® ә рекеттесуі нә тижесінде не тү зіледі:
A. SO3, H2O
B. H2, SO3
C. H2SO3
D. S, H2O
Е. H2SO3, S
$$$C
Хлорлы сутекті лабораторияда қ алай алады:
A. H2 + Cl2 ®
B. CaCl2 + H2SO4 ®
C. NaClTB + H2SO4 ®
D. BaCl2 + H2SO4 ®
Е. NaCl + HF ®
$$$C
Фосфор трихлориді РСl3 гидролизденгенде не тү зіледі:
A. НРО3
B. Н3РО4
C. Н3РО3
D. Н3РО2
Е. Н4Р2О7
$$$E
Иодты лабораторияда алу ү шін қ ай реакцияны қ олданады:
A. KJp-p + F2 ®
B. KJTB + H2SO4 конц ®
C. KJp-p + Cl2 ®
D. KJO3 p-p + Cl2 ®
Е. HJO3 p-p + Cl2 ®
$$$B
Оттегінің аллотропиялық тү рө згерістері нешеу:
A. 1
B. 2
C. 3
D. 4
Е. 5
$$$B
Силан формуласын кө рсет:
A. SiO2
B. SiH4
C. SiC
D. SiCl4
Е. CaSiO3
$$$A
Оттегі қ ай газ атмосферасында жанады:
A. F2
B. H2S
C. H2
D. N2
Е. CO2
$$$A
Кальцийдің ауада жануы кезінде не тү зілетінін кө рсет:
A. СаО
B. Са2О2
C. СаО2
D. Са3N2
Е. Са2О2 и Са3N2
$$$D
Темірді сұ йытылғ ан кү кірт қ ышқ ылыда еріту кезінде не тү зілетінін кө рсет:
А. Fe2(SO4)3
B. SO2
C. SO2 и Fe2(SO4)3
D. FeSO4 жә не H2
Е. реакция жү рмейді
$$$B
Фосфин формуласын кө рсет:
A. Р2О5
B. РН3
C. Са3Р2
D. Н3РО2
Е. РСl5
$$$C
Хлормен ә рекеттеспейтін затты кө рсет:
A. Na
B. H2
C. O2
D. KJ
Е. KBr
$$$B
SO2 жә не Cl2 қ оспасы кү н сә улесі тү суі нә тижесінде қ андай зат тү зіп, ә рекеттеседі:
A. SO3
B. SO2Cl2
C. S
D. SOCl
Е. Cl2O7
$$$D
Аммиактың оттегімен каталитикалық тотығ уы кезінде қ андай зат тү зіледі:
A. N2O
B. N2O3
C. N2O4
D. NO
Е. N2O5
$$$C
Ақ фосфор қ андай еріткіште ериді:
A. H2O
B. HCl
C. CS2
D. CH3COOH
Е. NH4OH
$$$E
Қ андай қ осылыстарды карбонилдер деп атайды:
A. металлдар мен кө міртекті
B. кө мір қ ышқ ылының тұ здарын
C. қ ымыздық қ ышқ ылының тұ здарын
D. бейметаллдар мен кө міртекті
Е. металлдар мен кө міртек оксиді
$$$A
Натрийдің ауада жануы кезінде не тү зіледі:
A. Na2O2
B. Na3N
C. Na2O
D. NaO2
Е. Na3N и Na2O
@@@ Сандық анализ.
$$$D
Сутектік кө рсеткіш:
А. pOH=-lg[OH-]; B. Kсу=[H+]*[OH-]; C. Kсу=-lg[H+];
D. pH=-lg[H+]; E. pH+pOH.
$$$B
Судың иондық кө бейтіндісінің мә ні:
А. 10-7; В. 10-14; С. 10-10; D. 7; Е. 14.
$$$C
Сутектік жә не гидроксидтік кө рсеткіштер байланысы мына формуламен кө рсетіледі:
А. рН+рОН=10-11; В. рН+рОН=10-14; С. рН+рОН=14
D. рН-рОН=14; Е. рН+рОН=1014.
$$$B
Ерітіндінің нейтрал ортасын сутегі ионының [H+] мына концентрациясымен кө рсетіледі (моль/л):
А. 0, 1; В. 10-7; С. 10-8; D. 0, 7; Е. 10-14.
$$$C
Сілтілік ерітіндіні сутегі ионының [H+] мына концентрациясы кө рсетіледі:
А. 7; В. 14; С. 10-3; D. 10-11; Е. 10-14.
$$$D
Қ ышқ ылдық ерітіндіні сутегі ионының [H+] мына концентрациясы кө рсетіледі (моль/л):
А. 14; В. 7; С. 3; D. 10-3; Е. 10-14.
$$$E
Ерітіндінің рН-тен 1-ге азаюы ү шін қ осылатын зат:
А. су; В. КОН; С. NaOH; D. сілті; E. HCI.
$$$D
Мына тұ з гидролизге ұ шырайды:
А. натрий хлориді; В. калий хлориді;
С. кальций хлориді; D. натрий карбонаты;
Е. калий нитраты.
$$$C
Мына тұ з гидролизге тү седі:
А. натрий хлориді; В. калий сульфаты;
С. натрий фосфаты; D. калий нитраты;
Е. калий хлориді.
$$$A
0, 5М Н3РО4 ерітіндісінің нормальді концентрациясы (н. ):
А. 1, 5; В. 2, 7; С. 2, 5; D. 1, 3; Е. 2, 3.
$$$A
Стандартты, титрленген ерітінді деп:
А. Титриметриялық анализ ә дісінде қ олданылатын
Концентрациясы дә л анық талғ ан В реагентінің ерітіндісі,
В. Реакцияғ а тү сетін зат,
С. Реакция нә тижесінде алынғ ан зат,
D. Ерітінді дайындауғ а алынғ ан зат,
Е. Жауабы В, С.
$$$C
250 мл NaOH ерітіндісіне 10, 00г осы зат еріген, оның титрі:
А. 0, 04500г/мл В. 0, 2500г/мл С. 0, 0400г/мл D. 0, 20г/мл Е. 0, 5г/мл
$$$D
РН=5 кезінде метилоранж тү сі:
А. тоқ сары, В. сары, С. тү ссіз, D. қ ызыл, Е. кү лгін.
$$$A
Индикатор дегеніміз:
А. Эквиваленттік нү ктені анық тау ү шін қ ажет зат,
В. Титрлеу ү шін қ ажет зат,
С. Концентрациясы дә л табылғ ан зат (титрант),
D. Фиксонал,
Е. Жауабы С, Д.
$$$E
5л ерітіндіде неше грамм H2SO4 бар, егер оның 25, 00 мл-не 22, 00 мл 0, 09500н КОН ерітіндісі жұ мсалса:
А. 20, 55г В. 20, 97г С. 20, 19г D. 19, 16г Е. 20, 48г
$$$A
0, 1М СН3СООН жә не 0, 1М CH3COONa тұ ратын буфер ерітіндісінің рН-ын есепте (Кд=1, 82*10-5):
А. 4, 75 В. 5, 20 С. 4, 80 D. 6, 24 Е. 3, 20
$$$B
Қ андай затты буфер ерітінділер деп атайды?
А. реакцияны тоқ тату ү шін қ олданылатын заттар,
В. сутегі иондарының концентрациясы сұ йытылғ аннан,
концентрленгенннен, аз мө лшерде қ ышқ ыл не сілті
ерітіндісін қ осқ аннан ө згермейтін ерітінділер,
С. коллоидты ерітінділер тү зетін заттар,
D. титрлеу кезінде тү сін ө згертетін заттар,
Е. Жауабы А, В, С.
$$$B
Егер 100мл суды титрлеуге 5, 00мл 0, 009н НСI ерітіндісі жұ мсалса, карбонатты кермектік нешеге тең?
А. 3, 89мэкв/л В. 4, 50мэкв/л С. 5, 05мэкв/л
D. 7, 30мэкв/л Е. 0, 3мэкв/л.
$$$A
Мына заттар қ оспасы буфер ерітінді болмайды:
А. NaOH+HCI B. CH3COOH+CH3COONa
C. NH4CI+NH4OH D. Na2CO3+NaHCO3
E. HCOOH+HCOONa.
$$$D
0, 057моль/л аммияк жә не 0, 1 моль/л аммоний хлоридінен
тұ ратын буфер ерітіндісінің рН-ы (КД=1, 76*10-5):
А. 0, 05 В. 7, 20 С. 9, 00 D. 5, 00 Е. 4, 15.
$$$A
Титриметриялық анализ негізінде:
А. Реакцияғ а кеткен дә л анық талғ ан реагент ерітіндісінің кө лемін
дә л ө лшеу;
В. Реагенттің ә р компонентін анық тау;
С. Ерітінді тү сінің қ оюлығ ын анық тау;
D. Индикатор тү сінің ө згеру;
Е. Индикатордың ө згеру интервалын анық тау.
$$$B
Титрлеу ү шін қ олданылатын ыдыс:
А. Цилиндр, В. Бюретка, С. Бюкс, D. Таразы, Е. Пипетка.
$$$C
Егер сү ттің қ ышқ ылдығ ы 17, 50Т болса, сү т қ ышқ ылының (СН3СНОНСООН) проценттік концентрациясы қ анша (%)?
А. 17, 5 В. 18, 18 С. 15, 75 D. 12, 45 Е. 11, 26.
$$$A
Индикатор тү сінің ө згеру интервалы деп:
А. Индикатор тү сі ө згерісі байқ алатын рН мә нінің интервалы;
В. Эквивалент нү кте пайда болғ ан кез;
С. Реакцияғ а қ атысатын заттар;
D. Индикаторлық кө рсеткіш мә ні;
Е. Аналитикалық кө рсеткіш мә ні.
$$$B
0, 0340г AgNO3 титрлеу ү шін 20, 00мл HCI ерітіндісі жұ мсалса, T HCI/Ag нешеге тең (г/мл):
А. 0, 0085 В. 0, 0011077 С. 0, 200000 D. 0, 02 Е. 0, 0020
$$$B
1л HNO3 ерітіндісінің дайындау ү шін оның 0, 2н. ерітіндісінен 50мл алғ ан болса, пайда болғ ан ерітіндінің титрі нешеге тең (г/мл):
A. 0, 004780 B. 0, 00063 C. 0, 0004516 D. 0, 056 E. 0, 0014
$$$B
0, 5н H2SO4 ерітіндісін n(1/2 H2SO4)=0, 1г/моль фиксаналынан дайындау ү шін қ андай ыдыс алу керек?
А. ө лшегіш колба 50 мл; В. ө лшегіш колба 200 мл;
C. цилиндр 100 мл; D. цилиндр 1000 мл;
Е. цилиндр 50 мл.
@@@
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|