
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
NH4NO3 → N2O + 2H2O
NH4NO3 → N2O + 2H2O
Категория Анализ смесей катионов (выбор)
:: 001:: Для совместного обнаружения ионов калия и кобальта(II) в уксуснокислой среде необходимо подействовать
перексидом водорода
нитритом калия
нитратом натрия
бихроматом калия
:: 002:: Для обнаружения ионов Co 2+ в присутствии ионов Fe3+ реактивом NH4SCN необходимо добавить
NH4OH
NH4F
NH4Cl
NH4Br
:: 003:: В смеси Fe 2+, Fe 3+, Al 3+ действием избытка NaOH можно выделить катионы
Fe2+
Fe3+
Al3+
Fe2+, Fe3+
:: 004:: Катион, который можно отделить в виде гидроксида из смеси ионов Al3+, Zn2+, Со2+, Sn2+ при действии избытка NaOH
Al3+
Sn2+
Co2+
Zn2+
:: 005:: Для полного отделения ионов Zn(II) от ионов Al(III) с помощью реакции
Zn(OH)2 + 4NH3 → [Zn(NH3)4]2+ + 2OH- необходимо обеспечить
нагревание
охлаждение
избыток NH3
повышение концентрации ионов OH-
:: 006:: При добавлении NaOH к раствору, содержащему катионы NH 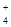 , К+, Ag+, Ba2+ осадок не образует ион
, К+, Ag+, Ba2+ осадок не образует ион
Ba2+
NH 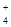
Ag+
К+
:: 007:: Обнаружению ионов К+ с использованием реактива Na3[Co(NO2)6] в водном растворе мешают ионы
аммония
натрия
цезия
магния
:: 008:: Для избирательного обнаружения ионов бария в водном растворе можно подействовать
хроматом калия
бихроматом калия в присутствии щелочи
бихроматом калия в присутствии ацетата натрия
пероксидом водорода
:: 009:: Обнаружению ионов Zn2+ гексацианоферратом(II) калия мешают катионы
аммония
железа (II)
хрома(III)
марганца(II)
:: 010:: Обнаружению ионов свинца с хроматом калия мешают катионы
Cu+
Au+
Ni2+
Ba2+
Категория Аналитические реактивы на анионы (выбор)
:: 001:: Сульфид-ионы в водном растворе можно обнаружить путем действия
хлорида магния
хлористоводородной кислоты
аммиачной воды
сульфата меди(II)
:: 002:: Иодид-ионы в кислой среде можно обнаружить путем добавления
сульфата калия
хлорной воды
аммиачной воды
хлорида меди(II)
:: 003:: Ацетат-ионы в нейтральной среде можно обнаружить путем действия
хлорида железа(II)
хлорида железа(III)
ацетона
аммиачной воды
:: 004:: Карбонат-ионы в водном растворе можно обнаружить после добавления кислоты при помощи
хлорной воды
сульфида калия
известковой воды
аммиачной воды
:: 005:: Действием AgNO3 + HNO3 обнаруживают анионы
CrO 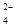
Cr2O 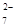
Cl-
Br-
:: 006:: Действием BaCl2 + HCl обнаруживают анионы:
сульфат
нитрат
нитрит
ацетат
:: 007:: Действием дифениламина в среде концентрированной серной кислоты обнаруживают анионы:
хлорид
бромид
нитрат
сульфат
Категория Аналитическая классификация анионов (выбор)
:: 001:: Согласно классификации анионов, основанной на различной растворимости солей бария и серебра в воде, к I группе относят анионы
S 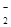 , Cl-, Br-, I-
, Cl-, Br-, I-
NO 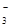 , NO
, NO 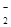 , CH3COO-
, CH3COO-
CO 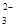 , SiO
, SiO 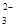 , PO
, PO 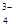
SO 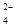 , SO
, SO 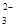 , S2O
, S2O 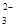
:: 002:: Согласно классификации анионов, основанной на различной растворимости солей бария и серебра в воде, к III группе относят анионы
NO 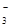 , NO
, NO 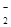 , CH3COO-
, CH3COO-
CO 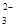 , SiO
, SiO 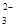 , PO
, PO 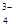
SO 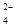 , SO
, SO 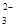 , S2O
, S2O 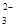 , F-
, F-
S 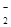 , Cl-, Br-, I-
, Cl-, Br-, I-
Категория Анализ неизвестного вещества (выбор)
:: 001:: Если при пропускании сероводорода через исследуемый раствор с pH 0, 5 выпадает желтый осадок, то в растворе присутствовали ионы
цинка
кадмия
ртути(II)
свинца
:: 002:: При пропускании сероводорода через исследуемый раствор при pH 0, 5 не выпадает осадок сульфида
цинка
кадмия
ртути(II)
свинца
:: 003:: При действии на солянокислый раствор анализируемого вещества хлорида бария образуется белый осадок, нерастворимый в HCl.
В анализируемом растворе присутствуют ионы
NO 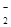
NO 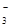
SO 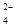
СО 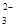
:: 004:: Газ, который окрашивает фильтровальную бумагу смоченную раствором Pb(CH3COO)2 в черный цвет
CO2
NO
H2S
NH3
:: 005:: Пламя горелки окрашивают в желтый цвет соли
бария
цезия
натрия
калия
:: 006:: Пламя горелки окрашивают в зеленый цвет соединения
калия
меди
стронция
натрия
:: 007:: Хорошо растворимое в воде бесцветное кристаллическое вещество, при нагревании разлагается с выделением бурого газа, с HCl образует творожистый осадок, с дифениламином в среде концентрированной H2SO4 дает фиолетовое окрашивание. Укажите это вещество.
AgCl
AgNO3
Ag2SO4
КNO3
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|