
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Основное уравнение МКТ газов. Модель идеального газа. Хаотичность молекулярного движения
Основное уравнение МКТ газов
Модель идеального газа
1. Межмолекулярные силы притяжения отсутствуют (можно пренебречь потенциальной энергией).
2. Взаимодействия молекул газа происходят только при их соударениях и являются упругими
3. Молекулы газа не имеют объема - рассматриваются как материальные точки.
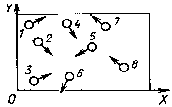
Хаотичность молекулярного движения
Проекции скоростей молекул на оси Ох и Оу положительны или отрицательны.
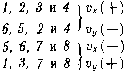
Модель: идеальный газ.
Задача: связать макроскопические параметры (то, что можно измерить) и микроскопические параметры (характеристики молекул), например давление и скорость движения молекул.
Следствие опыта: давление газа объясняется ударами молекул о дно и стенки сосуда.
Предварительное обсуждение:
1. Давление тем больше, чем больше количество ударов. Количество ударов определяется концентрацией молекул. Значит, давление зависит от концентрации.
2. Давление тем больше, чем больше энергия соударения, т.е. чем больше кинетическая энергия молекулы. Значит, давление зависит от массы молекул и квадрата скорости движения молекул.
3. Т.к. все молекулы движутся с различными скоростями, то некоторые молекулы не успеют долететь до стенки.
4. Т.к. молекулы движутся в различных направлениях, то необходимо учесть, что не все молекулы смогут принять участие в создании давления. Т.к. молекул много, то скорости молекул можно усреднить.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|