
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Химия 17 . Задача №1.. Задача №2
Гр.189 СА
Химия 17
Тема урока: Решение задач по химическим уравнениям.
Тип урока: Консультация.
План урока:
- Прорешайте образцы решения задач.
- Решите задачу по своему варианту..
- Выполненное задание направить в личном сообщении https://vk.com/id5826096
Индивидуальное задание для самостоятельного решения:
Задача №1.
1. Какая соль и в каком количестве получится, если аммиак объёмом 2,24 л.(н.у.) пропустить через раствор дигидрофосфата аммония массой 115 г. с массовой долей (NH4)H2PO4 10%?
Образец решения:
а) Записываем уравнение реакций:
2,24 л. 11,5 г. Х г.
NH3 + (NH4)H2PO4 ® (NH4)2HPO4
22,4 л. 115 г. 132 г.
б) Условия задачи показываем над уравнением, найденные молекулярные массы - под уравнением.
в) Находим массу дигидрофосфата аммония по формуле:
w(х)= 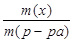 ; m(х)= w(х)´m(р-ра); m(x)= 0,1´115= 11,5 г. (NH4)H2PO4.
; m(х)= w(х)´m(р-ра); m(x)= 0,1´115= 11,5 г. (NH4)H2PO4.
г) Проставляем найденное значение над уравнением реакции и находим по уравнению какое из реагирующих веществ взято в избытке:
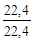 =
=  - вещества взяты в равных количествах.
- вещества взяты в равных количествах.
д) Находим массу получившейся соли, составляя пропорции с любым из реагирующим веществом:
2,24 л. NH3 - х г.
2,24 л. NH3 - 132 г.
х = 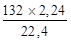 ; х = 13,2 г. (NH4)HPO4.
; х = 13,2 г. (NH4)HPO4.
е) Записываем ответ: 13,2 г. (NH4)HPO4.
Задача №2
Вычислите массу оксида углерода (IV), который может быть получен при обработке мрамора массой 100 г. с массовой долей CaCO3 95% р-ром соляной кислоты массой 200 г. с массовой долей HCl 25%.
Образец решения:
а) Записываем уравнение реакции:
95 г. 50 г. Х г.
СаСО3 + 2НСl ® СaCl2 + CO2 + H2O
100 г. 73 г. 44 г.
б) Условия задачи указываем над уравнением, найденные молекулярные массы - под уравнением.
в) Находим массу чистого CaCO3:
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|