
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Кафедра: «Физика». Лабораторная работа № 1.01. Изучение спектра водорода и определение постоянной Ридберга». Лабораторная работа № 1.01. Изучение спектра водорода и определение постоянной Ридберга». ВВЕДЕНИЕ
Федеральное агентство по образованию
Муромский институт (филиал)
Государственного образовательного учреждения высшего профессионального образования
Владимирский государственный университет
Кафедра: «Физика»
Дисциплина: физика
Лабораторная работа № 1.01
«Изучение спектра водорода и определение постоянной Ридберга»
Утверждена на методическом семинаре кафедры физики
Зав. кафедрой_____________
Муром 2005
| |
ТЕХНИКА БЕЗОПАСНОСТИ
1. Сборку и разборку схемы производить только при отключенном источнике питания.
2. Не включать собранную схему, пока не изучите инструкцию по данной работе и не получите на это разрешение лаборанта или преподавателя.
3. Схема должна находиться под напряжением только во время регулировки и снятия показаний с приборов. КАТЕГОРИЧЕСКИ ЗАПРЕЩАЕТСЯ оставлять схему под напряжением без присмотра.
4. Строго соблюдать порядок выполнения работы, описаний и инструкции.
5. На рабочем месте не должно быть посторонних предметов. Твёрдо знать, где расположен общий выключатель и порядок пользования им.
6. После окончания работы отключить источник питания, а затем разобрать схему и привести в порядок рабочее место.
Лабораторная работа № 1.01
«Изучение спектра водорода и определение постоянной Ридберга»
ПРИБОРЫ И ПРИНАДЛЕЖНОСТИ:
- двухтрубный спектроскоп;
- дуговая ртутная лампа;
- газоразрядная трубка с водородом, укреплённая в специальном держателе;
- выпрямитель.
1 ВВЕДЕНИЕ
1.1 Закономерности в атомных спектрах
Разряженные газы, пары металлов испускают спектр, состоящий из отдельных спектральных линий. В соответствие с этим спектр испускания веществ, образованный возбужденными атомами называется линейчатым спектром.
Изучение атомных спектров послужило ключом к познанию строения атомов. Прежде всего, было замечено, что линии в спектрах многих атомов расположены не беспорядочно, а объединяются в группы, или как их называют серии спектральных линий. Отчётливее всего это обнаруживается в спектре простейшего атома – водорода.
Швейцарский физик Бальмер в 1885 году установил, что длины волн спектральных линий в видимой области спектра укладываются в простейшую формулу:
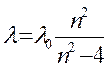 (1),
(1),
где  - целое число, принимающее значения 3, 4, 5, 6 и т. д.
- целое число, принимающее значения 3, 4, 5, 6 и т. д.
В спектроскопии принято характеризовать спектральные линии величиной, обратной длине волны  , которая называется волновым числом.
, которая называется волновым числом.
Если преобразовать формулу (1) в выражение для чисел, то получим:
 (2),
(2),
где  =3, 4, 5, 6, ……,
=3, 4, 5, 6, ……,
 - постоянная Ридберга
- постоянная Ридберга
R=10973730,9 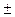 0,012 см
0,012 см 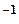 или
или 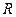 =1,097
=1,097  107 м
107 м 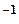 .
.
Дальнейшие исследования показали, что в спектре водорода имеется ещё несколько серий. Оказывается, что волновые числа всех серий в спектре
атомарного водорода можно выразить одной формулой, обобщающей формулу Бальмера (2):
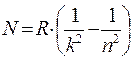 (3).
(3).
Из (3) находим волновые числа всех линий.
1. Серия Лаймана. Находится в ультрафиолетовой области спектра. Для неё 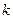 =1,
=1, 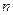 =2, 3, 4, 5, и т. д.:
=2, 3, 4, 5, и т. д.:
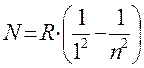 .
.
2. Серия Бальмера.(см. формулу (2)).
3. Серия Пашена. Находим в ближайшей инфракрасной области. 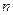 =4, 5, 6:
=4, 5, 6:
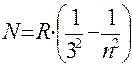 .
.
В инфракрасной области обнаружено ещё несколько серий.
1.2 Атом водорода по теории Бора.
Опытами Резерфорда по рассеянию  -частиц веществом была обоснована ядерная (планетарная) модель атома. Однако ядерная модель атома оказалась в противоречии с законами классической механики и электродинамики. Классическая теория не смогла объяснить ни устойчивости атомов, ни дискретный (линейчатый) спектр атомов.
-частиц веществом была обоснована ядерная (планетарная) модель атома. Однако ядерная модель атома оказалась в противоречии с законами классической механики и электродинамики. Классическая теория не смогла объяснить ни устойчивости атомов, ни дискретный (линейчатый) спектр атомов.
Выход из создавшегося (положения) тупика был найден в 1913 году датским физиком Бором на основании предположений, противоречащих классической физике. Эти предположения содержатся в двух высказанных им постулатах.
1) Из бесконечного множества электронных орбит, возможных с точки зрения классической физики, осуществляются только определенные, стационарные орбиты, для которых орбитальный момент количества движения (импульс) 
 электрона может принимать ряд дискретных значений.
электрона может принимать ряд дискретных значений.
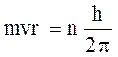 (4),
(4),
 |
или
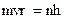 ,
, 
 |
где
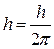 , а
, а 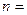 1, 2, 3,….
1, 2, 3,….
Пока электрон движется по стационарной орбите, атом не излучает и не поглощает света.
2) При переходе электрона с одной стационарной орбиты на другую происходит излучение или поглощение кванта света, энергия которого равна разности энергий электрона при движении по соответствующим стационарным орбитам с номерами 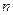 и k
и k
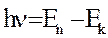 (5).
(5).
Если 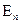 >
> 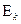 , то имеет место излучение света. Когда наблюдается
, то имеет место излучение света. Когда наблюдается 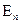 <
< 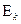 , то происходит поглощение света.
, то происходит поглощение света.
Рассмотрим атом водорода и предположим, что электрон вокруг ядра движется по круговым орбитам. Используя формулу (4) и применяя закон Ньютона к движению электрона:
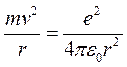 (6).
(6).
Найдём радиус электронных орбит:
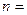 1, 2, 3,….,
1, 2, 3,….,
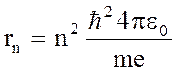
и скорости электронов на них:
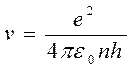
Легко найти и энергию атома водорода при движении электрона по стационарной орбите.
 (7).
(7).
Исходя из условия частот Бора (5) и вводя в рассмотрение волновое число, получим:
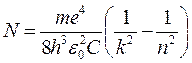 (8).
(8).
Сравнивая с (3), получим, что
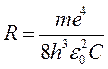 .
.
В (8) запишется:
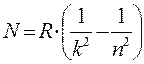 или
или 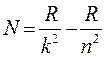
Числа  и
и 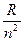 получили название спектральных термов. Они пропорциональны энергии стационарных состояний атома.
получили название спектральных термов. Они пропорциональны энергии стационарных состояний атома.
1.3. Квантомеханическая теория атома водорода.
Теория Бора объяснила все основные закономерности в спектре водорода. Однако она не смогла построить теорию атома гелия. Самой слабой стороной теории Бора была ее внутренняя противоречивость. Эта теория не была ни последовательно классической, ни последовательно квантовой. Она представляет собой лишь переходный этап на пути к созданию последовательной теории атомных явлений. Такой теорией стала квантовая механика.
В 1924 году французский физик Луи де Бройль выдвинул гипотезу о том, что все микрочастицы обладают волновыми свойствами. По идее де Бройля с движением микрочастиц связана волна. Эти волны имеют длину
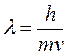 (9).
(9).
Состояние движения микрочастиц описывается волновой функцией координат частицы и времени 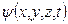 . Например, с движением свободной частицы связана плоская волна, уравнение которой может быть записано в виде:
. Например, с движением свободной частицы связана плоская волна, уравнение которой может быть записано в виде:
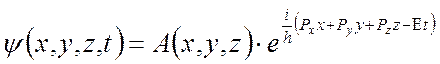 (10), где
(10), где 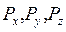 - соответствующие импульсы частицы;
- соответствующие импульсы частицы;
а 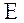 - её энергия.
- её энергия.
Физический смысл волновой функции состоит в том, что квадрат ее модуля дает плотность вероятности (вероятность, отнесенную к единице объема) нахождения частицы в соответствующем объеме пространства.
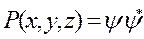
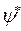 - комплексное сопряжение с
- комплексное сопряжение с 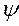 .
.
Волновая функция может быть найдена путем решения уравнения:
 |  |
 (11).
(11).
Это уравнение получено Шредингером в 1926 году и называется временным уравнением Шредингера. Здесь 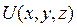 - потенциальная энергия частицы.
- потенциальная энергия частицы.
Как видно из (2) вид волновой функции определяется потенциальной энергией 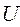 , т.е. природой всех сил, которые действуют на частицу. Для стационарных состояний уравнение Шредингера примет вид:
, т.е. природой всех сил, которые действуют на частицу. Для стационарных состояний уравнение Шредингера примет вид:
 |
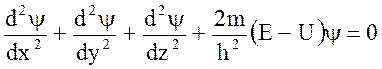 (12).
(12).
Здесь Е - полная энергия частицы, U - ее потенциальная энергия. Решение уравнения (12) позволяет найти волновые функции и полную энергию любой квантомеханической системы. Применим уравнение Шредингера для атома водорода. В атоме водорода потенциальная энергия равна:
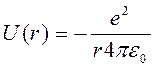
где r – расстояние электрона от ядра.
Потенциальное поле обладает сферической симметрией. Удобно внести в рассмотрение сферические координаты 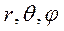 , тогда уравнение Шредингера запишется:
, тогда уравнение Шредингера запишется:
 |
 (13).
(13).
Это уравнение имеет физически обоснованные решения при любых
положительных значениях энергии Е и при дискретных отрицательных значениях Е равных:
 |
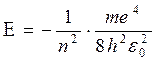 , где n = 1,2,3,…. (14)
, где n = 1,2,3,…. (14)
Случай Е > 0 соответствует электрону, пролетающему вблизи ядра и удаляющемуся в бесконечность. Случай Е < 0 соответствует электрону, находящемуся в пределах атома.
Сравнивая (14) и (7) видно, что квантовая механика приводит к тем же значениям энергии атома водорода, что и теория Бора. Однако в квантовой механике эти значения получаются логическим путем из ее основных положений без каких-либо дополнительных предположений. Число n, определяющее значение энергии электрона в (14) называется главным квантовым числом. Решение уравнения (13) дает значения орбитального момента импульса (количества движения) электрона.
LZ = 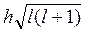 (15),
(15),
где 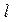 - азимутное или орбитальное квантовое число, принимающее значения
- азимутное или орбитальное квантовое число, принимающее значения 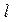 =0, 1, 2, ..., n-1 (всего n-значений).
=0, 1, 2, ..., n-1 (всего n-значений).
Из решения уравнения (13) следует, что ряд дискретных значений принимает так же проекция орбитального момента на выделенное направление в пространстве (оно обычно принимается за направление оси OZ - направление магнитной индукции).
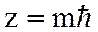 (16),
(16),
где 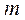 - магнитное квантовое число, принимающее значения
- магнитное квантовое число, принимающее значения 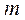 =0,
=0, 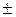 1,
1, 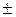 2, …
2, … 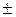
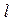 , всего
, всего 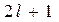 - значения для данного
- значения для данного 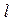 .
.
Каждому значению энергии Е соответствует несколько состояний электрона в атоме, отличающихся значением квантовых чисел 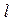 ,
, 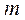 . Состояния с одинаковой энергией называются вырожденными, а число таких состояний называется кратностью вырождения. Легко можно доказать, что в атоме водорода кратность вырождения равна n. Согласно (14) можно схематически изобразить энергетические уравни атома водорода (рис. 1).
. Состояния с одинаковой энергией называются вырожденными, а число таких состояний называется кратностью вырождения. Легко можно доказать, что в атоме водорода кратность вырождения равна n. Согласно (14) можно схематически изобразить энергетические уравни атома водорода (рис. 1).
Состояние с Е=0 соответствует поляризованному атому водорода. Рассмотрим основное состояние атома водорода (n=1). Для него 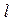 =0 и
=0 и 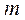 =0. Следовательно, в основном состоянии атома водорода его единственный электрон не обладает орбитальным моментом импульса. Полученный результат совершенно не понятен с точки зрения классической физики. Электрону присущи волновые свойства, учет которых позволяет объяснить отсутствие механического момента, связанного с орбитальным движением электрона в основном состоянии атома.
=0. Следовательно, в основном состоянии атома водорода его единственный электрон не обладает орбитальным моментом импульса. Полученный результат совершенно не понятен с точки зрения классической физики. Электрону присущи волновые свойства, учет которых позволяет объяснить отсутствие механического момента, связанного с орбитальным движением электрона в основном состоянии атома.
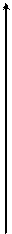







 n=5
n=5

 n=4
n=4
|
 n=3
n=3
 n=2
n=2
 n=1
n=1
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|