
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Основания Бренстеда.
5.2.2. Основания Бренстеда.
Для оснований Бренстеда действуют те же закономерности, что и для кислот. Также рассматривается кислотно-основная реакция, которая приводит к образованию сопряженной кислоты:
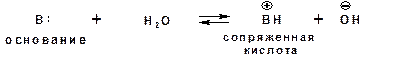
Константу равновесия обозначают как Кb
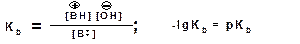
Чем больше Кb , тем выше сила основания.
Более универсальной оценкой силы органического основания, является рКа его сопряженной кислоты - рКа(ВН+):
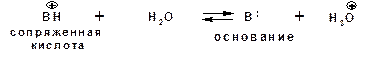
Соответствующая константа и рК:
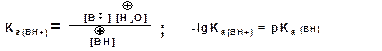
Слабым основаниям соответствуют сильные сопряженные кислоты и наоборот: сильным основаниям соответствуют слабые сопряженные кислоты. Типичными органическими основаниями по Бренстеду являются амины. Проиэтом алифатические амины значительно более сильные основания, чем ароматические.
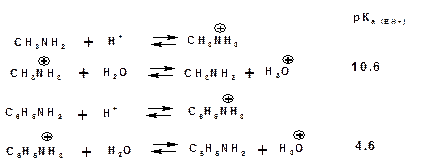
В молекуле анилина НЭП атома азота сопряжена с π-электронами бензольного кольца. Этот эффект повышает силу его сопряженной кислоты и соответственно снижает основность анилина по сравнению с метиламином:
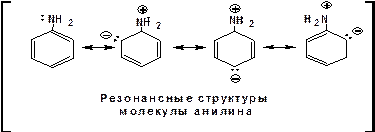
В молекуле метиламина НЭП полностью локализована на атоме азота. Это способствует снижению силы его сопряженной кислоты, а следовательно повышает основность анилина.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|