
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Запишем уравнения реакций
Запишем уравнения реакций
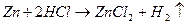
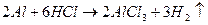
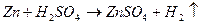
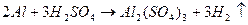
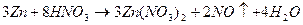
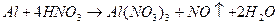
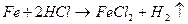
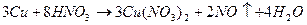
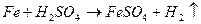 Pb + 4HNO3 -> Pb(NO3)2 + 2NO2 + 2H2O
Pb + 4HNO3 -> Pb(NO3)2 + 2NO2 + 2H2O
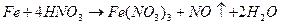
Опыт 4. Отношение алюминия к щелочам
Кусочек Al погрузили в раствор щелочи. Сначала реакция задерживалась из-за растворения оксидной пленки, а затем начала протекать бурно с выделением водорода и образованием алюмината натрия.
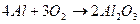
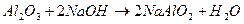
Освобожденный от пленки алюминий, будучи активным металлом, взаимодействует с водой подобно щелочным и щелочноземельным металлам:
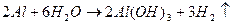
Образовавшийся гидроксид алюминия, являясь амфотерным гидроксидом, взаимодействует со щелочью:
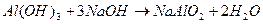
Складывая последние два уравнения, получаем суммарное уравнение взаимодействия алюминия с раствором щелочи:
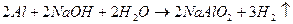
Вывод: в ходе проделанной работы мы ознакомились с различными поведениями металлов при взаимодействии с кислотами и щелочами. Оказалось, что при нагревании реакции протекают более выражено.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|