
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
I. Промышленный способ. II. Лабораторный способ. I.ХР присоединения. II.ХР окисления. Домашнее задание
I. Промышленный способ
1.Крекинг (расщепление алканов, керосина)
2. Дегидрирование алканов
500°; Ni
СН3—СН3 — СН2=СН2 + Н2.
Этан этилен
II. Лабораторный способ
1.Дегидратация этилового спирта (отщепление воды)
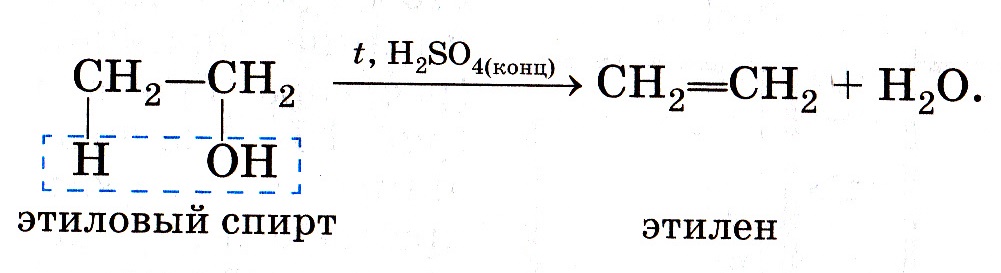
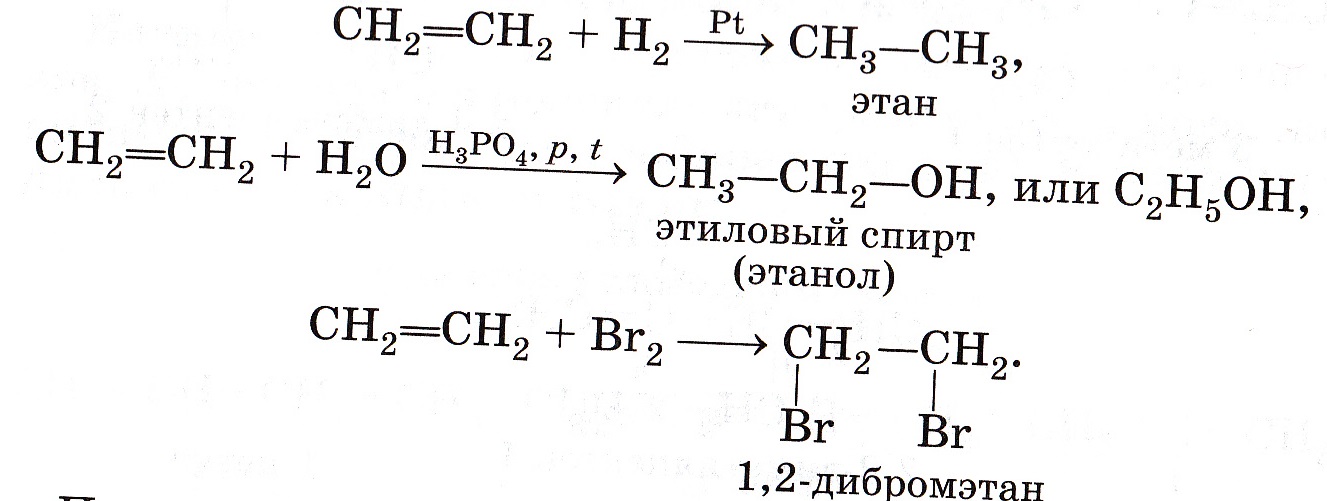
|
СН2=СН2 симметричный алкен
СН2=СН—СН3 несимметричный алкен
I.ХР присоединения
1.Гидрирование (присоединение водорода)
2. Гидратация (присоединение воды)
3.Галогенирование (присоединение галогенов)
(качественная реакция на кратную связь (двойную,
тройную)
4.Полимеризация
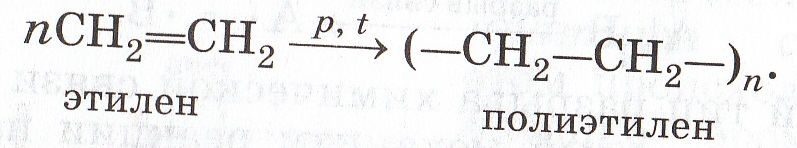

II.ХР окисления
1.Горение
2С3Н6 + 9О2 — 6СО2 + 6Н2О
2. Обесцвечивание раствора перманганата калия (марганцовка) — качественная р-я на АЛКЕНЫ (р—я Вюрца)
[О]
СН2=СН2 + KMnO4 — НО— СН2=СН2 — ОН
Домашнее задание
· §4 (читать весь, конспект), письменно выполнить №7 (стр. 32), запишите в тетради уравнения взаимодействия пропена с водородом, кислородом, водой, хлором, реакцию полимеризации
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|