
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
См. рис. 11 на стр. 57
См. рис. 11 на стр. 57
Элементы – неметаллы более способны, по сравнению с металлами, к аллотропии.
 Способность атомов одного химического элемента образовывать несколько простых веществ называется аллотропией, а эти простые вещества – аллотропными видоизменениями или модификациями.
Способность атомов одного химического элемента образовывать несколько простых веществ называется аллотропией, а эти простые вещества – аллотропными видоизменениями или модификациями.
Ковкость отсутствует
Блеска нет
Теплопроводность (только графит)
Цвет разнообразный: желтый, желтовато-зеленый, красно-бурый.
Электропроводность (только графит и черный Фосфор.)
Агрегатное состояние:
газообразное(H2, O2, Cl2 ,F2, O3)
твердое (Р, С)
жидкое (Br2)
4. Химические свойства неметаллов.
Работаем с текстом учебника стр. 58-61
1) Перед вам ряд электроотрицательности неметаллов
 Окислитель – элемент, принимающий электроны;
Окислитель – элемент, принимающий электроны;
Восстановитель элемент, отдающий электроны.
Фтор – самый электроотрицательный элемент, он не отдает свои электроны другим элементам.
Кислород отдает свои электроны только фтору, у остальных элементов он электроны принимает.
Азот отдает свои электроны кислороду и т.д.
Один и тот же неметалл может быть как окислителем, так и восстановителем в зависимости от того, с каким элементом он вступает в реакцию.
Ознакомьтесь с разделом «Окислительные свойства» стр. 58 – 60
Ознакомьтесь с разделом «Восстановительные свойства» стр. 60 – 61.
IV. Задания
1) Перепишите текст, вставив пропущенные слова
Атомы ____ в отличие от атомов ____ легко принимают наружные электроны, являются ____.
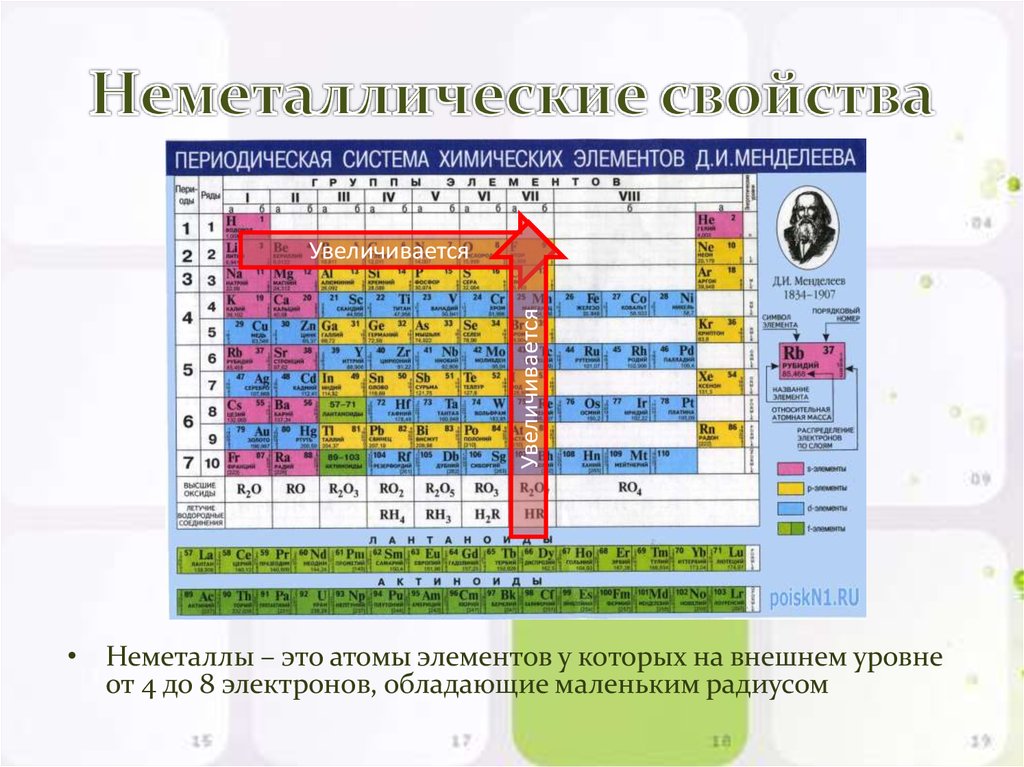
Неметаллические свойства элементов с увеличением порядкового номера в периодах ____
В группах неметаллические свойства элементов ____
2) Пользуясь периодической таблицей, запишите молекулярные формулы высших оксидов неметаллов III периода. Как будет изменяться кислотный характер?
3) Водород занимает в периодической таблице два места: в I А группе и в VII А группе. Запишите молекулярные формулы водородных соединений Na, K, Cl, F.
4) Определите, окислителем или восстановителем является сера в следующих реакциях:
H2+S=H2S
2SO2 + O2 → 2SO3
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|