
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Воздействие или реактив. Наблюдаемая реакция
Воздействие или реактив
Наблюдаемая реакция
Пламя
Карминово-красное окрашивание
Пламя
Желтое окрашивание
Пламя
Фиолетовое окрашивание
Пламя
Кирпично-красное окрашивание
Пламя
Карминово-красное окрашивание
Пламя
S042-
Желто-зеленое окрашивание
Выпадение белого осадка, не растворимого в кислотах: Ва2+ + S042- 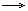 BaS04
BaS04 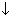
Вода
Гидратированные ионы Сu2+ имеют голубую окраску
S2-
Выпадение черного осадка: Pb2+ + S2- 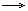 PbS
PbS 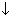
Cl-
Выпадение белого осадка; не растворимого в HNO3, но растворимого в конц.NH3 • Н20:
Аg+ +Cl- 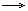 AgCl
AgCl 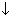
Гексациано-феррат (III) калия (красная кровяная соль) K3[Fe(CN)6]
Выпадение синего осадка:
К++ Fe2+ + [Fe(CN)6]3- 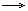 KFe[Fe(CN)6]4
KFe[Fe(CN)6]4
1) гексацианоферрат (II) калия (желтая
кровяная соль)
K4[Fe(CN)6]
2) роданид-ион
SCN-
Выпадение синего осадка:
К+ + Fe3+ + [Fe(CN)6]4- 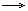 KFe[Fe(CN)6]
KFe[Fe(CN)6] 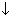
Появление ярко-красного окрашивания за счет образования комплексных ионов Fe(SCN)2+, Fe(SCN)+2
щелочь (амфотерные свойства гидроксида)
Выпадение осадка гидроксида алюминия при приливании первых порций щелочи и его растворение при дальнейшем приливании
щелочь, нагрев
Запах аммиака: NH4+ + ОН- 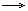 NH3
NH3 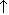 + Н20
+ Н20
Индикаторы: лакмус, метиловый оранжевый
красное окрашивание
красное окрашивание
Анион
Реактив
S042-
Ва2+
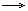 BaS04
BaS04 
N03-
1) добавить конц. H2SO4 и Си, нагреть "2) смесь
H2S04 +FeSO4