
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
а) Раствор от переработки кремнемышьяковых отвалов. В нем ~2 % WO3 от поступившего с основным раствором, т.е.
Содержание
Введение……………………………………………………...…….....4
1.Технологические расчёты………………………………………….7
1.1.Исходные данные………………………………………………….
1.2. Расчёт процесса очистки раствора…………………………...…8
1.2.1. Очистка раствора от кремнекислоты ……………….…….....11
1.2.2.Очистка раствора от мышьяка и фосфора …….…….…….…12
1.2.3.Очистка раствора от молибдена ……………………….…..…14
Заключение………………..……………………………….….......….17
Список литературы…………………………..…………………...…18
Введение
Растворы вольфрамата натрия, содержащие 80 - 150 г/л  , с целью получения триоксида вольфрама требуемой чистоты до настоящего времени преимущественно перерабатывали по традиционной схеме, которая включает: очистку от соединений элементов – примесей (Si, P, As, F, Mo); осаждение вольфрамата кальция (искусственного шеелита) с последующим его разложением кислотами и получением технической вольфрамовой кислоты; растворение вольфрамовой кислоты в аммиачной воде с последующей выпаркой раствора и кристаллизацией паравольфрамата аммония (ПВА); прокаливание ПВА с получением чистого триоксида вольфрама.
, с целью получения триоксида вольфрама требуемой чистоты до настоящего времени преимущественно перерабатывали по традиционной схеме, которая включает: очистку от соединений элементов – примесей (Si, P, As, F, Mo); осаждение вольфрамата кальция (искусственного шеелита) с последующим его разложением кислотами и получением технической вольфрамовой кислоты; растворение вольфрамовой кислоты в аммиачной воде с последующей выпаркой раствора и кристаллизацией паравольфрамата аммония (ПВА); прокаливание ПВА с получением чистого триоксида вольфрама.
Основной недостаток схемы – многостадийность, проведение большинства операций в переодическом режиме, длительность ряда переделов. Разработана и уже используется на предприятиях экстракционная и ионообменная технология перевода раствора 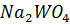 в растворы
в растворы 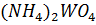 .
.
Очистка от примесей
Очистка от кремния. При содержании в растворах Si 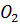 , превышающем 0,1 % от содержания
, превышающем 0,1 % от содержания 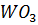 , необходима предварительная очистка от кремния. Очистка основана на гидролитическом разложении
, необходима предварительная очистка от кремния. Очистка основана на гидролитическом разложении 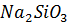 при кипячении раствора, нейтрализованного до pH = 8 – 9 с выделением кремниевой кислоты.
при кипячении раствора, нейтрализованного до pH = 8 – 9 с выделением кремниевой кислоты.
Растворы нейтрализуют соляной кислотой, добавляемой тонкой струйкой при перемешивании (во избежание местных перекислений) к нагретому раствору вольфрамата натрия.
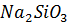 + 2
+ 2 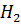 O = 2NaOH +
O = 2NaOH + 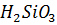
Очистка от фосфора и мышьяка. Для очистки от фосфат - и арсенат – ионов используют метод осаждения аммонийно – магниевых солей Mg( 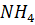 )P
)P 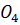 · 6
· 6 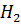 O и Mg(
O и Mg( 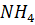 )As
)As 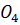 · 6
· 6 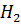 O. Растворимость этих солей в воде при 20°C 0,058 и 0,038 % соответственно. В присутствии избытка ионов
O. Растворимость этих солей в воде при 20°C 0,058 и 0,038 % соответственно. В присутствии избытка ионов 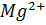 и
и 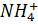 растворимость ниже.
растворимость ниже.
Осаждение примесей фосфора и мышьяка ведут на холоду:
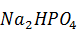 +
+ 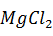 +
+ 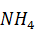 OH =
OH = 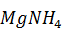 P
P 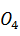 +2NaCL +
+2NaCL + 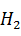 O,
O,
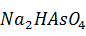 +
+ 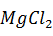 +
+ 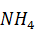 OH =
OH = 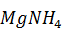 As
As 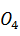 + 2NaCL +
+ 2NaCL + 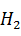 O.
O.
После длительного стояния (48ч) из раствора выпадают кристаллические осадки аммонийно – магниевых солей.
Очистка от фторид – ионов. При высоком содержании флюорита в исходном концентрате содержание фторид – ионов достигает 5 г/л. Растворы очищают от фторид–ионов осаждением фторидом магния из нейтрализованного раствора, в который добавляют Mg 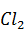 . Очистку от фтора можно сочетать с гидролитическим выделением кремниевой кислоты.
. Очистку от фтора можно сочетать с гидролитическим выделением кремниевой кислоты.
Очистка от молибдена. Растворы вольфрамата натрия необходимо очищать от молибдена в том случае, если его содержание превышает 0,1% от содержания 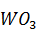 (т.е. 0,1 – 0,2 г/л). При концентрации молибдена 5-10 г/л выделение молибдена приобретает особое значение, так как имеет целью получение молибденового химического концентрата.
(т.е. 0,1 – 0,2 г/л). При концентрации молибдена 5-10 г/л выделение молибдена приобретает особое значение, так как имеет целью получение молибденового химического концентрата.
Распространённый способ состоит в осаждении из раствора малорастворимого трисульфида молибдена 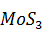 .
.
Известно, что при добавлении в растворы вольфрамата или молибдата натрия сернистого натрия образуются сульфосоли 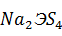 или оксосульфосоли
или оксосульфосоли 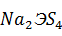 :
:
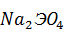 + 4NaHS =
+ 4NaHS = 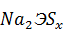
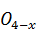 + 2NaOH.
+ 2NaOH.
Константа равновесия этой реакции для 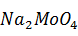 значительно больше, чем для
значительно больше, чем для 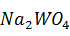 . Поэтому, если в раствор добавлено количество
. Поэтому, если в раствор добавлено количество 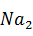 S, достаточное лишь для взаимодействия с
S, достаточное лишь для взаимодействия с 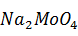 , то преимущественно образуется сульфосоль молибдена. При последующем подкислении раствора до pH = 2,5 -3,0 сульфосоль разрушается с выделением трисульфида молибдена:
, то преимущественно образуется сульфосоль молибдена. При последующем подкислении раствора до pH = 2,5 -3,0 сульфосоль разрушается с выделением трисульфида молибдена:
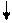
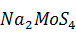 + 2HCL =
+ 2HCL = 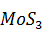 + 2NaCl +
+ 2NaCl + 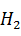 S.
S.
Оксосульфосоли разлагаются с выделением оксосульфидов. Вместе с трисульфидом молибдена соосаждается некоторое количество трисульфида вольфрама. Растворением сульфидного осадка в растворе соды и повторным осаждением трисульфида молибдена получают молибденовый концентрат с содержанием 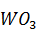 не более 2 % при потере вольфрама 0,3 – 0,5 % от исходного количества.
не более 2 % при потере вольфрама 0,3 – 0,5 % от исходного количества.
После частичного окислительного обжига осадка трисульфида молибдена (при 450 – 500°С) получают молибденовый химический концентрат с содержанием 50 – 52 % молибдена.
Недостаток способа осаждения молибдена в составе трисульфида – выделение сероводорода по реакции, что требует затрат на обезвреживание газов. Выделение трисульфида молибдена ведут из раствора, нагретого до 75 – 80°С. Операцию проводят в герметичных стальных реакторах, гуммированных или покрытых кислотоупорной эмалью. Осадки трисульфида отделяют от раствора фильтрацией на фильтр – прессе.
1.Технологические расчёты
1.1.Исходные данные
1.1.1 Состав спека, %: 25,21 Na2WO4, 0,03 Na2MoO4, 0,10
Na3PO4, 0,06 Na3AsO4, 1,15 Na2SO4, 3,00 Na2CO3, 0,11 Na2O, 0,54 Na2SiO3, 0,11 NaCl, остальное – нерастворимые соединения. Механические потери WO3 при выщелачивании 0,1 % от поступившего со спеком. Расчёт вести на объем раствора 800 дм3. Концентрацию WO3 в крепком растворе принять равной 155 г/дм3
1.1.2. Соляная кислота техническая, сорт первый. Массовая доля хлористого водорода 31,5 %.
1.1.3. Аммиачная вода из синтетического аммиака, сорт первый. Массовая доля аммиака (NH3) 25 %.
1.1.4. Аммоний хлористый технический. Массовая доля хлористого аммония 99,5 %.
1.2. Расчёт процесса очистки раствора
При выщелачивании спека растворимые компоненты примесей переходят в раствор пропорционально вольфрамату натрия. Зададимся концентрацией WO3 в растворе 155 г/дм3 и рассчитаем содержание в этом растворе примесей. Примем объем раствора 800 дм3, тогда масса WO3 в нем
155 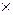 800/1000 = 124 кг
800/1000 = 124 кг
Расчет концентраций примесей и их масс в 800 дм3 раствора приводится в таблице 1.
На очистку кроме основного поступают оборотные растворы:
а) Раствор от переработки кремнемышьяковых отвалов. В нем ~2 % WO3 от поступившего с основным раствором, т.е.
124 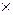 0,02 = 2,48 кг
0,02 = 2,48 кг
Примем концентрацию этого раствора вдвое меньше, чем основного, т.е.
155/2 = 77,5 г/дм3
Объем этого раствора:
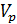 =
= 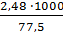 = 32
= 32 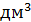
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|