
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Рис. 54. Модель молекулы уксусной (этановой) кислоты: 1 — шаростержневая; 2 — масштабная
Рис. 54. Модель молекулы уксусной (этановой) кислоты: 1 — шаростержневая; 2 — масштабная
Уксусная кислота — хороший растворитель многих органических соединений, применяется при крашении, в кожевенном производстве, лакокрасочной промышленности (рис. 55). Кроме этого, уксусная кислота является исходным сырьем для производства многих важных в техническом отношении органических соединений: искусственных волокон, ядохимикатов, кино- и фотопленок и т. д. Уксусная кислота чрезвычайно опасна при попадании на кожу, поэтому необходимо соблюдать меры безопасности при работе с уксусной эссенцией.

Рис. 55. Применение уксусной кислоты: 1 — консервирование; 2 — производство искусственных волокон, тканей; 3 — приправа к пище; 4—8 — производство органических соединений (пестицидов 4, лаков 5, красок 6, фотопленки 7, клея 8)
С увеличением относительной молекулярной массы в гомологическом ряду предельных одноосновных карбоновых кислот увеличиваются их плотность, температуры кипения и плавления, уменьшается растворимость в воде.
Высшие карбоновые кислоты, также называемые жирными (догадались почему), являются твердыми веществами. Это, например, пальмитиновая С15Н31СООН (рис. 56, 1) и стеариновая С17Н35СООН кислоты (рис. 56, 2).
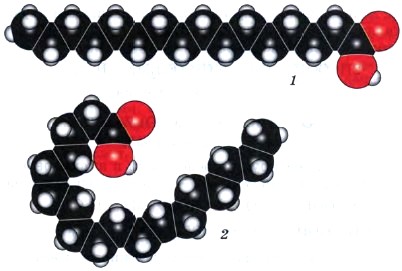
Рис. 56. Масштабные модели молекул: 1 — пальмитиновой кислоты; 2 — стеариновой кислоты
Химические свойства карбоновых кислот определяются в первую очередь их принадлежностью к типу кислот вообще. Подобно неорганическим кислотам, карбоновые кислоты являются электролитами, правда очень слабыми, а потому диссоциируют обратимо:
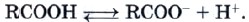
Водные растворы карбоновых кислот изменяют окраску индикаторов.
С увеличением углеводородного радикала происходит уменьшение степени электролитической диссоциации.
Как и неорганические кислоты, карбоновые взаимодействуют с металлами, основными и амфотерными оксидами, основаниями, амфотерными гидроксидами и солями.
Так, муравьиная и уксусная кислоты взаимодействуют с металлами, стоящими в электрохимическом ряду напряжений до водорода:
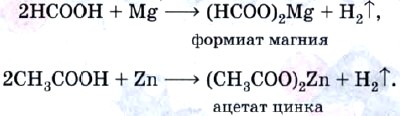
Эти кислоты реагируют с основными и амфотерными оксидами с образованием солей — формиатов и ацетатов:
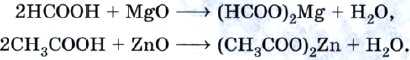
Аналогично муравьиная и уксусная кислоты взаимодействуют с основаниями и амфотерными гидроксидами:
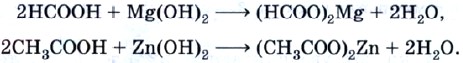
Взаимодействуют эти кислоты с солями более слабых кислот. Реакции идут до конца, если образуется осадок или газ:
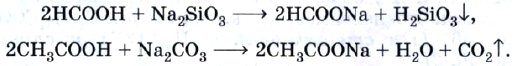
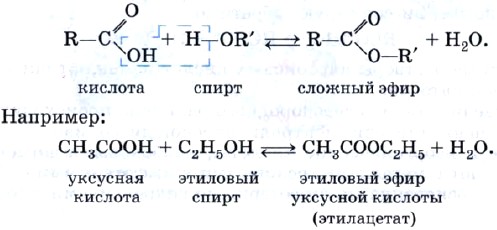
Органические кислоты, как вы уже знаете, вступают в реакцию этерификации со спиртами, образуя сложные эфиры, согласно уравнению
Новые слова и понятия
1. Карбоксильная группа.
2. Карбоновые кислоты. Предельные одноосновные карбоновые к
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|