
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Запишите тему в тетрадь и ответьте на вопросы
| № | ФИ обучающегося | 16.04 Конс. +2 п. вопр. | 24.04 П.р.3 | 27.05 тест | 2.06 Конс + задача | 3.06 Задача СхНуОz | 8.06 К.р.3 | 2 полуг. |
| Берлизев Виталий Владимирович | н/а | |||||||
| Бредихин Денис Дмитриевич | н/а | |||||||
| Долгих Иван Сергеевич | н/а | |||||||
| Долгих Сергей Сергеевич | н/а | |||||||
| Зоря Артём Русланович | н/а | |||||||
| Лавриненко Станислав Олегович | + | + | + | + | + | н/а | ||
| Матузов Сергей Владимирович | + | н/а | ||||||
| Мишин Виктор Романович | н/а | |||||||
| Старцев Никита Игоревич | + | + | + | + | + | н/а | ||
| Усатов Игорь Максимович | н/а | |||||||
| Черников Данил Андреевич | н/а | |||||||
| Чупрынов Максим Владимирович | н/а | |||||||
| Чуркин Александр Евгеньевич | + | + | + | н/а | ||||
| Шеховцов Семен Анатольевич | н/а |
16.04.20
Запишите тему в тетрадь и ответьте на вопросы
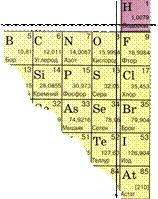 Тема. Общая характеристика неметаллов. Окислительно-восстановительные свойства неметаллов
Тема. Общая характеристика неметаллов. Окислительно-восстановительные свойства неметаллов
Металлы располагаются в основном в конце малых и больших периодов периодической системы химических элементов.
Окислительные и восстановительные свойства неметаллов.Число электронов на внешних уровнях неметаллов равно номеру группы. Для завершения внешних электронных уровней атомы неметаллов присоединяют электроны и являются окислителями.
Активнее всех неметаллов присоединяет электроны атом фтора. Он является самым сильным окислителем. У остальных неметаллов эта способность уменьшается в соответствии с электроотрицательностью:
F, O, Cl, N, I, S, C, P, H, Si
 Уменьшение окислительной способности
Уменьшение окислительной способности
Фтор не проявляет восстановительных свойств. Кислород только в соединениях со фтором является восстановителем.
Химические свойства неметаллов:
а) Взаимодействуя с металлами, неметаллы образуют соединения с ионной связью:
Cl2 + 2Na = 2NaCl;
б) В определённых условиях неметаллы взаимодействуют между собой, образуя соединения с ковалентной связью: Si + 2F2 = SiF4;
в) С водородом неметаллы образуют летучие соединения: S + H2 = H2S;
г) С кислородом неметаллы образуют кислотные оксиды: S + O2 = SO2.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|