
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Анионы 2-ой аналитической группы
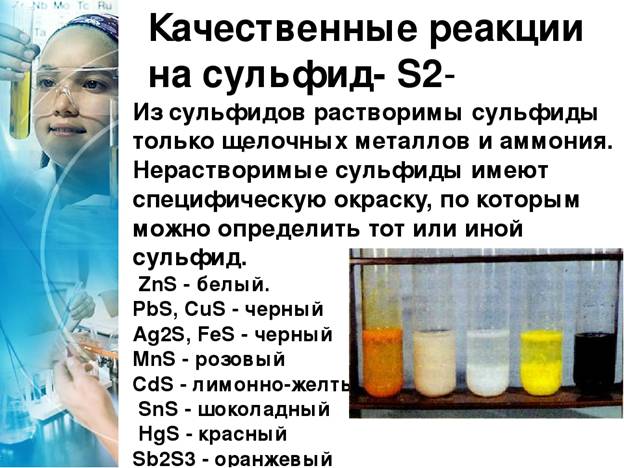
Анионы 2-ой аналитической группы
Ко второй группе относятся анионы бескислородных кислот: хлорид-ион Cl-, бромид-ион Br-, йодид-ион I-, сульфид-ион S2-. Они дают нерастворимые в воде и разбавленной азотной кислоте остатки солей серебра. Соли серебра в присутствии азотной кислоты являются групповым реактивом.
Применение в медицине и фармации
Хлориды щелочных и щелочноземельных металлов – хлорид натрия, калия, кальция – широко используются в виде инъекционных растворов при различных заболеваниях. Бромиды калия, натрия и аммония назначают в микстурах как успокаивающие и регулирующие деятельность ЦНС средства.
Йодиды калия и натрия применяют в микстурах при заболеваниях щитовидной железы, бронхиальной астме, воспалительных процессах, грибковых заболеваниях. Элементарный йод применяют при заболеваниях щитовидной железы, атеросклерозе, как антисептическое и раздражающее средство, в виде раствора Люголя. Йодид калия используют при лечении заболевания горла.
Действие группового реактива
Нитрат серебра в присутствии азотной кислоты осаждает из растворов осадки солей серебра с анионами 2-ой группы:
AgNO3+KCl→ AgCl↓ +KNO3
AgNO3+KBr→ AgBr↓ +KNO3
AgNO3+KI→ AgI↓ +KNO3

Анионы 3-й аналитической группы
К третьей группе анионов относятся нитрат-ион NO3-, нитрит-ион NO2-, ацетат-ион СН3СОО-. Группового реагента на анионы третьей группы нет.
Частные реакции нитрат-иона NO3 -
1. Дифениламин (С6Н5)2NH с нитрат-ионом образует интенсивно-синее окрашивание.
Опыт. На чистое сухое часовое стекло поместите 4-5 капель раствора дифениламина в концентрированной серной кислоте. Внесите туда же стеклянной палочкой каплю испытуемого раствора и перемешайте. В присутствии аниона NO3- появляется интенсивно-синяя окраска раствора вследствие окисления дифениламина. Аналогичное окрашивание дает и анион NO2-.

Частные реакции нитрит-иона NO2 -
Описанные реакции для аниона NO3- характерны также и для аниона NO2-.
Анион NO2- можно отличить от аниона NO3- следующими реакциями:
Кислоты разлагают все нитриты с выделением окислов азота:
2NaNO2 + H2SO4 = Na2SO4 + 2HNO2
2HNO2 = NO2 + NO +H2O
Реакции ацетат-ионов СН3СОО -
1. Серная кислота, взаимодействуя с ацетатами, вытесняет из них свободную уксусную кислоту, которая, улетучиваясь при нагревании, придает раствору специфический запах уксуса.
Опыт. В пробирку поместить 5-6 капель раствора ацетата натрия и добавьте 2 капли концентрированной серной кислоты. Нагреть. Обнаружьте уксусную кислоту по запаху.
2. При взаимодействии спиртов с растворами ацетатов образуются эфиры, которые узнаются по запаху:
2CH3COONa + H2SO4 ®=Na2SO4 + 2CH3COOH
CH3COOH + C5H11OH 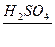 = CH3COOC5H11 + H2O
= CH3COOC5H11 + H2O
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|