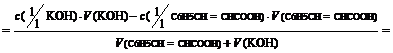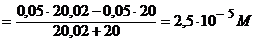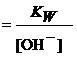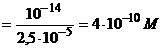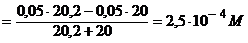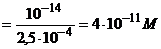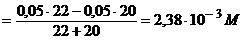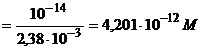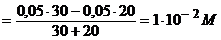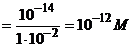- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Таблица 1. Продолжение таблицы 1
Российский Химико-Технологический Университет им. Д. И. Менделеева
Кафедра аналитической химии.
Расчётно графиеская работа:
«Титрование раствора слабой кислоты раствором сильного основания».
Выполнил:
студент группы
 Вариант 3. Титрование раствора слабой кислоты раствором сильного основания
Вариант 3. Титрование раствора слабой кислоты раствором сильного основания
Задание. Рассчитать и построить кривую титрования 20 мл 0, 05 М раствора C6H5CH=CHCOOH (Кα = 3. 7∙ 10− 5). Титрант: раствор KOH 0, 05 M.
Пояснения: Кривую титрования строят по расчетным точкам. Расчетные точки должны соответствовать следующим этапам титрования:
1. Начальная точка
2. Область до точки эквивалентности
3. Точка эквивалентности (ТЭ)
4. Область после точки эквивалентности
Расчет приводят в виде таблицы:
Таблица 1
Расчет кривой титрования 20 мл 0, 05 М раствора C6H5CH=CHCOOH 0, 05 М раствором KOH
| Этап титрования | Оттитровано, кислоты, % | Объем добавленного ттитранта, мл | Общий объем смеси в колбе для титрования, мл | Состав раствора | Расчетная формула | рН | ||||
|
|
| C6H5CH=CHCOOH | [H+] = 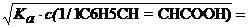
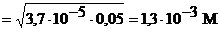
| 2, 9 | ||||||
|
Продолжение таблицы 1 | ||||||||||
|
|
|
| C6H5CH=CHCOOH + C6H5CH=CHCOOK | [H+]=
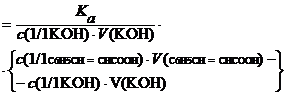 [H+] =
[H+] = 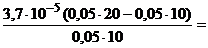
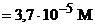
|
4, 4 | |||||
| 99, 0 |
19, 8 |
39, 8 | C6H5CH=CHCOOH + C6H5CH=CHCOOK | [H+] 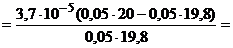
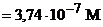
|
6, 4 | |||||
| 99, 9 |
19, 98 |
39, 98 | C6H5CH=CHCOOH + C6H5CH=CHCOOK | [H+] = 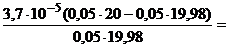
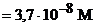
|
7, 4 | |||||
|
|
| C6H5CH=CHCOOK | [OH-] =
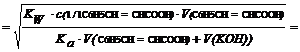 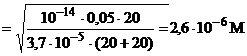 [H+] =
[H+] =
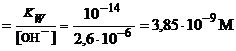
|
8, 4 | ||||||
| Окончание таблицы 1 | ||||||||||
|
| Избток титранта 0, 1% | 20, 02 |
40, 02 |
C6H5CH=CHCOOH + KOH | [OH-] =
[H+] [H+] | 9, 4 | ||||
| Избток титранта 1% | 20, 2 |
40, 2
|
C6H5CH=CHCOOK + KOH | [OH-] =
[H+] | 10, 4 | |||||
| Избток титранта 10% |
|
C6H5CH=CHCOOH + KOH | [OH-] =
[H+] | 11, 4 | ||||||
| Избток титранта 50% |
|
C6H5CH=CHCOOK + KOH | [OH-] [H+] | |||||||
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|