
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
А25. Конечным веществом в цепочке превращений на основе азота
Единый государственный экзамен по химии
Тема «Неметаллы»
Часть 1
А1. В каком случае представлены химические знаки наиболее активных неметаллов, расположенных в порядке усиления их неметалличности:
А) N, C, B; В) F, S, Cl; Б) Сl, O, F; Г) Si, B, H.
А2. Бор имеет кристаллическую решетку:
А) атомную; В) ионную; Б) молекулярную; Г) металлическую.
А3. Из предложенных ниже групп формул водородных соединений неметаллов выберите ту, которая включает формулы веществ со свойствами кислот, расположенных в порядке увеличения их силы:
А) CH4, NH3, H2O; В) H2S, PH3, SiH4; Б) HBr, HCl, HI; Г) HCl, HBr, HI.
А4. К солеобразующим оксидам относится:
А) CO; В) NO; Б) N2O; Г) N2O5.
А5. Какой высший оксид неметалла 4 периода обладает наименее ярко выраженными кислотными свойствами: А) SeO3; В) As2O3; Б) Mn2O7; Г) As2O5.
А6. Выберите наиболее сильную кислоту:
А) H3PO4; Б) H3AsO4; В) H3SbO4.
А7. Из предложенных ниже групп формул водородных соединений неметаллов выберите ту, которая содержит формулы веществ со свойствами оснований:
А) CH4, NH3, H2O; В) NH3, PH3; Б) SiH4, HCl; Г) H2O, H2S, H2Se.
А8. Выберите наиболее сильную кислоту:
А) HClO; В) HClO3; Б) HClO2; Г) HClO4
А9. Кислотные свойства от оксида фосфора (V) к оксиду серы (VI) увеличиваются по следующим причинам:
А) увеличение радиуса атома Б) увеличение положительного заряда неметалла;
В) уменьшение электроотрицательности неметалла.
А10. По агрегатному состоянию бром является:
А) газом Б) жидкостью; В) твёрдым веществом.
А11. Реакционная способность галогенов – простых веществ – в подгруппе сверху вниз с ростом порядкового номера:
А) уменьшается; В) уменьшается, а затем возрастает; Б) увеличивается; Г) не изменяется.
А12. Только восстановительные свойства проявляет кислота:
А) HClO; В) HCl; Б) HClO2; Г) HClO4.
А13. Соляная кислота - это:
А) водный раствор хлора; Б) тяжелая маслянистая жидкость с желтоватым оттенком;
В) водный раствор хлороводорода; Г) бесцветные кристаллы.
А14. Температуры плавления и кипения галогенов – простых веществ – в подгруппе сверху вниз с ростом порядкового номера:
А) уменьшаются; В) уменьшаются, а затем возрастают; Б) увеличиваются Г) не изменяются.
А15. Свободный хлор Cl2 может выделиться в результате реакции:
А) HCl + F2 → В) HCl + Mg → Б) HCl + Br2 → Г) HCl + MgO →
А16. При добавлении раствора йодида натрия к раствору нитрата серебра образуется осадок:
А) жёлтого цвета; Б) желтоватого цвета; В) белого цвета.
А17. Наличие в растворе сульфат-ионов можно определить с помощью раствора:
А) индикатора; В) хлорида бария; Б) гидроксида калия; Г) соляной кислоты.
А18. В водном растворе какой соли среда щелочная:
А) хлорид аммония; В) сульфат бария; Б) карбонат калия; Г) нитрат магния.
А19. Коэффициент перед формулой окислителя в равнении реакции, схема которой NH3 + O2 → NO + H2O равен: А) 1; В) 3; Б) 2; Г) 5.
А20. Для увеличения скорости реакции в 81 раз (температурный коэффициент равен 3), температуру газообразной смеси следует повысить на: А) 40º С; В) 20º С; Б) 30º С; Г) 50º С
А21. Химическое равновесие реакции N2(газ) + O2(газ) ⇋ 2NO(газ)–Q смещается в сторону образования продукта реакции при:
А) понижении температуры; В) повышении температуры; Б) уменьшении давления; Г) увеличении давления.
А22. Аллотропными формами одного и того же элемента являются:
А) кислород и озон; В) вода и лед; Б) кварц и кремень; Г) сталь и чугун.
А23. В реакции цинка с концентрированной азотной кислотой окислителем является:
А) Zn2+; В) H+; Б) NO3-; Г) Zn0.
А24. В периодической системе химических элементов Д. И. Менделеева неметаллы расположены в углу:
А) правом верхнем; В) левом верхнем; Б) правом нижнем; Г) левом нижнем.
А25. Конечным веществом в цепочке превращений на основе азота
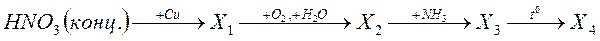
А) нитрат аммония; В) оксида азота (IV); Б) оксида азота (I); Г) азотная кислота.
А26. Для того, чтобы идентифицировать углекислый газ с помощью раствора хлорида кальция, в последний надо добавить: А) NaCl; В) HCl; Б) NaOH; Г) Ca(NO3)2.
А27. Силан образуется в результате реакции:
А) Si + H2 →; В) Mg2Si + HCl (раствор)→; Б) SiO2 + H2 →; Г) Si +NaOH (раствор)→.
А28. Для проведения опыта необходимо взять некоторое количество питьевой соды, на склянках же с реактивами указаны только формулы веществ. Склянку с какой этикеткой необходимо взять:
А) Na2CO3; В) KHCO3; Б) K2CO3; Г) NaHCO3.
А29. При обработке карбоната металла кислотой образуется:
А) углерод; В) угарный газ; Б) кислород; Г) углекислый газ.
А30. Вещество А в цепи превращений H2S→ S→ A→ SO3 → Na2SO4
А) оксид серы (IV); В) сероводород; Б) вода; Г) сернистая кислота.
А31. Свойство концентрированной серной кислоты отражает уравнение:
А) C + H2SO4 → CO2 + SO2 + H2O; Б) Zn + H2SO4 → ZnSO4 + H2;
В) Ca + H2SO4 → CaSO4 + H2; Г) Al2O3 + H2SO4 → Al2(SO4)3 + H2O.
А32. Химическая связь в молекуле фтороводорода:
А) ковалентная полярная; В) ионная; Б) ковалентная неполярная; Г) водородная.
А33. При обжиге пирита получается: А) сера и оксид железа (III); Б) сернистый газ и оксид железа (III); В) сернистый газ и оксид железа (II); Г) сернистый газ и железо.
А34. Кислые соли сероводородной кислоты называются:
А) гидросульфиды; В) гидросульфаты; Б) гидросульфиты; Г) сульфиды.
А35. Соляная кислота НЕ взаимодействует с:
А) магнием; В) гидроксидом калия; Б) ртутью Г) карбонатом натрия
Часть 2
В1. Какова массовая доля серы в сульфиде магния? Ответ: _____.
В2. Высший оксид фосфора имеет формулу____________ и при растворении в воде даёт____________(формула).
В3. Самые активные неметаллы находятся в ________группе, их высшая степень окисления равна________, по отношению к металлам они выполняют функцию_____________.
В4. В сокращённом ионном уравнении реакции серной кислоты с нитратом бария сумма коэффициентом равна_______________.
В5. Запишите число нейтронов в ядре атома фосфора-31. Ответ: _____.
В6. Соединения азота с металлами называются ____________.
В7. Что такое аллотропия (напишите определение)?
В8. Фенолфталеин в водном растворе аммиака приобретает ____________окраску.
В9. При действии электрического тока на смесь азота и кислорода можно получить соединение ________.
В10. Доказать наличие в растворе нитратов (например, нитрата натрия) можно с помощью реакций_________.
Часть 3
С1. При обработке фосфида кальция водой выделяется газ фосфин – аналог аммиака. Какой объём фосфина (измеренный при нормальных условиях) можно получить из 18, 2 г фосфида кальция?
С2. При кипячении 100 см3 раствора серной кислоты, содержащего 10% H2SO4 по массе и имеющего плотность 1, 07 г/см3, выпарили 50 мл воды. Опрделеите массовую долю серной кислоты в полученном растворе. Сколько моль гидроксида калия необходимо для полной нейтрализации полученного раствора H2SO4?
С3. При нагревании 126, 4 г перманганата калия получили 6, 72 л кислорода. Какова массовая доля неразложившегося KMnO4?
С4. Первой стадией получения азотной кислоты в промышленности является окисление аммиака кислородом. Рассчитайте объём воздуха (н. у. ), который необходим для получения 1 м3 (н. у. ) оксида азота (II) из аммиака, если выход продукта 75%.
С5. Реакция образования фосгена обратима:
СО(газ) + Сl2 (газ) ⇋ COCl (газ) + Q
Перечислите все условия, при которых происходит смещение равновесия в этой системе в сторону исходных веществ. Объясните действие каждого из условий.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|