
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Тема: «Основные законы идеальных газов»
Тема: «Основные законы идеальных газов»
Задача 1. Параметры смеси газов. Истечение газов
В помещении компрессорной станции объемом V произошла разгерметизация трубопровода, по которому транспортируется горючий газ под давлением P1 при температуре Т1 через образовавшееся в трубопроводе сквозное отверстие площадью f газ выходит в помещение.
Рассчитать, через какое время τ во всем объеме компрессорной станции может образоваться взрывоопасная смесь, а также среднюю молекулярную массу, плотность, удельный объем и изобарную удельную массовую теплоемкость смеси, если ее температура Т = 293 К, а давление Р = 100 кПа. Коэффициент расхода отверстия ξ = 0, 7. Воздухообмен не учитывается. Данные, необходимые для расчетов, приведены в таблице 1.
Таблица 1
| Вариант | 1, 11 | 2, 12 | 3, 13 | 4, 14 | 5, 15 | 6, 16 | 7, 17 | 8, 18 | 9, 19 | 10, 20 |
| V∙ 10-2, м3 f∙ 10 4, м2 | 4, 2 | 5, 9 | 5, 0 | 2, 0 | 5, 1 | 4, 1 | 5, 0 | 6, 0 | 4, 2 | 1, 5 |
| Вариант | 10, 20 | 9, 19 | 8, 18 | 7, 17 | 6, 16 | 5, 15 | 4, 14 | 3, 13 | 2, 12 | 1, 11 |
| Р1, МПа Т1, К | 0, 5 | 0, 7 | 0, 7 | 1, 6 | 1, 0 | 1, 6 | 0, 3 | 0, 5 | 0, 2 | 0, 8 |
| Газ | Бутан | Этан | Пропан | Метан | Этилен | Водород | Бутилен | Ацетилен | Аммиак | Пропилен |
Указания к решению задачи
Время образования взрывоопасной концентрации
τ = М1/G1,
где М1 – масса газа в помещении при концентрации, равной нижнему концентрационному пределу воспламенения (НКПВ), кг;
G1 – расход газа через отверстие в трубопроводе, кг/с.
Из уравнения состояния
М1 = pr1V/R1T,
Где p, V, T – соответственно, давление, объем и температура смеси (данные по условию); r1 – значение НКПВ газа в объемных долях (приложение 1); R1 = 8314/μ 1 – газовая постоянная, Дж/(кг∙ К); μ 1 – молекулярная масса газа (приложение 1).
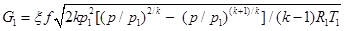 ,
,
если 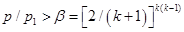 .
.
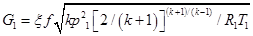
если 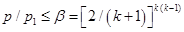 .
.
k – показатель адиабаты (приложение 1).
Молекулярная масса смеси:
μ см = rμ + r1μ 1,
где μ – молекулярная масса воздуха (приложение 1);
r = 1– r1 – объемная доля воздуха в смеси
Удельная газовая постоянная смеси:
Rсм = 8314/μ см
Плотность смеси:
ρ см = p/RсмT
Удельный объем смеси:
ν см = RсмT/p
Изобарная теплоемкость смеси:
Сpсм = Cpg – Cp1g1,
где Cp и Cp1 – соответственно массовая удельная теплоемкость воздуха и газа, Дж/(кг∙ К); g и g1 – соответственно, массовые доли воздуха и газа
g = μ r/μ см; g1 = μ 1r1/ μ см
Сp = μ Cp/μ ; Сp1 = μ 1Cp1/μ 1
μ Cp и μ 1Cp1 – соответственно мольная теплоемкость воздуха и газа, Дж/(моль∙ К) (приложение 1).
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|