
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Задание на 18сентября 2021г. (1пара занятий)
Задание на 18сентября 2021г. (1пара занятий)
Тема:
Методы контроля над процессом горения
Реакции горения компонентов газообразного топлива
Задание:
1. Изучить предложенную лекцию.
- Ответить на контрольные вопросы:
2. 1 Как определить эффективность сжигания газа?
2. 2 Охарактеризуйте видимые признаки нарушения процесса горения.
2. 3 Контроль процесса горения с помощью газоанализатора.
2. 4 Что необходимо помнить для правильного ведения процесса горения?
2. 5 Анализ по цвету дыма из дымовой трубы.
2. 6 Напишите основные реакции горения топлива.
2. 7 Сделайте вывод по пройденной теме.
Лекция
Методы контроля над процессом горения
Для оценки эффективности сжигания горючих газов и принятия мер по устранению недостатков большое значение имеет проведение быстрого и точного анализа состава продуктов сгорания. По составу продуктов сгорания можно оценить полноту сгорания газа, коэффициент избытка воздуха, потери теплоты от химической неполноты сгорания и с уходящими дымовыми газами. Для обеспечения высокого качества сжигания горючих газов в первую очередь следует применять газогорелочные устройства серийного производства, прошедшие Государственные испытания и имеющие технический паспорт с указанием рабочих параметров газа.
Работу газогорелочного устройства оценивают следующим методом: по видимым признакам, проведением анализа дымовых газов (продуктов сгорания) и автоматическими газоанализаторами. К видимым признакам нарушения нормального процесса относятся:
● изменение формы и размеров газового факела по сравнению с оптимальными параметрами, установленными для газоиспользующей установки;
● изменение цвета факела, появление коптящего пламени;
● усиление шума факела по сравнению с нормальным шумом при оптимальной работе;
● появление признаков отрыва и проскока пламени.
Однако видимые признаки не могут дать количественной оценки полноты сгорания газа.
Для точной оценки процесса горения необходимо провести анализ продуктов сгорания (дымовых газов). Для анализа компонентного состава используют хроматографический метод. Этот анализ сухих охлаждённых продуктов сгорания проводится с целью определения в них углекислого газа, азота, кислорода, окиси углерода и водорода. Для определения состава продуктов сгорания используют хроматографы и газоанализаторы, основанные на избирательном поглощении отдельных компонентов продуктов сгорания поглотительными растворами.
Перечисленные методы контроля состава продуктов сгорания применяются периодически и связаны с затратами значительного времени. Для оперативного контроля состава дымовых газов применяют автоматические газоанализаторы непрерывного действия. Для измерения объёмной концентрации кислорода в дымовых газах котельных установок применяют стационарный автоматический газоанализатор МН-5110Т. Действие газоанализатора основано на использовании парамагнитных свойств кислорода. Газоанализатор регистрирует содержание кислорода в двух точках (с двух сторон котла). Для непрерывного измерения концентрации кислорода в топочных газах в пределах 0 - 10% (по объёму) применяют газоанализатор МН-5106.
Для непрерывного автоматического измерения содержания углекислого газа применяют газоанализатор ТП-2221М. Измерение углекислоты в этом приборе основано на отличии теплопроводности углекислоты по сравнению с теплопроводностью других газов.
Для правильного ведения процесса горения необходимо помнить:
1. Чем больше процент углекислого газа СО2, тем меньше избыток воздуха в топке и тем меньше расход воздуха на горение топлива.
2. Если стрелка газоанализатора СО+Н2 находится на нуле, то горение в топке полное. Чем сильнее отклоняется стрелка вправо, тем больше содержание СО+Н2, тем больше неполнота горения и тем больше недостаток воздуха в топке.
Самое наивыгоднейшее горение будет при наибольшем проценте СО2, при котором горение остаётся полным, то есть когда стрелка указателя СО+Н2 стоит на нуле.
Если имеется газоанализатор с содержанием СО2, то устанавливается самый выгодный процент СО2. В этом случае значение имеет контроль за полнотой сгорания по цвету дыма, особенно при сжигании газообразного топлива.
Вывод. Необходимо добиваться более высокого процента СО2, при котором горение остаётся полным, не допуская потемнения в трубе отходящих дымовых газов.
О качестве горения газа также можно судить по цвету его пламени и цвету дыма в дымовой трубе.
По цвету дыма. При полном сгорании образуются водяные пары и углекислый газ, следовательно, при полном сгорании дыма из трубы видно не будет, а в холодное время года будет виден водяной пар. При избытке воздуха наблюдается то же самое явление. При недостатке воздуха или понижении температуры в топке, так как наблюдается неполное сгорание, из трубы может показаться чёрный дым. Значит, по цвету дыма можно определить качество горения только при неполном горении.
Реакции горения компонентов газообразного топлива
1. Горение углерода.
С+О2=СО2+8100ккал (34000кДж)
При полном сгорании 1кг углерода выделяется 8100ккал (34000кДж) тепла. При недостатке кислорода окисление углерода может быть неполным и конечным продуктом будет окись углерода:
2С+О2=2СО+2760ккал(11699кДж)
Выделяющееся при этом тепло составляет около 30% тепла, выделенного при полном окислении углерода.
2. Горение водорода: 2Н2+О2=2Н2О+28640ккал (120600кДж)
При сгорании 1кг водорода выделяется 28640 ккал тепла. Эта величина представляет собой низшую теплоту сгорания водорода без учёта теплоты парообразования. Жаропроизводительность водорода 2235оС.
3. Горение метана:
При достаточном количестве воздуха в топке метан сгорает, образуя водяные пары и углекислый газ. При таком горении выделяется 8555ккал тепла с 1м3 воздуха, то есть:
СН4+ 2О2=2Н2О+СО2
Одна молекула метана, соединяясь с двумя молекулами кислорода, образует две молекулы водяных паров и одну молекулу углекислого газа. Такое горение называется полным.
При неполном горении:
1. Часть метана сгорает, образуя водяные пары и окись углерода вместо углекислого газа: СН4+ 1, 5О2=2Н2О+СО;
2. Часть метана сгорает, образуя водяные пары и частицы твёрдого углерода - сажу СН4+ О2=2Н2О+С,
Из дымовой трубы может показаться чёрный дым и на поверхности нагрева котла осесть сажа.
3. Часть метана не сгорит совсем и уйдёт вместе с отходящими газами в трубу.
4. Горение тяжёлых углеводородов.
Горение такое же, как и метана, только для сгорания одной молекулы этих газов требуется больше кислорода, так как эти молекулы содержат в себе большее количество водорода и углерода - больше горючего вещества.
С3Н8+ 5О2=3Н2О+4СО2, при этом выделяется 21800ккал тепла.
Реакция горения любого из углеводородов типа CmHn может быть выражена следующим уравнением:
CmHn + (m + 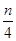 ) О2 = mCO2+
) О2 = mCO2+ 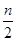 H2O
H2O
Вывод. При неполном горении газообразного топлива выделение тепла в топке будет меньше, чем при полном горении. Если осядет сажа на поверхности нагрева котлов, то перерасход топлива увеличивается за счёт того, сажа является плохим проводником. Она уменьшает отдачу тепла котлу и увеличивает потери тепла с отходящими газами. Следовательно, сжигая топливо, нужно добиваться полного сгорания топлива. Для этого следует подавать в горелку и топку достаточное количество воздуха.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|